Professional Documents
Culture Documents
Bab Ii
Uploaded by
Ivhen AninOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Bab Ii
Uploaded by
Ivhen AninCopyright:
Available Formats
BAB II
TINJAUAN PUSTAKA
II.1 Tinjauan Tentang Faloak
Faloak merupakan tanaman obat yang termasuk dalam family Malvaceae.
Pohon faloak tumbuh di daerah dengan iklim tropis pada ketinggian 0-900 meter
di atas permukaan laut. Pohon faloak tumbuh tersebar di Australia (Australia
Barat, Queendsland, New South Wales) dan Papua Nugini. Namun pohon faloak
banyak ditemukan di pulau Timor, Nusa Tenggara Timur (NTT) (Siswadi et al,
2013).
II.1.1 Nama Tanaman
Nama Indonesia : Faloak
Nama asing : Red-fruit Kurrajong
Sinonim : Sterculia quadrifida R.Br (1844)
Gambar 1. Pohon faloak
Dalam sistem klasifikasi tumbuhan, tanaman faloak diklasifikasikan
sebagai berikut :
Kingdom : Plantae
Division : Angiospermae
Ordo : Malvales
Family : Malvaceae
Genus : Sterculia
Species : Sterculia quadrifida R.Br (1844) (Siswadi et al, 2013)
II.1.2 Morfologi Tanaman
Tanaman faloak terdiri dari akar, batang, daun, bunga, buah dan biji.
Pohon faloak dapat tumbuh mencapai tinggi lebih dari 15 meter. Tanaman ini
memiliki kulit batang berwana abu-abu terang dan mengeluarkan getah transparan
ketika di sayat. Tanaman faloak berbunga pada bulan April hingga Juni dan
berbuah pada bulan Juni hingga Oktober setiap tahun. Pangkal daun tumbul
dengan ujung daun yang meruncing. Buah berwarna kuning, orange hingga merah
dengan permukaan luar ditutupi bulu-bulu halus rapat yang ketika matang akan
terbuka, berisi 4-8 biji berwarna hitam mengkilap. Biji berbentuk elips dengan
ukuran kira-kira 10 mm, dapat di makan dan memiliki rasa seperti kacang. Di
pulau Timor, faloak dapat ditemukan di semua daerah, disamping itu, berdasarkan
survey vegetasi tercatat bahwa faloak dapat pula ditemukan di pulau Sumba dan
daerah Ngada, Pulau Flores (Russell-Smith et al, 2006). Di Timor Leste tanaman
faloak dikenal dengan nama Komila (Siswadi et al, 2013).
II.1.3 Kandungan Kimia dan Kegunaan
Berdasarkan penelitian yang dilakukan oleh Siswadi et al (2013),
ditemukan bahwa kulit pohon faloak mengandung senyawa fenolik, flavonoid,
alkaloid dan terpenoid. Sedangkan berdasarkan penelitian yang dilakukan oleh
Ranta et al (2012) berhasil diisolasi senyawa 3-hydroxyoctadecanoic acid yang
berkhasiat sebagai antifungi terhadap jamur C.Albicans.
Bagian dari faloak yang digunakan sebagai obat herbal oleh masyarakat
khususnya di pulau Timor kulitnya. Kulit batang faloak dipercaya dapat
mengobati beberapa penyakit seperti hepatitis, kanker, gangguan saluran
pencernaan, diabetes, reumatik, dan sebagai penguat sel darah merah. Umumnya,
masyarakat tradisional mengkonsumsi kulit batang faloak dengan cara direbus,
baik tanpa tambahan bahan lain atau dengan tambahan misalnya rempah-rempah
seperti kunyit maupun kencur (Siswadi et al, 2013).
II.2 Radikal Bebas
Selama berjalannya metabolisme, terjadi pembentukan beberapa oksidan
kuat, baik di sel darah maupun di kebanyakan sel lain tubuh. Oksidan ini dikenal
sebagai radikal bebas. Radikal bebas adalah atom atau sekelompok atom yang
memiliki elektron tak berpasangan. Radikal bebas juga dapat terbentuk dari
senyawa lain yang sebenarnya bukan radikal bebas. Misalnya, hidrogen peroksida
(H
2
O
2
), ozon, dan lain-lain. Berbagai oksidan ini disebut sebagai spesies oksidan
reaktif (reactive oxygen species, ROS). (Murray et al, 2006).
Adanya elektron tidak berpasangan menyebabkan senyawa tersebut sangat
reaktif mencari pasangan dengan cara menyerang dan mengikat elektron molekul
yang berada di sekitarnya. Jika elektron yang terikat oleh senyawa radikal bebas
tersebut bersifat ionik, dampak yang timbul memang tidak begitu berbahaya.
Akan tetapi, bila elektron yang terikat radikal bebas berasal dari senyawa yang
berikatan kovalen, akan sangat berbahaya karena ikatan digunakan secara
bersama-sama pada orbital luarnya, umumnya senyawa yang memiliki ikatan
kovalen adalah molekul-molekul besar (biomakromolekul) seperti lipid, protein,
maupun DNA (Winarsih, 2007).
Semakin besar ukuran biomolekul yang mengalami kerusakan, semakin
parah akibatnya. Kerusakan sel akan berdampak negatif pada struktur dan
fungsinya. Secara biologis senyawa biomolekul memiliki fungsi yang sangat
penting. Oleh karena itu, adanya kerusakan struktur dan fungsi sel akan sangat
mengganggu kerja sistem organ secara umum (Winarsih, 2007).
Radikal bebas yang sangat berbahaya bagi makhluk hidup antara lain
adalah golongan hidroksil (OH
-
), superoksida (O
-
2
), nitrogen monooksida (NO),
dan peroksidal (RO
-
2
), peroksinitrit (ONOO
-
), asam hipoklorit (HOCL), hidrogen
peroksida (H
2
O
2
) (Silalahi, 2006).
Senyawa dan reaksi kimia yang dapat menghasilkan spesies oksigen
berpotensi toksik dapat disebut sebagai pro-oksidan. Dipihak lain, senyawa dan
reaksi yang menyingkirkan (membersihkan) spesies-spesies ini, menekan
pembentukannya, atau melawan efeknya disebut antioksidan yang mencakup
beberapa senyawa, seperti NADPH, GSH, asam askorbat dan vitamin E. Pada sel
normal terdapat keseimbangan antara pro-oksidan dan antioksidan. Namun,
keseimbangan ini dapat bergeser ke arah pro-oksidan jika pembentukan spesies
oksigen meningkat dengan pesat (misalnya setelah ingesti bahan kimia atau bahan
obat tersebut) atau jika kadar antioksidan berkurang (misalnya akibat inaktivasi
enzim yang berperan dalam pembersihan spesies oksigen serta akibat berbagai
keadaan yang menyebabkan turunnya berbagai kadar antioksidan yang disebutkan
sebelumnya). Keadaan ini disebut stres oksidatif dan dapat menyebabkan
kerusakan sel yang serius jika stres berlangsung secara masif atau berkepanjangan
(Murray et al, 2006).
II.3 Antioksidan
II.3.1 Pengertian Antioksidan
Antioksidan didefenisikan sebagai senyawa yang dapat bekerja
menghambat oksidasi dengan cara bereaksi dengan radikal bebas reaktif
membentuk radikal bebas yang tidak reaktif yang stabil. Jika dikaitkan dengan
penyakit, antioksidan dapat didefenisikan sebagai senyawa-senyawa yang
melindungi sel dari efek berbahaya radikal bebas oksigen reaktif. Antioksidan
juga merupakan senyawa yang dapat menghambat spesies oksigen reaktif atau
spesies nitrogen reaktif (ROS/RNS) dan juga radikal bebas sehingga antiksidan
dapat mencegah penyakit-penyakit yang dihubungkan dengan radikal bebas
seperti karsinogenesis, kardiovaskular dan penuaan (Tjay, 2002).
II.3.2 Klasifikasi Antioksidan
Secara umum antioksidan dikelompokkan menjadi 2 yaitu antioksidan
enzimatis dan non-enzimatis. Antioksidan enzimatis misalnya enzim superoksida
dismutase (SOD), katalase dan glutation peroksidase. Antioksidan non-enzimatis
masih dibagi dalam 2 kelompok lagi yaitu antioksidan larut lemak seperti
tokoferol, karotenoid, flavonoid, quinon dan bilirubin serta antioksidan larut air
seperti vitamin C, asam urat, protein pengikat logam dan protein pengikat heme.
Berdasarkan mekanisme kerjanya, antioksidan digolongkan menjadi 3
kelompok, yaitu :
1. Antioksidan primer
Antioksidan primer disebut juga antioksidan enzimatis. Suatu senyawa
dikatakan sebagai antioksidan primer, apabila dapat memberikan atom
hidrogen secara cepat kepada senyawa radikal, kemudian radikal antioksidan
yang terbentuk segera berubah menjadi senyawa yang lebih stabil. Antioksidan
primer bekerja dengan cara mencegah pembentukan senyawa radikal bebas
baru atau mengubah radikal bebas yang telah terbentuk menjadi molekul yang
kurang reaktif (Youngson, 2005).
2. Antioksidan sekunder
Antioksidan sekunder disebut juga antioksidan eksogenus atau
antioksidan non-enzimatis. Antioksidan dalam kelompok ini juga disebut
sistem pertahanan preventif. Dalam sistem pertahanan ini, terbentuknya
senyawa oksigen reaktif dihambat dengan cara pengkelatan metal atau dirusak
pembentukannya. Pengkelatan metal terjadi dalam cairan ekstraselular.
Antioksidan non-enzimatis dapat berupa komponen non-nutrisi dan komponen
nutrisi dari sayuran dan buah-buahan. Kerja sistem antioksidan non-enzimatik
yaitu dengan cara memotong reaksi oksidasi berantai dari radikal bebas atau
dengan cara menangkapnya. Akibatnya radikal bebas tidak akan bereaksi
dengan komponen selular.
Antioksidan sekunder meliputi vitamin C, vitamin E, karoten, flavonoid,
asam urat, bilirubin dan albumin. Senyawa antioksidan non-enzimatis bekerja
dengan cara menangkap radikal bebas (free radical scavenger), kemudian
mencegah reaktivitasnya. Ketika jumlah radikal bebas berlebihan, kadar
antioksidan non-enzimatik yang dapat diamati dalam cairan biologis menurun
(Youngson, 2005).
3. Antioksidan tersier
Kelompok antioksidan tersier meliputi enzim DNA-repair dan metionin
sulfoksida reduktase. Enzim-enzim ini berfungsi dalam perbaikan biomolekuler
yang rusak akibat reaktivitas radikal bebas (Youngson, 2005).
Berdasarkan sumbernya antioksidan dibagi atas:
1. Antioksidan sintetik
Antioksidan sintetik meliputi Butil Hidroksil Arisol (BHA), Butil
Hidroksil Toluen (BHT), propil galat, Tert-Butil Hidroksil Quinon (TBHQ),
vitamin C dan vitamin E. Antioksidan tersebut merupakan antioksidan alami yang
telah diproduksi secara sintetis untuk tujuan komersial.
2. Antioksidan alami
Antioksidan alami umumnya adalah senyawa fenolik atau polifenolik
yang dapat berupa golongan flavonoid, turunan asam sinamat, kumarin dan asam-
asam organik polifungsional. Golongan flavonoid memiliki aktivitas antioksidan
meliputi flavon, flavonol, isoflavon dan kalkon. Sementara turunan asam sinamat
meliputi asam kafeat, asam ferulat, asam klorogenat dan lain-lain. Senyawa
antioksidan polifenolik ini adalah multifungsional dan dapat bereaksi sebagai
pereduksi, penangkap radikal, pengkelat logam dan peredam terbentuknya singlet
oksigen (Trilaksani, 2003).
II.5. Uraian Spektrofotometri
II.5.1. Pengertian spektrofotometri
Spektrofotometri UV-Vis dapat digunakan untuk informasi kualitatif
sekaligus dapat digunakan untuk analisis kuantitatif bahan kimia. Dalam aspek
kuantitatif, suatu berkas radiasi dikenakan pada cuplikan (larutan sampel) dan
intensitas sinar radiasi yang diteruskan diukur besarnya. Radiasi yang diserap oleh
cuplikan ditentukan dengan membandingkan intensitas sinar yang diteruskan
dengan intensitas sinar yang diserap jika tidak ada spesies penyerap lainnya.
Intensitas atau kekuatan radiasi cahaya sebanding dengan jumlah foton yang
melalui satu satuan luas penampang perdetik (Gandjar, 2007).
Pengukuran pada spektrofotometri UV-Vis dapat dilakukan pada daerah
radiasi lembayung yaitu pada panjang gelombang 190-380 nm atau pada daerah
radiasi cahaya tampak pada panjang gelombang 380-780 nm (Anonim, 1979).
Spektrum UV-Vis disebut juga spektrum elektronik karena terjadi sebagai hasil
interaksi radiasi elektron. Interaksi itu terjadi karena adanya gugus berikatan
rangkap atau terkonjugasi yang mengabsorbsi radiasi elektromagnetik di daerah
UV-Vis.
Apabila suatu radiasi elektromagnetik dikenakan kepada suatu larutan
dengan intensitas radiasi semula (Io), maka sebagian radiasi tersebut akan
diteruskan (It), dipantulkan (Ir) dan diabsorbsi (Ia), sehingga :
Io =Ia + It + Ir (24)
Hukum Lambert-Beer menyatakan bahwa Intensitas yang diteruskan oleh
larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan.
Hukum ini dapat dituliskan sebagai berikut :
log
o
a aa a
Keterangan : A = Absorban
a = absorptivitas
b = tebal kuvet (cm)
c = konsentrasi (Gandjar, 2007).
II.5.2. Hal-hal yang harus diperhatikan dalam analisis menggunakan
spektrofotometri UV-Vis
Ada beberapa hal yang harus diperhatikan dalam analisa dengan
spektrofotometri UV-Vis terutama untuk senyawa yang semula tidak berwarna
yang akan dianalisis dengan spektrofotometri visibel karena senyawa tersebut
harus diubah terlebih dahulu menjadi senyawa yang berwarna. Berikut adalah
tahapan-tahapan yang harus diperhatikan :
1. Pembentukan molekul yang dapat menyerap sinar UV-Vis
Hal ini perlu dilakukan jika senyawa yang dianalisis tidak menyerap
pada daerah tersebut. Cara yang digunakan adalah dengan merubah menjadi
senyawa lain atau direaksikan dengan pereaksi tertentu. Pereaksi yang digunakan
harus memenuhi beberapa persyaratan yaitu :
a. Reaksinya selektif dan sensitive
b. Reaksinya cepat, kuantitatif dan reprodusibel (ajeg)
c. Hasil reaksi stabil dalam jangka waktu yang lama
Keselektifan dapat dinaikan dengan mengatur pH, pemakaian masking
agent atau penggunaan teknik ekstraksi (Gandjar, 2007).
2. Pemilihan panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah
panjang gelombang yang mempunyai absorbansi maksimal. Untuk memilih
panjang gelombang maksimal, dilakukan dengan membuat kurva hubungan antara
absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi
tertentu.
Ada beberapa alasan mengapa harus menggunakan panjang gelombang
maksimal, yaitu :
a. Pada panjang gelombang maksimal, kepekaannya juga maksimal karena pada
panjang gelombang maksimal tersebut, perubahan absorbansi untuk setiap
satuan konsentrasi adalah yang paling besar.
b. Disekitar panjang gelombang maksimal, bentuk kurva absorbansi datar dan
pada kondisi tersebut hukum Lambert-Beer akan terpenuhi.
c. Jika dilakukan pengukuran ulang maka kesalahan yang disebabkan oleh
pemasangan ulang panjang gelombang akan kecil sekali ketika digunakan
panjang gelombang maksimal (Gandjar, 2007).
3. Pembuatan kurva baku
Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai
konsentrasi. Masing-masing absorbansi larutan dengan berbagai konsentrasi
diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi (y)
dengan konsentrasi (x). Bila hukum Lamber-Beer terpenuhi, maka kurva baku
berupa garis lurus. Kemiringan atau slope adalah a (absorptivitas) atau
(absorptivitas molar). Penyimpangan dari garis lurus biasanya dapat disebabkan
oleh kekuatan ion yang tinggi, perubahan suhu dan reaksi ikutan yang terjadi
(Gandjar, 2007).
4. Pembacaan absorbansi atau cuplikan
Absorbansi yang terbaca pada spektrofotometri hendaknya antara 0,2
sampai 0,8 atau 15% sampai 70% jika dibaca sebagai transmitans. Anjuran ini
berdasarkan anggapan bahwa kesalahan dalam pembacaan T adalah 0,005 atau
0,5% (kesalahan fotometrik) (Gandjar, 2007).
II.5.3. Instrumen spektrofotometri UV-VIS
Spektrofotmetri pada dasarnya terdiri atas sumber sinar monokromator,
tempat untuk zat yang diperiksa, detektor, penguat arus dan alat ukur atau
pencatat. Berikut adalah instrumen kerja spektrofotmetri.
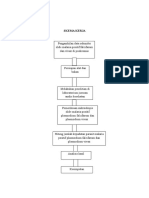
Gambar 2. Instrumen spektrofotometri UV-VIS
Sumber
Radiasi
Monokrom
ator
Sampel
Kompartemen
(Kuvet)
Penguat
Pembaca
Detektor
Setiap bagian peralatan optik dari spektrofotometri memegang fungsi
sendiri-sendiri:
1. Sumber radiasi
Sumber radiasi berfungsi untuk menghasilkan cahaya yang kontinyu dan
meliputi daerah spektrofotometri dimana alat bekerja.
2. Monokromator
Monokromator merupakan serangkaian alat optik yang menguraikan
radiasi polikromatik menjadi jalur-jalur yang efektif atau panjang gelombang
tunggal.
3. Detektor
Detektor merupakan suatu instrumen yang berfungsi mengubah energi
radiasi menjadi energi listrik.
4. Penguat
Berfungsi menguatkan sinyal elektrik yang diterima oleh detektor yang
kemudian diteruskan ke alat pengukur sehingga dapat dibaca.
5. Pembaca
Berfungsi untuk mencatat hasil dalam bentuk gambar atau angka-angka
(Underwood, 1999).
You might also like
- FaloakDocument12 pagesFaloakTheresia AvillaNo ratings yet
- Makalah Fitokimia Pembuatan Simplisia Daun Mahkota DewaDocument14 pagesMakalah Fitokimia Pembuatan Simplisia Daun Mahkota Dewauswatun khasanahNo ratings yet
- Laporan Lengkap Bab 1-5 PulaiDocument51 pagesLaporan Lengkap Bab 1-5 Pulaidevy100% (1)
- Senyawa Alkaloid, Sumber Dan Perannya Dalam TumbuhanDocument71 pagesSenyawa Alkaloid, Sumber Dan Perannya Dalam TumbuhanWieliyani AriNo ratings yet
- 1 3Document10 pages1 3Udha Sosial LampNo ratings yet
- Makalah Cengkeh 3Document13 pagesMakalah Cengkeh 3mugimardatillah100% (1)
- PulaiDocument2 pagesPulaiNovianty Uloli100% (1)
- Pembuatan Simplisia Dan Metode EkstraksiDocument15 pagesPembuatan Simplisia Dan Metode EkstraksiAmni HamidNo ratings yet
- Belimbing WuluhDocument4 pagesBelimbing WuluhSawer AhmedNo ratings yet
- Tanaman KirinyuDocument4 pagesTanaman Kirinyudonald kartikaNo ratings yet
- Makalah FitokimiaDocument15 pagesMakalah Fitokimianur annisaNo ratings yet
- Isolasi AlkaloidDocument12 pagesIsolasi AlkaloidPungkyUmiNo ratings yet
- Contoh Laporan NosiDocument13 pagesContoh Laporan NosiAnisa Ashfahany100% (1)
- Farmakognosi Tanaman BeracunDocument10 pagesFarmakognosi Tanaman Beracunrio kurnia wijayaNo ratings yet
- Formulasi Tablet Ekstrak Daun Kersen On GoingDocument41 pagesFormulasi Tablet Ekstrak Daun Kersen On Going003 SilviyaniNo ratings yet
- Bahan SingkongDocument5 pagesBahan SingkongBayu Gank100% (1)
- Perhitungan DosisDocument13 pagesPerhitungan DosisMUJRIAH TNo ratings yet
- Etnobiologi TANAMAN OBATDocument12 pagesEtnobiologi TANAMAN OBATSindy Ayu Kirana100% (1)
- Makalah (MATOA)Document11 pagesMakalah (MATOA)Anonymous M5aPOe7x100% (4)
- Simplisia BaruDocument26 pagesSimplisia Barurizky fatma sofyaniNo ratings yet
- DAUN KEMANGI (Autosaved) YyyyDocument3 pagesDAUN KEMANGI (Autosaved) YyyyDewi Anriani MunirNo ratings yet
- Anisar 3. EssayDocument6 pagesAnisar 3. EssayanisarNo ratings yet
- Temu LawakDocument5 pagesTemu LawakAinunNo ratings yet
- Pendahuluan MelatiDocument9 pagesPendahuluan MelatiWanti Putri LestariNo ratings yet
- Dagusibu MetforminDocument4 pagesDagusibu MetforminAnisa Eka Pancarani100% (2)
- SIMPLISIADocument20 pagesSIMPLISIAVina RamdianiNo ratings yet
- GAMBARDocument5 pagesGAMBARFidyah MuhdarNo ratings yet
- Orchidaceaea PDFDocument7 pagesOrchidaceaea PDFSarah SaviraNo ratings yet
- Reaksi Warna FlavonoidDocument29 pagesReaksi Warna Flavonoidcha_jaeheeNo ratings yet
- Tinjauan Pustaka Poin ADocument4 pagesTinjauan Pustaka Poin AifaNo ratings yet
- Makalah Kayu Manis - Kelompok 4Document23 pagesMakalah Kayu Manis - Kelompok 4al azhar fauzanNo ratings yet
- Taksonomi Dan TatanamaDocument12 pagesTaksonomi Dan TatanamaMiftah AnnurNo ratings yet
- Farmakognosi Simplisia Dari Sumber Tanaman & Struktur IntiDocument17 pagesFarmakognosi Simplisia Dari Sumber Tanaman & Struktur IntiIndah ApriliaNo ratings yet
- FarmakognosiDocument5 pagesFarmakognosisherina adellyaNo ratings yet
- Klasifikasi Dan Morfologi DurianDocument3 pagesKlasifikasi Dan Morfologi DurianMUHAMMAD DAFFANo ratings yet
- Kayu Secang (Caesalpina Sappan LDocument15 pagesKayu Secang (Caesalpina Sappan LBunga Debi LestariNo ratings yet
- Laporan Praktikum Farmakognosi Identifikasi AmilumDocument16 pagesLaporan Praktikum Farmakognosi Identifikasi Amilumwiwit apriliyaniNo ratings yet
- Klasifikasi Cinchonae Cortex Kel 2Document2 pagesKlasifikasi Cinchonae Cortex Kel 2Fitri Florida Wes'tNo ratings yet
- Keadaan Umum TalasDocument4 pagesKeadaan Umum TalasDeagisti Prima YoriskaNo ratings yet
- Lulur Kulit Jeruk Nipis 2Document24 pagesLulur Kulit Jeruk Nipis 2Nur Ulfahni100% (2)
- Damar Makalah NewDocument12 pagesDamar Makalah NewvaniaNo ratings yet
- Ot, Simplisia, Medicinal Herb, Nourishing Herb, EkstraksiDocument85 pagesOt, Simplisia, Medicinal Herb, Nourishing Herb, EkstraksiAmalia E100% (1)
- Makalah DelimaDocument15 pagesMakalah DelimaAyu Anggreini100% (1)
- Drymaria Cordata WildDocument9 pagesDrymaria Cordata WildAchmadHadiRatifuNo ratings yet
- Farmakognosi "Kulit Batang Kina "Document48 pagesFarmakognosi "Kulit Batang Kina "INDRI AULIANo ratings yet
- Soal Tugas Coaching 1Document28 pagesSoal Tugas Coaching 1Nabila BasalamahNo ratings yet
- Tanin Final.Document13 pagesTanin Final.Rhiny Mulyawati0% (1)
- Resume AromatikDocument14 pagesResume AromatikElla AprilyaNo ratings yet
- Jambu BijiDocument15 pagesJambu BijiOctavia WdNo ratings yet
- Uji Toksisitas Terhadap BiotaDocument20 pagesUji Toksisitas Terhadap BiotaKianNo ratings yet
- Makalah Mahkota DewaDocument22 pagesMakalah Mahkota DewaM Roni Putra Mulya100% (5)
- Tinjauan Botani FAloakDocument5 pagesTinjauan Botani FAloakHelen MinozNo ratings yet
- Laporan AmilumDocument15 pagesLaporan AmilumWanda Gita Van GobelNo ratings yet
- Makalah Ibuprofen AntiDocument23 pagesMakalah Ibuprofen AntiShaoran AuliaNo ratings yet
- Analisis AntioksidanDocument12 pagesAnalisis AntioksidanjungtantriNo ratings yet
- Aktivitas Antioksidan Daun SalamDocument18 pagesAktivitas Antioksidan Daun Salamadvent simangunsongNo ratings yet
- MAKALAHDocument32 pagesMAKALAHDry IkadheraNo ratings yet
- Makalah AntioksidanDocument12 pagesMakalah AntioksidanlusyNo ratings yet
- NO 2 Prof - RisyaDocument34 pagesNO 2 Prof - Risyaihdina ibrahimNo ratings yet
- Hariyatmi 7 NewDocument9 pagesHariyatmi 7 NewrianiNo ratings yet
- Laporan Pkpa Bab I-Ii (Fixxx)Document78 pagesLaporan Pkpa Bab I-Ii (Fixxx)Ivhen AninNo ratings yet
- Laporan Pkpa Bab III-lampiranDocument65 pagesLaporan Pkpa Bab III-lampiranIvhen AninNo ratings yet
- Bab IDocument8 pagesBab IIvhen AninNo ratings yet
- Nyeri Otot 1Document4 pagesNyeri Otot 1Ivhen AninNo ratings yet
- Tugas PengadaanDocument4 pagesTugas PengadaanIvhen AninNo ratings yet
- Tugas PengadaanDocument4 pagesTugas PengadaanIvhen AninNo ratings yet
- Pkpa Rsd. Dr. Soebandi Jember Feb-Mar 2017 PDFDocument154 pagesPkpa Rsd. Dr. Soebandi Jember Feb-Mar 2017 PDFernaNo ratings yet
- Drug Utilility Study: Cirroshis Hepatic + AscitesDocument16 pagesDrug Utilility Study: Cirroshis Hepatic + AscitesIvhen AninNo ratings yet
- Suplementasi Besi Merupakan Cara Efektif Karena Kandungan Besinya Yang Dilengkapi Asam Folat Yang Sekaligus Dapat Mencegah Anemia Karena Kekurangan Asam FolatDocument6 pagesSuplementasi Besi Merupakan Cara Efektif Karena Kandungan Besinya Yang Dilengkapi Asam Folat Yang Sekaligus Dapat Mencegah Anemia Karena Kekurangan Asam FolatIvhen AninNo ratings yet
- Tugas F.praktis Bu Utari AniDocument20 pagesTugas F.praktis Bu Utari AniIvhen AninNo ratings yet
- Drug Utilility Study: Cirroshis Hepatic + AscitesDocument16 pagesDrug Utilility Study: Cirroshis Hepatic + AscitesIvhen AninNo ratings yet
- Tugas F.praktis Bu Utari AniDocument20 pagesTugas F.praktis Bu Utari AniIvhen AninNo ratings yet
- NoDocument1 pageNoIvhen AninNo ratings yet
- RawDocument9 pagesRawIvhen AninNo ratings yet
- 1.MAKALAH OsteoporosisDocument19 pages1.MAKALAH OsteoporosisIvhen AninNo ratings yet
- Wa0000Document4 pagesWa0000Ivhen AninNo ratings yet
- WarfarinDocument1 pageWarfarinIvhen AninNo ratings yet
- Kanker Serviks NewDocument29 pagesKanker Serviks NewIvhen AninNo ratings yet
- Bab IDocument6 pagesBab IIvhen AninNo ratings yet
- WarfarinDocument1 pageWarfarinIvhen AninNo ratings yet
- Makalah Insulin SC Bu KisDocument13 pagesMakalah Insulin SC Bu KisIvhen AninNo ratings yet
- Alat Dan Perbekalan FarmasiDocument3 pagesAlat Dan Perbekalan FarmasiIvhen Anin0% (1)
- Makalah Insulin SC Bu KisDocument13 pagesMakalah Insulin SC Bu KisIvhen AninNo ratings yet
- Apakah Metadon ItuDocument1 pageApakah Metadon ItuIvhen AninNo ratings yet
- Daftar OT Yang DitarikDocument3 pagesDaftar OT Yang DitarikIvhen AninNo ratings yet
- Lamp IranDocument1 pageLamp IranIvhen AninNo ratings yet
- Apakah Metadon ItuDocument1 pageApakah Metadon ItuIvhen AninNo ratings yet
- Artikel SelesaiDocument7 pagesArtikel SelesaiIvhen AninNo ratings yet
- TUGAS Dr. RatihDocument10 pagesTUGAS Dr. RatihIvhen AninNo ratings yet
- Daftar OT Yang DitarikDocument3 pagesDaftar OT Yang DitarikIvhen AninNo ratings yet