Professional Documents
Culture Documents
Universidade Federal de Campina Grand1
Uploaded by
Sérgio CesárioCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Universidade Federal de Campina Grand1
Uploaded by
Sérgio CesárioCopyright:
Available Formats
1
UNIVERSIDADE FEDERAL DE CAMPINA GRANDE CURSO: LICENCIATURA EM QUMICA DISCIPLINA: QUMICA ORGNICA EXPERIMENTAL GRUPO 2
FRANCISCO SRGIO CESRIO DE ANDRADE
SNTESE DO CIDO ACETILSALICLICO (ASPIRINA)
CAJAZEIRAS PB JULHO DE 2013
UNIVERSIDADE FEDERAL DE CAMPINA GRANDE CURSO: LICENCIATURA EM QUMICA DISCIPLINA: QUMICA ORGNICA EXPERIMENTAL GRUPO 2
FRANCISCO SRGIO CESRIO DE ANDRADE
SNTESE DO CIDO ACETILSALICLICO (ASPIRINA)
O objetivo deste trabalho obter a Aspirina (cido Acetilsaliclico), que um cristal de cor branca, a partir do cido Saliclico e do Anidrido Actico. A reao acontecer na presena de cido sulfrico que atua como catalisador.
CAJAZEIRAS-PB JULHO DE 2013
SUMRIO
CAPA........................................................................................................................1 CONTRA CAPA......................................................................................................2 SUMRIO................................................................................................................3 INTRODUO........................................................................................................4 MATERIAIS UTILIZADOS....................................................................................5 REAGENTES UTILIZADOS...................................................................................6 PROCEDIMENTO EXPERIMENTAL....................................................................8 RESULTADO E DISCUSSO................................................................................9 CONCLUSO..........................................................................................................12 QUESTIONRIO.....................................................................................................13 BIBLIOGRAFIA......................................................................................................16 ANEXOS...................................................................................................................17
INTRODUO
O cido acetilsaliclico (em latim acidum acetylsalicylicum) um frmaco do grupo dos anti-inflamatrios no esteroides, utilizado como anti-inflamatrio, antipirtico, analgsico e tambm como antiplaquetar. , em estado puro, um p de cristalino branco ou cristais incolores, pouco solveis na gua, facilmente solvel no lcool e solvel no ter. Um dos medicamentos mais famosos base de cido acetilsaliclico a Aspirina. O seu nome foi obtido da seguinte maneira: A vem de acetil; Spir se refere Spiraea ulmaria (planta que fornece o cido saliclico); e o in era um sufixo utilizado na poca, formando o nome Aspirin, que depois foi aportuguesado para Aspirina. Em alguns pases, Aspirina ainda nome comercial registrado, propriedade dos laboratrios farmacuticos da Bayer para o composto cido acetilsaliclico. o medicamento mais conhecido e consumido em todo o mundo. Em 1999 a Aspirina completou 100 anos.
MATERIAIS UTILIZADOS
cido saliclico (C7H6O3) cido sulfrico (H2SO4) Anidrido actico Bquer de 250 e 100 mL Papel de filtro Basto de vidro Kitassato de 250 e 125 mL Esptula Proveta de 25 e 10 mL Erlenmeyer de 125 mL Funil de Bchner Pipeta de Pasteur (conta gotas) Pipeta de 10 mL Chapa eltrica Bomba de vcuo Tubos de ensaio Cavalete
REAGENTES UTILIZADOS
cido saliclico (C7H6O3) O cido saliclico um cido orgnico, de frmula qumica C7H6O3, pertencente ao grupo dos hidroxicidos (possui uma hidroxila e uma carboxila em sua estrutura), no seu estado puro slido, apresenta forma de cristais brancos ou de p cristalino, inodoro, pouco solvel em gua, mas solvel em solventes polares e ter. O nome saliclico vem do latim salix, que quer dizer rvore do salgueiro, de onde foi isolado pela primeira vez. Pode ser produzido a partir da biossntese da fenilalanina, um tipo de aminocido. Nos vegetais, o cido saliclico um hormnio, geralmente encontrado sob a forma de ter metlico e atua como retardador do envelhecimento natural das flores, processo conhecido como senescncia. Tambm estimula a resistncia individual de algumas espcies vegetais. (http://www.infoescola.com/quimica/acido-salicilico/)
cido sulfrico (H2SO4) O cido Sulfrico um composto qumico inorgnico, cuja frmula H2SO4. um lquido incolor, viscoso e oxidante, pouco voltil, seu Ponto de Ebulio 338C e densidade 1,84g/cm3. extremamente solvel em gua, porm, isto deve ser feito com muita cautela, sempre despejando o cido na gua e no o contrrio, pois se isto no for seguido, seus vapores so liberados agressivamente, podendo causar queimaduras graves no corpo do operador ou de algum prximo. um cido corrosivo e txico, pode causar bastante irritao e queimaduras, alm de ser nocivo caso haja inalao, contato com a pele ou ingesto. (http://www.brasilescola.com/quimica/uso-Acido-sulfurico-pela-industria.htm)
Anidrido actico (C4H6O3) Anidrido actico o composto qumico com frmula (CH3CO)2O. Comumente abreviado Ac2O, um dos mais simples anidridos de cidos e largamente usado como reagente em sntese orgnica. um composto incolor que cheira fortemente a cido actico, que formado pela sua reao com a umidade do ar. So utilizados largamente como agente de acetilao e desidratao na sntese de produtos orgnicos para a indstria qumica e farmacutica. Ac2O principalmente usado para a acetilao da celulose a acetato de
celulose para filmes fotogrficos e outras aplicaes, historicamente em substituio a outros filmes mais inflamveis e at explosivos (nitrocelulose). Na indstria txtil, utilizado para a obteno do acetato rayon. (http://pt.wikipedia.org/wiki/Anidrido_ac%C3%A9tico)
lcool etlico O lcool etlico uma substncia orgnica obtida da fermentao de acares, hidratao do etileno ou reduo a acetaldedo, encontrado em bebidas como cerveja, vinho e aguardente, bem como na indstria de perfumaria. No Brasil, tal substncia tambm muito utilizada como combustvel de motores de exploso, constituindo assim um mercado em ascenso para um combustvel obtido de maneira renovvel e o estabelecimento de uma indstria de qumica de base, sustentada na utilizao de biomassa de origem agrcola e renovvel. (http://pt.wikipedia.org/wiki/Etanol)
PROCEDIMENTO EXPERIMENTAL
Inicialmente pesou-se 3,008g de cido saliclico (C7H6O3) e 15 mL de anidrido actico logo em seguida houve o deposito da mistura em um balo de 100 mL. Utilizando-se uma pipeta de Pasteur (conta gotas), adicionou-se 10 gotas de cido sulfrico H2SO4. Sempre, agitando o recipiente para que houvesse uma melhor mistura dos reagentes. Depois de uma total mistura dos reagentes houve o aquecimento da reao em banho-maria (um mtodo cientfico utilizado tanto em laboratrios qumicos e na indstria culinria, farmacutica, cosmtica, conservas, etc., para aquecer lenta e uniformemente qualquer substncia lquida ou slida num recipiente, submergindo-o noutro, onde existe gua a ferver ou quase). Tudo isso em uma temperatura que estava em torno de 50 a 60C. Logo depois tirou a reao do aquecimento e deixou-a esfriar para um melhor desempenho, e em seguida foi adicionado 15 mL de gua gelada (A gua foi utilizada para acelerar o processo de cristalizao, pois o cido acetilsaliclico apresenta baixa solubilidade em gua) fazendo tudo isso para uma melhor formao dos cristais logo em seguida com o aparecimento dos cristais houve a filtrao da reao em um funil de Buchner utilizando papel de filtro redondo, lavou-se novamente com gua gelada. Logo em seguida para uma melhor purificao do produto, houve uma dissoluo do slido que foi formado em 15 mL de lcool etlico, logo depois houve um processo de aquecimento e depois q a reao j estava bem aquecida houve o processo inverso, ou seja, o processo de esfriamento da soluo, logo em seguida houve a filtrao dos cristais que foram formados. Logo depois para testar a pureza do produto foi utilizado uma pipeta de 10 mL para colocar 5 mL de gua destilada nos trs tubos de ensaio que j estavam marcados cada um com um numero que equivalia de 1 a 3, tudo feito para que no acontecesse nenhum problema com o experimento. Onde no 1 tubo houve o acrscimo de 1 mL de soluo de fenol, no 2 tubo foram colocados alguns cristais de cido saliclico e no 3 tubo foram colocados alguns dos cristais da soluo que foram formados durante o experimento. Depois houve o acrscimo de mais 10 gotas soluo de cloreto frrico em cada um dos tubos de ensaio, a fim de tentar mostrar se a reao teria ou no chegado ao resultado esperado. Logo depois, levou-se o produto final obtido a estufa para secar e logo aps a secagem e resfriamento ao ar livre, determinou-se a massa do composto obtido.
RESULTADO E DISCUSSO
A aspirina, ou cido acetilsaliclico, um slido branco. Sua sntese se d atravs da reao entre o anidrido actico e o cido saliclico, representada a seguir: Anidrido actico + cido saliclico + cido fosfrico produzindo cido acetilsaliclico + cido actico
Noes sobre mecanismo de reao:
A reao de acetilao do cido saliclico ocorre atravs do ataque nucleoflico do grupo OH fenlico sobre o carbono carbonlico do anidrido actico, seguido de eliminao de cido actico, formando um subproduto da reao, o cido acetilsaliclico. Aps o aquecimento da reao em banho-maria (50-60C) durante 15 minutos, observou-se a formao de duas fases na mistura. No teste de pureza, observou-se que os tubos de ensaio 1 e 2 apresentaram a colorao violeta aps ser adicionado o cloreto Frrico (FeCl3), o que comprovou-se a presena do acido saliclico no produto devido a irregularidades no processo de purificao. O terceiro tubo que deveria ter alguns cristais do produto de reao no se utilizou, pois a reao apresentou-se
10
em duas fazes, precisando-se usar outro tubo com o precipitado da reao. J o 4 tubo de ensaio que se adicionou apenas o precipitado da reao manteve a cor amarelada, o que comprova o sucesso da esterificao. Com a adio de gua gelada soluo, j iniciado o processo de resfriamento, observa-se a formao de precipitado no fundo do Erlenmeyer. Aps a filtrao, atravs do funil de Buchner, obtm-se o produto cido acetilsaliclico, restando como resduo lquido, o cido saliclico, anidrido actico e cido sulfrico. Aps o resfriamento (em gua gelada) da soluo aquecida de cido acetilsaliclico + lcool etlico acrescida de 40mL de gua tambm aquecida, observou-se formao de cristais. Pode-se descrever a massa e o volume dos matrias utilizados com a seguinte tabela:
PRODUTO cido saliclico Anidrido actico Papel filtro Vidro de relgio Produto formado Papel filtro + AAS AAS
MASSA (g) 3 16,2 0,8251 91,403 0,9269 1,752 0,9269
Volume (mL) 15
Para obteno do cido acetilsaliclico, foi necessrio reproduzir a reao do cido saliclico como anidrido actico utilizando cido sulfrico como catalisador da reao. O cido sulfrico no um reagente nessa reao, pois apenas serve para aumentar a velocidade da mesma. A aspirina bruta (antes da recristalizao) apresentou-se em cor branca e com granulaes. Aps a recristalizao a aspirina se apresentou transparente, em forma de cristais.
Calculando o rendimento:
A reao qumica a seguinte: cido saliclico + anidrido actico = cido acetilsaliclico + acido actico C7H6O3 + C4H6O3 C9H6O4 + H3CCOOH cido saliclico 1 mol C7H6O (138g) anidrido actico 1 mol C4H6O3 (102g)
11
3g
X= 306,27/138.1 X = 2,1 g de anidrido reagira com 3g de cido saliclico. Anidrido actico (densidade 1,082 g/cm3) D=m/v 1,08=m/15ml m= 1,08x15 m= 16,2 g de anidrido actico da 16,2 g 2,1 g = 14.1g de excesso
Logo em seguida houve o calculo do rendimento terico:
cido saliclico 138,1g 3g
cido acetilsaliclico 180,15g de X
X = 3,91 g de cido acetilsaliclico
E por ultimo calculou-se o rendimento obtido em toda a reao:
Massa do conjunto papel de filtro + acido acetilsaliclico = 1,752 g Papel de filtro = 0,8251g Acido acetilsaliclico formado= 1,752g - 0,8251g = 0,9269g 3,91g de cido acetilsaliclico 100% 0,9269g X X= 23,7% O rendimento obtido foi de apenas 23,7%, e no foi satisfatrio visto que ocorreram alguns problemas no ato da sntese.
12
CONCLUSO
No final do trabalho prtico pode-se concluir que possvel sintetizar cido acetilsaliclico em laboratrio fazendo reagir cido saliclico com anidrido actico e utilizando cido sulfrico para catalisar esta reao. possvel concluir que este processo de sntese permite obter cristas de cido acetilsaliclico com um rendimento baixo. No estamos na posse do rendimento para este processo, no entanto, aquele que obtivemos 23,7% parecenos bastante baixo.
13
QUESTIONRIO
1) Verifique qual o reagente limitante da reao.
cido saliclico 1 mol C7H6O (138g) 3g
anidrido actico 1 mol C4H6O3 (102g) X
X= 306,27/138.1 X = 2,1 g de anidrido reagira com 3g de cido saliclico. Anidrido actico (densidade 1,082 g/cm3) D=m/v 1,08=m/15ml m= 1,08x15 m= 16,2 g de anidrido actico Logo, o reagente limitante e o cido saliclico (3g) que apresenta uma menor quantidade e determina o rendimento mximo de produto, ou seja, limita a reao. da 16,2 g 2,1 g = 14.1g de excesso
2) Determine o percentual de excesso do reagente usado em maior quantidade. Massa de anidrido (densidade 1,082 g/cm3) D=m/v 1,08=m/15ml m= 1,08x15 m= 16,2 g de anidrido actico Percentagem em excesso 2,1g 100% 14,1g X X = 671,4 % em excesso. da 16,2 g 2,1 g = 14.1g de excesso
Logo, o percentual de excesso do reagente usado em maior quantidade de 671,4%.
14
3) Qual a funo do cido sulfrico adicionado ao meio reacional. Atua na reao de preparao do AAS, como um reagente ou como um catalisador? Justifique sua resposta:
O cido sulfrico atua como um catalisador da reao, ele no um reagente nesta rao, usa-se o cido sulfrico apenas para aumentar a velocidade da reao, caso no se utilize o cido sulfrico a reao iria ocorrer muito mais lentamente.
4) Sugira um mecanismo para a reao mostrando a ao do catalisador.
Mecanismo da reao do H2SO4
Esta reao envolve um mecanismo de catlise cida. O primeiro passo, representado na figura 3, consiste na protonao do anidrido actico pelo cido sulfrico. Forma-se ento um carboction com um grupo hidroxila. Este carboction atacado pelo par de eltrons do
15
oxignio do grupo hidroxila do cido saliclico, agora com carga formal positiva. No prximo passo o prton (tomo H+) transferido para o tomo de oxignio do ter. Por fim, ocorre uma reao de eliminao que origina o cido actico. O outro produto converte-se no cidoacetil saliclico apenas pela perda de um prton, o que permite, adicionalmente, a recuperao do catalisador.
5) Ao purificar um composto por recristalizao, aconselhvel esfriar a soluo lenta ou rapidamente? Explique. Cite outras tcnicas utilizadas para iniciar a formao de cristais.
O resfriamento deve ser um processo lento para que se permita a disposio das molculas em retculos cristalinos, ou seja, para que ocorra a formao de cristais com formaes de cristais grandes e puros. Alm do resfriamento podem ser empregadas outras tcnicas no processo de cristalizao, so eles: Concentrao, evaporao de solvente, saturao de solutos, liofilizao.
6) Por que recomendvel utilizar-se apenas uma quantidade mnima de solvente na etapa de recristalizao e quais critrios devero ser levados em considerao para que um solvente possa ser empregado neste processo?
Quanto menor for quantidade de solvente, menor vai ser a fixao da amostra, e consequentemente a obteno de cristais vai ser maior. Caso se descubra que a substncia muito solvel em um dado solvente para permitir uma recristalizao satisfatria, mas insolvel em outro. Os pares de solventes devem ser completamente miscveis. (exemplos: metanol e gua, etanol e clorofrmio, clorofrmio e hexano, etc.).
7) Na etapa de filtrao a vcuo, os cristais formados so lavados com gua gelada. Por qu?
A velocidade de resfriamento tem um papel determinante no tamanho dos cristais. Este procedimento importante para remover impurezas na superfcie dos cristais formados e a gua gelada para minimizar perdas durante a lavagem.
16
REFERNCIAS BIBLIOGRFICAS
SOLOMONS, T.W.G.; FRYHLE, C.B. Qumica Orgnica. 7. Ed. Rio de Janeiro: LTC, 2002.
http://www.infoescola.com/quimica/acido-salicilico/ http://www.brasilescola.com/quimica/uso-Acido-sulfurico-pela-industria.htm http://pt.wikipedia.org/wiki/Anidrido_ac%C3%A9tico http://pt.wikipedia.org/wiki/Etanol
http://pt.wikipedia.org/wiki/Wikip%C3%A9dia: P%C3%A1gina_principal
17
ANEXOS
ANEXO A: Aspirina (cido Acetilsaliclico), que um cristal de cor branca.
ANEXO B: sntese da aspirina
ANEXO C: formao de cristais durante a reao
18
You might also like
- Seminario Organica, Gorduras SaturadasDocument15 pagesSeminario Organica, Gorduras SaturadasSérgio CesárioNo ratings yet
- Análise sistemática dos cátions do subgrupo do cobreDocument10 pagesAnálise sistemática dos cátions do subgrupo do cobreSérgio CesárioNo ratings yet
- Universidade Federal de Campina Grand1Document18 pagesUniversidade Federal de Campina Grand1Sérgio CesárioNo ratings yet
- 2.prática de Cinética QuímicaDocument1 page2.prática de Cinética QuímicaSérgio CesárioNo ratings yet
- Universidade Federal de Campina Grand1Document18 pagesUniversidade Federal de Campina Grand1Sérgio CesárioNo ratings yet
- A Post I Lad Equi Mica GeralDocument56 pagesA Post I Lad Equi Mica GeralSérgio CesárioNo ratings yet
- RelatorioDocument11 pagesRelatorioSérgio CesárioNo ratings yet
- QUÍMICA ORGÂNICA EXPERIMENTALDocument44 pagesQUÍMICA ORGÂNICA EXPERIMENTALSérgio CesárioNo ratings yet
- Universidade Federal de Campina GrandeDocument10 pagesUniversidade Federal de Campina GrandeSérgio CesárioNo ratings yet
- Regras elaboração relatórioDocument5 pagesRegras elaboração relatórioSérgio CesárioNo ratings yet
- Direito a 1/3 hora-atividade para todos os profissionais da educaçãoDocument7 pagesDireito a 1/3 hora-atividade para todos os profissionais da educaçãoTiago TondinelliNo ratings yet
- Risoto de Frango - Cozinha TécnicaDocument3 pagesRisoto de Frango - Cozinha TécnicaCasa CasaNo ratings yet
- Seminovos em Belo Horizonte CarbigDocument1 pageSeminovos em Belo Horizonte CarbigVictor SantosNo ratings yet
- Relatório 2 - Movimento Sobre Um Trilho de Ar HorizontalDocument11 pagesRelatório 2 - Movimento Sobre Um Trilho de Ar HorizontalAna CostaNo ratings yet
- Karl Popper, o filósofo da ciênciaDocument5 pagesKarl Popper, o filósofo da ciêncialex-fsNo ratings yet
- Ldia12 Questao Aula Ed Lit Alberto CaeiroDocument2 pagesLdia12 Questao Aula Ed Lit Alberto CaeiroDiogo FrescoNo ratings yet
- Relatorio Eng Da Producao e A Profissao (Jonesigley Da Silva Duraes RU 4443925Document2 pagesRelatorio Eng Da Producao e A Profissao (Jonesigley Da Silva Duraes RU 4443925Jonesigley da Silva DurãesNo ratings yet
- Doenças Crônicas Que Determinam A Realização de Atividades Home OfficeDocument6 pagesDoenças Crônicas Que Determinam A Realização de Atividades Home OfficeAline Sousa JorgeNo ratings yet
- Ficha de atendimento previdenciárioDocument8 pagesFicha de atendimento previdenciárioEmanuely Lima100% (1)
- Partilha de Imovel em IRC e No Socio PT18751 1 de Março2017Document14 pagesPartilha de Imovel em IRC e No Socio PT18751 1 de Março2017Americo AraujoNo ratings yet
- Ajudante de Produção-ServenteDocument1 pageAjudante de Produção-ServenteElisaldo SilvaNo ratings yet
- Estaca hélice contínua monitoradaDocument35 pagesEstaca hélice contínua monitoradapressottiNo ratings yet
- Lista de Geometria Circunferencias e Quadrilc3a1teros1Document6 pagesLista de Geometria Circunferencias e Quadrilc3a1teros1zilmarsoares5618No ratings yet
- Geometria analítica: retas e ângulosDocument3 pagesGeometria analítica: retas e ângulosJulio CarraroNo ratings yet
- Fiscal de TributosDocument12 pagesFiscal de TributosFrancisco carpegeano Felix da silvaNo ratings yet
- Chave de Nivel Tipo Boia PeraDocument1 pageChave de Nivel Tipo Boia PeraAngelo MachadoNo ratings yet
- As quatro sugestões para mudançaDocument3 pagesAs quatro sugestões para mudançaRegina CoeliNo ratings yet
- 38fatorial, Permutações E Arranjos SimplesDocument40 pages38fatorial, Permutações E Arranjos SimplesZé OtávioNo ratings yet
- PLANIFICAÇÃODocument4 pagesPLANIFICAÇÃOAna NevesNo ratings yet
- Felicidade e Objeções Á Teoria de MillDocument2 pagesFelicidade e Objeções Á Teoria de MillTiago Afonso LopesNo ratings yet
- Manual UFCD 8598Document209 pagesManual UFCD 8598marianampmartinss_69No ratings yet
- Brown e Holmes. Capitulo 6 Exerccios e Respostas Do Livro.Document15 pagesBrown e Holmes. Capitulo 6 Exerccios e Respostas Do Livro.Rafael CarvalhoNo ratings yet
- As Grandes Profecias Relativas Aos Gentios - G. H. PemberDocument406 pagesAs Grandes Profecias Relativas Aos Gentios - G. H. PemberEDGAR DE PAULO SilvaNo ratings yet
- História Da Língua PortuguesaDocument3 pagesHistória Da Língua PortuguesaJOHnnY dAiNNo ratings yet
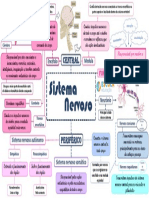
- Sistema nervoso: estrutura e funções principaisDocument1 pageSistema nervoso: estrutura e funções principaisGabriela PiresNo ratings yet
- Franquia Barbearia Seu Elias - Menos deDocument21 pagesFranquia Barbearia Seu Elias - Menos deDaniel RodriguesNo ratings yet
- Vim20 Ti P339 07 PortuguesDocument9 pagesVim20 Ti P339 07 PortuguesAndreNo ratings yet
- Cartilha Informativa - Síndrome de BurnoutDocument10 pagesCartilha Informativa - Síndrome de BurnoutIsabela SouzaNo ratings yet
- Porifera ResearchDocument694 pagesPorifera ResearchLuiz Mello LulaNo ratings yet
- Arte 7 AnoDocument2 pagesArte 7 AnoMárcia BarrosNo ratings yet