Professional Documents
Culture Documents
Pratica 03e04 - QIExpII
Uploaded by
Paulo Vitor SilvaOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Pratica 03e04 - QIExpII
Uploaded by
Paulo Vitor SilvaCopyright:
Available Formats
Curso: QUIMICA (5 TERMO) Disciplina: QUIMICA INORGNICA EXPERIMENTAL II Profa: Simone Fujii
AULA 3
PRTICA 3: SNTESE DO CLORETO DE HEXAMINONIQUEL(II) [Ni(NH3)6]Cl2 INTRODUO
O cloreto de hexaaminonquel(II), [Ni(NH3)6]Cl2, um slido (cristais de cor azulvioleta) com estrutura cristalina octadrica, solvel em gua e em soluo aquosa de amnia, mas insolvel em amnia concentrada, lcool etlico e ter. Este complexo decompe-se pelo aquecimento liberando NH3(g), transformando-se em um slido de cor verde. O mesmo acontece com sua soluo aquosa, que muda de azul-violeta para verde com o aquecimento. A obteno de [Ni(NH3)6]Cl2 pode ser feita pela reao entre a amnia concentrada e soluo de cloreto de nquel(II). A equao da reao de obteno pode ser escrita como: NiCl2.6H2O (s) + 6 NH3 (aq) [Ni(NH3)6]Cl2 (s) + 6 H2O (l) OBJETIVO Sintetizar o composto de coordenao cloreto de hexaaminonquel(II) [Ni(NH3)6]Cl2. Observar suas caractersticas e calcular o rendimento da reao. MATERIAIS E REAGENTES
Pipeta graduada 10 mL Bquer 50 e 100 mL Basto de vidro Funil de Buchner Kitasato Placa de Petri + papel de filtro Bomba de vcuo Hidrxido de amnio conc. Cloreto de niquel hexahidratado (NiCl2 . 6 H2O) Cloreto de amnio (NH4Cl) Etanol ter etlico Banho de gelo
PROCEDIMENTO PARTE 1: SINTESE DO COMPLEXO [Ni(NH3)6]Cl2 -Preparar a soluo amoniacal de NH4Cl: Adicionar 5 ml de NH4OH concentrado em um bquer 50mL e dissolver NH4Cl pouco a pouco at saturar a soluo. Transferir para uma proveta de 10mL e completar o volume para 10 ml com NH4OH. Deixar a soluo amoniacal em repouso at o momento do uso, fechada com filme plstico. -Pesar 5 g de NiCl2.6H2O em bquer de 100 mL e dissolver em quantidade suficiente (mnima) de gua destilada, adicionando pequenas quantidades com agitao. -Na capela, adicionar gradualmente 15 mL de soluo concentrada de NH4OH. Nesse ponto a soluo dever ficar com a cor violeta. Ocorre a a complexao. CUIDADO, reao EXOTRMICA. -Esfriar a soluo em gua corrente e adicionar 10 mL de soluo amoniacal de NH4Cl preparada no incio da aula.
-Deixe repousar a soluo em banho de gelo por 20 minutos. -Filtrar o precipitado por filtrao a vcuo, lavando-os com uma poro de NH4OH concentrado, lcool etlico e ter etlico (aprox. 10 ml em cada poro), nesta sequencia, e depois guardar o material na placa de petri; -Colocar a placa no dessecador a temperatura ambiente e deixe por dois ou trs dias para secar o material; -Depois de secos, pesar os cristais obtidos -Calcular o rendimento da reao de sntese e comparar com o rendimento terico. -Guardar os cristais obtidos para executar a parte 2 (Caracterizao do complexo produzido)
Curso: QUIMICA (5 TERMO) Disciplina: QUIMICA INORGNICA EXPERIMENTAL II Profa: Simone Fujii
AULA 4
PRTICA 4: SNTESE E CARACTERIZAO DO CLORETO DE HEXAMINONIQUEL(II) [Ni(NH3)6]Cl2
OBJETIVO Caracterizar o composto de coordenao cloreto de hexaaminonquel(II) [Ni(NH3)6]Cl2 e observar suas caractersticas. MATERIAIS E REAGENTES
Conta-gotas Tubos de ensaio Bquer 100mL Papel tornassol vermelho Hidrxido de amnio conc. Soluo alcolica de dimetilglioxima 1% Soluo de AgNO3 3 mol/L Soluo de HNO3 3 mol/L Banho-maria Bico de gs
PROCEDIMENTO PARTE 2: CARACTERIZAO E IDENTIFICAO DO COMPLEXO [Ni(NH3)6]Cl2 -Preparar em bquer de 100 mL uma soluo (ou suspenso) aquosa do complexo para caracterizar os componentes do produto obtido e fazer, em tubos de ensaio, as reaes indicadas a seguir. A) Caracterizao do Ni2+(aq) -Em um tubo de ensaio, colocar 10 gotas da soluo do complexo e aquecer cuidadosamente em banho-maria. -Esfriar e verificar se o meio est bsico usando papel tornassol vermelho. -Adicionar 3 gotas de soluo alcolica de dimetilglioxima. Observar e anotar o resultado -Adicionar gotas de soluo HNO3 3 mol/L soluo anterior at observar o desaparecimento do precipitado rosa. -Adicionar soluo de NH4OH conc. e observar o resultado. B) Caracterizao do Cl-(aq) - Em um tubo de ensaio, colocar 5 gotas da soluo do complexo e adicionar 3 gotas de soluo de AgNO3 3 mol/L. Observar e anotar o resultado. C) Caracterizao de NH3 Pode ser feita pelos seguintes processos: - Em um tubo de ensaio, colocar 5 gotas da soluo do composto e aquecer cuidadosamente em banho-maria. -Aproximar boca do tubo de ensaio uma tira de papel tornassol vermelho umedecida com gua destilada. Observar e anotar o resultado.
-Colocar um pouco do complexo slido em um tubo de ensaio e aquecer diretamente na chama do bico de gs. -Aproximar boca do tubo de ensaio uma tira de papel tornassol vermelho umedecida com gua destilada. Observar e anotar o resultado. QUESTIONRIO (O GRUPO DEVE RESPONDER E ANEXAR JUNTO AO RELATRIO) Obteno e Caracterizao do [Ni(NH3)6]Cl2 1) Escrever todas as equaes das reaes que se passam na prtica: obteno do [Ni(NH3)6]Cl2; decomposio do [Ni(NH3)6]Cl2 pelo aquecimento; caracterizao do Ni 2+; caracterizao do Cl - ; caracterizao de NH3 . 2) Considerando que o NiCl2.6H2O utilizado na reao de obteno continha 15 % de impurezas,qual a massa de [Ni(NH3)6]Cl2que poderia ser obtido ? 3) Qual o rendimento prtico do processo quando se obtm apenas 2,0 g do composto ? 4) Quais as quantidades mnimas de NiCl2.6H2O 100 % puro e de NH3 15 mol/L necessrias para se obter exatamente 20,0 g do composto? 5) A separao dos cristais de [Ni(NH3)6]Cl2 feita por meio de filtrao vcuo. Qual ou quais as vantagens desta filtrao sobre a filtrao comum ? 6) Aps a separao dos cristais do [Ni(NH3)6]Cl2 estes so lavados com lcool etlico e finalmente com ter. Pode-se substituir lcool etlico ou ter por gua destilada ? Explique. 7) Seria possvel determinar o ponto de fuso deste complexo ? Justificar sua resposta.
You might also like
- Curso Operacao de Filtro CopersucarDocument59 pagesCurso Operacao de Filtro CopersucarPaulo Vitor Silva100% (1)
- Curso 24 1 CentrifugaSecagemDocument40 pagesCurso 24 1 CentrifugaSecagemPaulo Vitor SilvaNo ratings yet
- Reações de OxidaçãoDocument13 pagesReações de OxidaçãoPaulo Vitor SilvaNo ratings yet
- Especificacoes Do-Alcool Focado para Mercado Mundial 000fxgfcrtu02wyiv80soht9hal6t8qxDocument9 pagesEspecificacoes Do-Alcool Focado para Mercado Mundial 000fxgfcrtu02wyiv80soht9hal6t8qxPaulo Vitor SilvaNo ratings yet
- Exercícios Óptica 03Document54 pagesExercícios Óptica 03Paulo Vitor SilvaNo ratings yet
- Sintese Do Cloreto de Pentaminclorocobalto III Welvis FurtadoDocument4 pagesSintese Do Cloreto de Pentaminclorocobalto III Welvis FurtadoPaulo Vitor SilvaNo ratings yet
- IFPADocument7 pagesIFPANelson CardosoNo ratings yet
- Art Reatores Duais RMBDocument13 pagesArt Reatores Duais RMBJosé Augusto Abreu de MouraNo ratings yet
- Gileuza - Estágio Supervisionado em Farmácia ComercialDocument15 pagesGileuza - Estágio Supervisionado em Farmácia ComercialAngelica MartinsNo ratings yet
- Modulo 06 - Tecnologias - BiorremediacaoDocument73 pagesModulo 06 - Tecnologias - BiorremediacaoLuisVieiraNo ratings yet
- Elementos de CoesãoDocument15 pagesElementos de CoesãoMarcelo LopesNo ratings yet
- Resultado - Mãe - João Paulo LemosDocument1 pageResultado - Mãe - João Paulo LemosDavidson GuimarãesNo ratings yet
- SlidesDocument52 pagesSlidesWillian Ricardo RitterNo ratings yet
- Proposta Comercial GtraceDocument10 pagesProposta Comercial GtraceFernando MachadoNo ratings yet
- CS - Direitos Difusos e Coletivos PDFDocument173 pagesCS - Direitos Difusos e Coletivos PDFDébora Gade100% (1)
- Algoritmos e Lógica de Programação: Contextualização ContextualizaçãoDocument10 pagesAlgoritmos e Lógica de Programação: Contextualização Contextualizaçãoeng.gustavobritesNo ratings yet
- Metodologia Científica (SLIDES DA AULA)Document67 pagesMetodologia Científica (SLIDES DA AULA)Arts Begbie100% (2)
- Folder TH Da CTBCDocument2 pagesFolder TH Da CTBCBruno da CostaNo ratings yet
- Periodo CompostoDocument34 pagesPeriodo CompostoRefúgio SeguroNo ratings yet
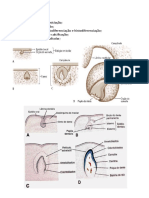
- RESUMO HISTOLOGIA - DentinogeneseDocument16 pagesRESUMO HISTOLOGIA - DentinogeneseSérgio Henrique Ferreira dos ReisNo ratings yet
- Lição Completa Tradição e SabedoriaDocument194 pagesLição Completa Tradição e SabedoriaDaniel GomesNo ratings yet
- Classes Invariáveis ExercíciosDocument6 pagesClasses Invariáveis Exercíciosandre luiz100% (1)
- Sistemas Políticos Comparados - ResumosDocument36 pagesSistemas Políticos Comparados - Resumosgabriela.resendeNo ratings yet
- Orações Subordinadas AdverbiaisDocument3 pagesOrações Subordinadas AdverbiaisJéssica Ulbricht100% (3)
- Pop Uenc 002Document12 pagesPop Uenc 002Juliana Coelho100% (1)
- Neomalignas II - 3Document72 pagesNeomalignas II - 3alessoncavalcanti2013No ratings yet
- Planificação 11 AnoDocument4 pagesPlanificação 11 AnoFrederico MarquesNo ratings yet
- Solomons ResolvidoDocument142 pagesSolomons ResolvidoAmanda Ramos87% (15)
- Alfred Hitchcock - Historias para Ler No CemiterioDocument164 pagesAlfred Hitchcock - Historias para Ler No CemiterioMagnoMendesNo ratings yet
- Guia de Fabricação Queijo MussarelaDocument7 pagesGuia de Fabricação Queijo MussarelaHeloísa Laticínios100% (1)
- BG 1944 v1 n11 FevDocument123 pagesBG 1944 v1 n11 FevCae MartinsNo ratings yet
- Inquerito TrabalhoDocument10 pagesInquerito TrabalhoVenancio Rabissone Missomali100% (3)
- Black Mirror e UberDocument17 pagesBlack Mirror e UberHandherson DamascenoNo ratings yet
- Manual Técnico Dos Extintores Portáteis ExtinpelDocument73 pagesManual Técnico Dos Extintores Portáteis ExtinpelNego1975No ratings yet
- Características Do Trabalho, Variáveis Sócio - Demográficas Como Determinantes Da Satisfação No Trabalho Na Marinha PortuguesaDocument11 pagesCaracterísticas Do Trabalho, Variáveis Sócio - Demográficas Como Determinantes Da Satisfação No Trabalho Na Marinha PortuguesaPROJETO DE PESQUISA FAINORNo ratings yet
- Divina de Jesus Scarpim - Deus Não Existe e Eu Posso Provar PDFDocument265 pagesDivina de Jesus Scarpim - Deus Não Existe e Eu Posso Provar PDFLuciano de Oliveira0% (1)