Professional Documents
Culture Documents
La Energía Nuclear 101
Uploaded by
Federico Marzullo0 ratings0% found this document useful (0 votes)
35 views14 pagesCopyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
35 views14 pagesLa Energía Nuclear 101
Uploaded by
Federico MarzulloCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
You are on page 1of 14
La Energa Nuclear 101
1. Principios bsicos para la comprensin de los fundamentos en
la energa nuclear
1.1 Modelo atmico de Niels Bohr
Su aporte fue fundamental para conocer cmo est compuesta fsicamente la materia,
en particular analizando la estructura del tomo. Explicando la presencia de rbitas
estables de electrones alrededor de un ncleo. Trabajos de Rutherford entre otros
pudieron dar un poco ms de luz en el tema.
Ahora bien, basndose en el tomo del Hidrgeno, ejemplo que vamos a describir a
continuacin:
Nota del grfico: Se aprecia la diferencia en el tamao de las partculas por algo muy sencillo; el protn tiene una
masa 1840 veces mayor que la del electrn, de alrededor de 1,6726x10
-27
kg. En este grfico no figuran neutrones,
pero su masa es muy similar a la del protn, alrededor de 1,6749x10
-27
kg.
Encontramos el Hidrgeno (identificado como Z = 1 por el nmero atmico del
elemento y la Z proviene del alemn Zahl, que significa nmero ya el propio
Mendeleiev haba organizado aos antes la tabla peridica de los elementos ubicando
cada uno con su nmero de electrones y protones en incremento hasta completar la
tabla, el Hidrgeno es Z = 1 por ser el ms simple de todos los elementos-), por su
configuracin electrnica: donde posee 1 protn en su ncleo (no contiene neutrones
en su ncleo ya veremos entonces ms adelante los casos especiales para sus
istopos-) y solo 1 electrn en rbita.
A priori y slo a modo de aclaracin, todo tomo est compuesto por 3 partculas:
Protones (carga positiva)
Neutrones (carga neutra)
Electrones (carga negativa)
Y a su vez, que existen dos zonas claramente identificables en los tomos:
Ncleo (compuesto por protones y neutrones luego veremos casos especiales
para algunos radionucledos e istopos-)
rbitas alrededor del ncleo, donde los electrones se ubican con cierta
organizacin (cosa que si quieren ver les recomiendo lean un poco de
modelos de Rutherford, teora cuntica de Heisenberg y ecuacin de Max
Planck)
Continuamos entonces
Sabemos que todo tomo entonces est no slo equilibrado (parte de los postulados
de Bohr), sino que tambin en ese estado de equilibrio natural, se encuentran
entonces tanto el ncleo como las rbitas en perfecta armona (en la jerga el tomo
est estable), con la misma cantidad de partculas positivas en el ncleo y con la
misma de negativas en las rbitas y a su vez con la misma cantidad de neutrones que
protones en su ncleo.
1.2 Istopos y Radionucledos
Los istopos son morfologas o configuraciones particulares de ciertos elementos,
donde tienen el mismo nmero atmico pero distinta masa, donde 2 tomos del
mismo elemento tienen la misma cantidad de protones pero no de neutrones. Lo
cierto es que las diferencias en la masa se deben a la presencia de distinto nmero de
neutrones en el ncleo del elemento en cuestin.
La pregunta ms comn en este momento es entonces: Y por qu no otra partcula
como un protn o un electrn en vez de variar los neutrones?
Precisamente porque dijimos que el elemento no cambia, debe seguir siendo el mismo
y adems mantenerse equilibrado, no es cierto?
Si incremento la cantidad de electrones debo incrementar en la misma cantidad la de
protones primero por una cuestin de equilibrio de cargas. Pero hacer esto implicara
que ya no estaramos hablando del mismo elemento sino de otro. Por ejemplo Z = 1 es
el Hidrgeno y Z = 2 es el Helio (un gas noble). Sumar un protn o electrn (o ms)
implicara hablar de otro elemento totalmente distinto al inicial. Es por eso entonces,
que los istopos slo varan la cantidad de neutrones (que no poseen carga elctrica),
precisamente porque debe mantenerse estable y conservar su equilibrio elctrico de
cargas positivas y negativas entre las partculas que lo componen.
Los radionucledos en cambio, adems de inestables y de tener una vida media de
duracin (que depender del istopo particular) experimentan un deterioro o
desintegracin radioactiva, es decir, manifiestan durante un determinado tiempo
radiacin en forma de partculas alfa o beta y rayos X o gamma.
Ya que estamos y para no estar saltando de un lugar a otro, vamos a definir entonces
un poco qu es eso de la radiacin alfa, beta y gamma; lo cual nos va a ayudar un poco
tambin a explicar ms en detalle esto de que los radionucledos son inestables
El que sean inestables se debe a que en ese instante de tiempo ese tomo no est
equilibrado en su cantidad de protones y electrones, en otras palabras: le sobre de
uno o le falta del otro. Y cmo es que esto se concibe si habamos hablado antes de un
equilibrio natural de los tomos? Precisamente como resultado de ese rechazo y
bsqueda del equilibrio es que ese tomo tiene que deshacerse de esas partculas
extra que est teniendo.
Este proceso lo realiza por irradiacin de dichas partculas al exterior de su estructura
atmica.
Los tipos entonces, con un poco ms de detalle son:
Radiacin Alfa: Recuerdan cuando hablamos antes del Z = 2? El Helio? Este tipo
de radiacin expulsa o mejor dicho ahora irradia ncleos de este elemento,
es decir, 2 neutrones y 2 protones. Son de las menos penetrantes entre las 3.
Radiacin Beta: Independientemente de si son positivas o negativas estas
irradiaciones, resultan de la desintegracin como habamos dicho
anteriormente de partculas (en este caso neutrones o protones del ncleo) en
un estado de excitacin. Son ms penetrantes que las Alfa. En este caso, luego
de la expulsin beta, como resultado ese tomo modifica su nmero atmico
por haber ganado o perdido un protn de su ncleo, con lo cual cambia el
elemento.
Radiacin Gamma: Este es el caso ms daino por ser el de mayor penetracin
irradiada. Son ondas electromagnticas de longitud de onda corta. Para aislar
este tipo de radiacin se requieren protecciones especiales biolgicas, en
general se utiliza el plomo en generosas cantidades entre otros.
Les pido disculpas por los tecnicismos, aqu fueron inevitables
1.3 El Hidrgeno y sus istopos
Muy bien, hasta aqu definimos la estructura normal, natural de un tomo de
Hidrgeno.
Lo que an no habamos hecho es analizar un poco los distintos tipos de estructuras
que puede adoptar el Hidrgeno
Como comnmente se lo encuentra en la naturaleza, es decir, con 1 protn en su
ncleo (obviamente, sino no sera Hidrgeno), sin neutrones y 1 electrn a su
alrededor bajo la rbita correspondiente (tambin ntese que conserva el equilibrio
con la cantidad de protones) se lo conoce como Protio.
Existe otro, que ya es un isotipo pero que de cuando en cuando alguno ingieren
accidentalmente porque se lo encuentra en la naturaleza aunque es poco comn; que
tiene 1 neutrn en su ncleo. A este se lo conoce como Deuterio. (el prefijo nos indica
2 partculas en el ncleo).
Finalmente, existe otro isotipo ms, que contiene en vez de 1 neutrn, 2. Fjense ahora
que es claro que estamos alterando el equilibrio interno del tomo, no es cierto?
Tendramos que tener 1 de cada uno a lo sumo (porque para el Hidrgeno en su forma
de Protio prescindimos del neutrn, verdad?). Entonces?
Bueno, a este isotipo se lo conoce como Tritio. (su nombre porque tiene 3 partculas
en su ncleo). Miren nuevamente en la pgina anterior la definicin de
radionucledos
Este isotipo es inestable y necesita sacarse de encima ese peso extra que trae en su
ncleo, ese neutrn extra. Precisamente por ese motivo es que el Tritio es radioactivo
y emite radiacin espontnea de tipo beta. Tiene entonces una vida promedio (en este
caso de unos 12,3 aos) y, como todos los radionucledos, por decaimiento tiende a
mutar a otro elemento y en este caso es a Helio 3 (He
3
), con lo cual vean nuevamente
en la definicin de la pgina anterior, gana un protn y un electrn por captura,
cambia su nmero atmico, cambia el elemento. A uno estable
Aprovechando, definimos entonces qu es decaimiento
En pocas palabras para nuevamente evitar caer en tecnicismos, se dice decaimiento de
un elemento a la transicin que lo lleva de un estado de excitacin A a otro B, donde
por ley de conservacin de la energa, A es ms alto que B. Podramos decir muy
vagamente y slo con fines ilustrativos que esa partcula en su decaimiento por
liberacin de radiacin (en forma de fotones) se va apagando, consumiendo, tal y
como vimos en la definicin de los radionucledos, recuerdan?
Bien, continuemos entonces
1.4 Molculas de agua y utilizacin de istopos de Hidrgeno
Sabemos que la molcula del agua que tomamos de cualquier canilla no es ni ms ni
menos que la unin qumica covalente de un tomo de Oxgeno (que naturalmente es
diatmico entre otros, ahora fuera de contexto- y por eso O
2
) con 2 tomos de
Hidrgeno: H
2
O. A esto se lo conoce como agua liviana.
De la utilizacin de los isotipos del Hidrgeno que vimos en el punto anterior, surgen:
El agua pesada (conocida tambin como D
2
O o Deuterio 2 Oxgeno
(recuerden que la valencia del Hidrgeno sigue siendo 1 entonces necesito 2
Deuterios para combinar con 1 Oxgeno).
El Tritio es un caso particular ya que se encuentra en estado natural en forma
de gas y no de agua, pero puede hallarse tambin en forma de agua tritiada.
Ya que estamos Cunto pesa un litro de cada agua liviana y de agua pesada en
comparacin?
A priori recordemos algo de estequiometria, as estamos seguros de que hablamos el
mismo idioma.
Todos los elementos tienen un peso atmico, cuya unidad es medida en UMA (Unidad
de Masa Atmica).
Detallemos entonces cul es la masa de cada partcula que compone al tomo de
forma tal de poder concentrarnos despus en las diferencias entre los istopos:
Masa del protn: 1,007276 UMA
Masa del neutrn: 1,008664 UMA
Masa del electrn: 0,000548 UMA
Ok, estamos listos para continuar entonces
Si el Hidrgeno tiene 1 protn en su ncleo y 1 electrn en rbita, podemos decir sin
miedo alguno que un tomo pesa: 1,007276 UMA + 0,000548 UMA = 1,007824 UMA
Partiendo de la base que un litro de agua liviana equivale a 1000 gramos (con una
densidad de 1gr/ml) y que un mol de molculas de agua (ac los agarr con algo de
estequiometria, les suena de la secundaria?) pesa (peso atmico) 18, donde: H=1 hay
2 tomos- y O=16, obteniendo por litro alrededor de 55,6 moles de molculas de agua.
Recuerdan el nmero de Avogadro? No era 6,02 x10
23
?
Decimos entonces:
1 mol de H
2
O pesa: H(1 * 2) + O(1 * 16) = 18
1000 ml de H
2
O = 1000/18 = 55,6 moles/litro de agua
Multiplicando, obtienen que 1 litro de agua liviana tiene alrededor de 334,712x10
23
molculas. Y pesa aproximadamente 1kg.
Qu pasa con el agua pesada??? Recuerden que ahora estoy teniendo 1 neutrn en
cada ncleo de Hidrgeno que antes no tena y que su masa era comparable a la del
protn, con lo cual estoy incrementando considerablemente la masa.
Hagamos entonces el mismo clculo de masa para el Deuterio, tal y como hicimos con
el Hidrgeno:
Cantidad de protones: 1
Cantidad de neutrones: 1
Cantidad de electrones: 1
Masa del Deuterio: 1,007276 UMA + 1,008664 UMA + 0,000548 UMA = 2,016488 UMA
Nota: Por problemas de defectos de masa del Deuterio, estamos perdiendo
alrededor de 0,002388 UMA, lo que resulta para el Deuterio una masa atmica total
de: 2,0141 UMA.
Continuamos, la densidad del agua pesada, que es superior a la del agua liviana y es de
1,1056 gr/ml. Por lo tanto, 1,1056 kg/l. El mol de agua pesada pesa 20,04 g/mol. Esto
son 55,169 moles de molculas de agua pesada. Utilizando entonces el nmero de
Avogadro nuevamente, obtenemos alrededor de 332,1173x10
23
molculas. Y como
dijimos anteriormente, pesa 1,1056 kg.
Ntese la diferencia en la cantidad de molculas para ambos casos, al tener ms masa
el agua pesada, es natural que entren menos molculas en el mismo volumen.
Finalmente:
1 mol de D
2
O pesa: H(1 * 2) + O(1 * 16) = 20,04 (estamos poniendo el incremental
del neutrn extra en el ncleo del Hidrgeno)
1105,6 ml (por la densidad) de D
2
O = 1105,6 / 20,04 = 55,169 moles/litro de agua
1.5 Qu son fusin nuclear y fisin nuclear?
Estos dos fenmenos tienen historia, vaya si la tienen
Desde el primer femptosegundo de existencia del Universo se han llevado a cabo
estos dos, los repasamos?
La fisin nuclear es la ruptura de un ncleo atmico en dos partes semejantes en
cantidad de protones, lo cual implica que ese tomo original fisionado termina
formando 2 tomos con similar (no siempre se da el caso en que sean exactos)
nmero Z, dependiendo cada caso por su lado. Cabe destacar que para aquellos
elementos que no son radionucledos se los debe inducir a que se fisionen,
mediante el uso de bombardeo neutrnico, el cual consiste en un can de
neutrones que dispara hacia un ncleo de un elemento y comienza as la fisin.
Para el caso de los radionucledos, dependiendo de las condiciones puede darse el
caso de no precisar un bombardeo neutrnico para comenzar la fisin sino que lo
realizan espontneamente.
A modo de ejemplo y ya que vamos a utilizarlo ms adelante, la energa producida
por una fisin de 1 gramo de Uranio es de alrededor de 85 Gigajoules o 85x10
9
Joules. La misma cantidad de energa obtenida al quemar 3 toneladas de carbn.
O en una ms conocida an, para una cantidad de 1 kg de Uranio
235
fisionado, la
cantidad de energa generada es de alrededor de 18,7 Gw/h (Giga watts/hora).
La fusin nuclear en cambio es la unin de dos ncleos ligeros para producir uno
ms pesado que los anteriores. Tal es el caso de dos istopos de Hidrgeno que se
unen formando un ncleo con dos protones y dos neutrones, lo cual forma un
tomo de Helio (Z=2).
El problema aqu es la cantidad de energa necesaria para forzar esa reaccin, y
digo forzar porque lo que se efecta en una fusin nuclear es precisamente empujar
tomos contra otros para que sus ncleos se fundan en uno. La energa liberada por
esta reaccin tambin es muy alta, de alrededor de 1700 Gigajoules (vean la
diferencia con la fisin del Uranio ms arriba).
Digamos que el clsico ejemplo de fusin nuclear es nuestro Sol, el cual es una
inmensa cantidad de explosiones constantes de fusiones nucleares, creando as una
increble cantidad de explosiones termonucleares como resultado.
Este es el principio de la conocida bomba de Hidrgeno o bomba H o bomba
Termonuclear, donde la energa necesaria es tan alta para generar la fusin que
para iniciarse la explosin termonuclear se necesita previamente una explosin
nuclear precursora.
1.6 Por qu utilizar Uranio?
Al momento de analizar cules elementos seran ms convenientes que otros en la
generacin de energa nuclear se analizaron varias cuestiones; entre ellas se
necesitaba un elemento que naturalmente tuviese una alta cantidad de neutrones
en su ncleo para poder ser utilizados al momento de fisionarlos. La primer fisin
nuclear da inicio a un efecto domin el cual permite obtener fisiones sostenidas y
mantener as un nivel estable de energa generada. En el caso del Uranio, el
elemento con mayor peso atmico en toda la naturaleza, tiene 92 protones y 92
electrones, pero en su ncleo alberga entre 141 y 146 neutrones.
El Uranio se encuentra en muy bajas concentraciones en la naturaleza,
principalmente en 3 istopos: U
234
, U
235
y U
238
.
Del Uranio en estado natural, alrededor del 99,2% es de tipo U
238
, istopo
considerado de poco enriquecimiento, este istopo tiene una vida promedio de
4.470 millones de aos, terminando su vida en forma de plomo; por su bajo y lento
decaimiento alfa se utiliza para estimaciones de edad de la tierra. Mediante
procesos industriales se extrae el U
235
y tiene la particularidad de ser el nico
istopo de la naturaleza que es fsil. Cabe destacar que estos 3 istopos son
emisores alfa y gamma.
Su utilizacin en distintas escalas de refinamiento determinar su uso. Si bien
depende inicialmente de la configuracin del reactor y de la potencia a extraer, para
uso en reactores nucleares de agua pesada va desde menos del 1%, reactores
nucleares de agua liviana utilizan valores ms elevados de concentracin de U
235
,
reactores nucleares para uso en submarinos requieren alrededor del 80% y por
ltimo el armamento nuclear, el cual precisa al menos de una pureza del 90% o
superior.
2. Cmo funciona un reactor nuclear?
El principio elemental de todo reactor nuclear es el de producir energa elctrica. De qu
manera?
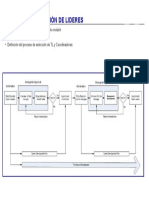
2.1 Principios de diseo y funcionamiento
Vamos a ver el diseo bsico de una central nuclear:
Sobre la izquierda se aprecia una gran botella de contencin, dentro de lo que
aparece como blindaje. Este blindaje es principalmente biolgico, una pared de
hormign macizo de alrededor de 1 metro y medio de espesor es capaz de contener
los altos niveles de radiacin dentro del ncleo. Dentro de ese tambin existe una
capa extra de acero de varios milmetros de espesor con el mismo fin. El reactor en
s mismo se compone bsicamente de un ncleo (con una geometra especfica no
entraremos en este tema por la complejidad que representa-, para la central nuclear
de Atucha I por ejemplo, la configuracin es hexagonal) compuesto por barras de
elementos combustible y barras de control. La cantidad de estas barras son
calculadas, aqu no existe el azar. Las barras de elementos combustibles estn
fabricadas de una aleacin llamada Zircaloy, en base a un metal llamado Circonio. La
particularidad de este material es que parece inerte frente al trfico de neutrones
a su alrededor, lo cual es bueno ya que como veremos luego, la clave es un alto flujo
(controlado) de neutrones. Las barras de elementos combustibles llegan a tener
hasta 6 metros de largo en el caso de Atucha, van insertadas en vainas especiales,
con una distancia suficiente como para poder mantener el flujo de neutrones entre
los elementos combustibles unos con otros. Dentro de estas barras hay pellets de U
natural y de U
235
, dependiendo la concentracin del segundo en cunto se precise
para el tipo de reactor en particular. Actualmente Atucha funciona con una cantidad
de U
235
del 0,85%.
Por otro lado, las barras de control son barras que adentro contienen un material
llamado Hafnio. La propiedad que tiene este metal es la de absorber neutrones, con
lo cual estas barras se utilizan dentro del reactor (bajndolas o subindolas de entre
los elementos combustibles) para controlar la cantidad de fisiones que los
neutrones que pululan dentro efectan. Al bajar las barras de control por completo
se efecta una actividad conocida como bajada de reactor. Esto implica la
detencin completa en la produccin de energa. Las barras son controladas por
bobinas y cada barra tiene 2 bobinas, una de empuje y otra de succin para retirar o
empujar las barras dentro del ncleo. En los casos de Atucha I y II, las barras de
control se introducen en forma oblicua a la disposicin de los elementos
combustibles, los cuales estn verticales al suelo. Existen otros tipos de reactores
donde los elementos combustibles se encuentran paralelos al suelo y las barras de
control perpendiculares a ellas, es decir, paralelas a la normal; lo cual es mucho ms
sencillo de controlar que en el otro caso donde estn dispuestas en forma oblicua.
Cada fisin nuclear desprende 2 cosas, primero energa en forma de potencial
elctrico, por un valor aproximado de 193 MeV, pero adems, una componente
calrica que es la que en realidad se aprovecha para generar energa.
Viendo esto, continuamos
Cabe destacar que el ncleo del reactor se encuentra sumergido en una sustancia
llamada moderador (en la imagen se ve en celeste). Por qu es necesario?
Pongamos un ejemplo simple Tenemos un vidrio al que queremos hacerle
impactos. Qu elemento propiciar mayor dao? Una bala o una piedra? An
suponiendo que ambos cuerpos tienen el mismo tamao es claro que la piedra har
ms dao dada la velocidad con la que atraviesa el vidrio. La misin del moderador
es la de moderar la velocidad con la cual los neutrones fisionan, absorbiendo
tambin la energa calrica desprendida en la fisin y convirtindose en lo que
despus transformar agua de otro circuito en vapor (ver turbina arriba al centro).
Como tipos de moderadores se conoce al agua pesada (compuesto que ya hemos
analizado), agua liviana y grafito (utilizado por ejemplo en la central nuclear de
Chernobyl). Las centrales nucleares de Atucha I y II utilizan agua pesada.
Debido a que la cantidad de agua pesada dentro del circuito primario no vara, es
decir el volumen es el mismo, al elevar su temperatura por la absorcin de la
energa calrica desprendida por las fisiones y por simple ley de los gases, la presin
debe aumentar. Entonces? Entonces se llega a presiones de hasta 115 kg/cm
2
de
presin dentro del reactor, algo as como 114 veces ms presin que la atmsfera
terrestre. El tener vapor dentro del reactor como en el grfico no es cierto (les pido
disculpas por no haber encontrado una imagen mejor), para esto existen circuitos
intercambiadores de calor (que se llaman circuitos secundarios) que transportan a
travs de tuberas el calor hacia un generador de vapor que contiene agua liviana y
genera a su vez el vapor que luego pasar por una turbina y generar la energa
elctrica. El agua liviana (desmineralizada al mximo) se condensa y se enfra
utilizando afluentes naturales como ros, lagos, mares y se vuelve a introducir al
circuito secundario para continuar con el proceso.
En resumen, la energa se produce como intercambio de calor entre el moderador y
la energa absorbida por las fisiones nucleares en el ncleo, que se transforma en
vapor y que luego mueve el rotor de una turbina, generando as, corriente elctrica.
Para esto, lo que se lleva a cabo es el constante control de la cantidad de fisiones
nucleares que se estn teniendo por unidad de tiempo, evitando una masa crtica, lo
cual culminara en un desastre, ya que implicara un desborde descontrolado de
fisiones nucleares y finalizara en un accidente nuclear con la explosin del ncleo
entre otras cosas.
2.2 Los elementos combustibles presentes en el reactor son eternos?
Cada una determinada cantidad de tiempo (en Atucha es alrededor de 6 meses por
cambio de elemento combustible) una gra especial dentro del reactor realiza
cambios en los mismos a medida que se van quemando. El quemado consiste en la
agotada emisin de neutrones y segn la posicin del elemento combustible el
quemado se realiza ms o menos parejo, con lo cual esta gra debe ir rotndolos
dentro del ncleo para maximizar el aprovechamiento de los mismos. Esto es,
algunas zonas de los elementos combustibles an tienen disponibles tomos de U
235
capaces de seguir fisionando otros tomos, la simple exposicin a otros que antes
no tena cerca produce que se contine generando energa hasta agotar por
completo el elemento.
Luego de consumidos, se transfieren a piletas especiales donde son contenidos
durante 5 a 7 aos hasta que pueden ser preparados para un depsito previo al
definitivo, el cual consta de un encamisado de hormign macizo que pueda evitar
escape de radioactividad.
En estas piletas se puede apreciar el verdadero color de la radiacin, que a
diferencia de la mayora de las pelculas y dibujos animados, presenta un color
azulado brillante, similar al Cobalto (uno de los istopos obtenidos por decaimiento
del U
235
es el Co60, que se utiliza en medicina para tratamientos oncolgicos en
quimioterapia). Este efecto luminoso se llama efecto Cherenkov, es una
irradiacin de tipo electromagntica y se debe a que los fotones desprendidos por
los elementos combustibles estn propagndose a velocidades superiores a la de la
luz en dicho medio.
Lo que se est viendo es el efecto de un choque de partculas, donde algo que va a
mayor velocidad que la velocidad de la luz en el medio se ve frenada por el propio
medio. Es la misma sensacin que experimenta un avin de combate al romper la
barrera del sonido o Match 1.
2.3 Un reactor nuclear se puede frenar y arrancar en cualquier momento?
Un reactor nuclear, como vimos anteriormente, puede frenar su operacin de varias
maneras (dependiendo de la situacin), entre ellas utilizando las barras de control o
por ejemplo inyectando cido deuterobrico en el ncleo del reactor. Lo que hace el
Boro es literalmente comerse los neutrones, dejando al ncleo sin neutrones
libres para efectuar fisiones y por ende cortando la generacin de energa.
Luego de apagado el reactor (decimos bien, detenida la reaccin en cadena),
comienza una generacin MUY acelerada de Xe
135
, un gas muy absorbente de
neutrones. Esto es conocido como envenenamiento por Xe (Xenn). Si luego de 40
minutos de parado el reactor no se inicia la actividad nuevamente por emisin
espontnea o disparando un haz de neutrones con un can hacia el ncleo para
inducir una fisin, el nivel de Xe
135
ser tan alto que no se podr bajo ningn punto
de vista volver a iniciar operacin. De esta forma, se debe quitar por filtrado el Xe
135
del agua del moderador, teniendo al reactor inactivo por 72 hs.
2.4 Cuando hablamos de una fisin nuclear de U
235
, de cunta energa
hablamos?
Veamos una tabla entonces con los valores de distribucin de energa de fisin
(valores expresados en MeVs):
Liberacin instantnea de energa: 180
Energa cintica de los fragmentos de fisin: 168
Energa de los rayos gamma instantneos: 7
Energa cintica de los neutrones instantneos: 5
Liberacin retardada de energa: 13
Desintegracin de partculas beta de los productos de fisin: 7
Desintegracin por rayos gamma de los productos de fisin: 6
Energa total liberada detectable debido a la fisin de un solo ncleo de U
235
: 193
MeV.
Dentro del reactor nuclear, cabe destacar que por cuestiones naturales, el agua
pesada (D
2
O del moderador) sometida a la radiacin gamma del ncleo suele
transformarse en Tritio, el cual es emisor beta, recuerdan que lo vimos?
La irradiacin de este radionucledo es de alrededor de 0,01859 MeV, lo cual
tambin hace, en una casi despreciable medida, su aporte energtico a la causa.
Existen filtros de Tritio en los reactores nucleares, con la finalidad de volver a
transformar ese Tritio en agua pesada y retornarlo al reactor nuclear.
Federico Marzullo
federico_marzu@hotmail.com
You might also like
- quimica basica1 capDocument2 pagesquimica basica1 capstephy3.spNo ratings yet
- UNIDAD 3 INTRODUCCION A LA ASTRONOMIA Estrellas - 1Document24 pagesUNIDAD 3 INTRODUCCION A LA ASTRONOMIA Estrellas - 1Demanledd OrtizNo ratings yet
- Composición AtómicaDocument5 pagesComposición Atómicasslaifstein100% (3)
- RADIOISOTOPOSDocument6 pagesRADIOISOTOPOSAngel ZamoraNo ratings yet
- Guia No.1 Conceptos BásicosDocument20 pagesGuia No.1 Conceptos BásicosCristian Javier Perez HernandezNo ratings yet
- Teoria AtomicaaDocument44 pagesTeoria AtomicaacarlosNo ratings yet
- La Teoria Atomica Covid-19Document9 pagesLa Teoria Atomica Covid-19LEWISNo ratings yet
- Química Nuclear Marco Teorico YbibliografiaDocument14 pagesQuímica Nuclear Marco Teorico YbibliografiaSadira MelaraNo ratings yet
- Material de Apoyo OsqDocument70 pagesMaterial de Apoyo OsqNoel PadillaNo ratings yet
- Guias de Quimica 2020 1Document37 pagesGuias de Quimica 2020 1ChrisLock E. RamirezNo ratings yet
- Conceptos Basicos Sobre RadiacDocument14 pagesConceptos Basicos Sobre RadiacSalvador Sanchez SantiagoNo ratings yet
- Clase 1 Estructura Atomica IP 2023Document41 pagesClase 1 Estructura Atomica IP 2023Sofía Alejandra Poblete FuentesNo ratings yet
- Química General - Capítulo 2Document22 pagesQuímica General - Capítulo 2karen elizabeth lopezNo ratings yet
- Qué Es Un ProtónDocument5 pagesQué Es Un ProtónSamanthaNo ratings yet
- Modelos atómicosDocument3 pagesModelos atómicosximena rodriguez cadena100% (2)
- Química ApuntesDocument14 pagesQuímica ApuntesFernando Jacuinde GuzmanNo ratings yet
- Apuntes Quim 3Document4 pagesApuntes Quim 3Wesley Mendoza OliverNo ratings yet
- Como Es Un AtomoDocument5 pagesComo Es Un AtomoAnita AceboNo ratings yet
- Estructura atómica y evolución de la teoría atómicaDocument7 pagesEstructura atómica y evolución de la teoría atómicaANGELICA TESONENo ratings yet
- Examen FinalDocument5 pagesExamen FinalManuel Jose Sandoval UrízarNo ratings yet
- Protón: descubrimiento, características y aplicacionesDocument16 pagesProtón: descubrimiento, características y aplicacionesHanny CastroNo ratings yet
- Bloque Fisica Moderna NuclearDocument11 pagesBloque Fisica Moderna NuclearCarlos AbrilNo ratings yet
- Estructura de La MateriaDocument24 pagesEstructura de La MateriaRoberto VillamarNo ratings yet
- Guía 3 Octavo Semanas Del 26 de Mayo Al 12 de JunioDocument7 pagesGuía 3 Octavo Semanas Del 26 de Mayo Al 12 de JunioAndrea OrtizNo ratings yet
- Que Es Un ProtonDocument4 pagesQue Es Un ProtonAlejandra VargasNo ratings yet
- FICHA SESION 02 de 3º - LECTIVA 11 - ESTRUCTURA ATÓMICADocument4 pagesFICHA SESION 02 de 3º - LECTIVA 11 - ESTRUCTURA ATÓMICALuis AstorgaNo ratings yet
- Tarea de CamposDocument4 pagesTarea de Camposcarlos huarcayaNo ratings yet
- Unidad Ii. Tarea 1Document4 pagesUnidad Ii. Tarea 1Lisandra MercedesNo ratings yet
- Estructura de La MateriaDocument24 pagesEstructura de La MateriaJOSE MANUEL ALVARADONo ratings yet
- BioelementosDocument5 pagesBioelementospmlalanguiNo ratings yet
- Guia 6 Estructura Atomica y ModelosDocument7 pagesGuia 6 Estructura Atomica y Modelosyanina CastroNo ratings yet
- MODELO ATOMICO - ESTRUCTURA DE ELECTRONES Y ENERGIA ATOMICA. Semana 3Document15 pagesMODELO ATOMICO - ESTRUCTURA DE ELECTRONES Y ENERGIA ATOMICA. Semana 3Juan Pablo BogadoNo ratings yet
- DaltonDocument11 pagesDaltonTony IngallsNo ratings yet
- ÍNDICE DEL ARTÍCULO AtomoDocument12 pagesÍNDICE DEL ARTÍCULO AtomoDennys LlontopNo ratings yet
- Desintegración Radioactiva Trabajo EscritoDocument7 pagesDesintegración Radioactiva Trabajo Escritodiego isaac burgos mirandaNo ratings yet
- Materia III BimestreDocument10 pagesMateria III Bimestreirvin macz reyNo ratings yet
- Documento Modelos ,Isótopos y EnlacesDocument6 pagesDocumento Modelos ,Isótopos y EnlacesLeandro R. Zárate RiveroNo ratings yet
- Guía 5Document5 pagesGuía 5Sofia DiazNo ratings yet
- Protones Con Carga PositivaDocument4 pagesProtones Con Carga PositivaRetro CartoonNo ratings yet
- Teoría atómica: partículas fundamentales y modelos históricosDocument137 pagesTeoría atómica: partículas fundamentales y modelos históricosPedro ArteroNo ratings yet
- Guà - A Teã Rica Clase 2Document16 pagesGuà - A Teã Rica Clase 2marce eugeNo ratings yet
- Introducción a la radiactividadDocument10 pagesIntroducción a la radiactividadMARCOS GONZALEZ CORTESNo ratings yet
- Secuencia 1 Partículas Subatómicas - Lectura Esas Maravillosas PartículasDocument40 pagesSecuencia 1 Partículas Subatómicas - Lectura Esas Maravillosas Partículasdiegochuyin00No ratings yet
- Tema 5 Modelos AtómicosDocument5 pagesTema 5 Modelos AtómicosIrene CastañonNo ratings yet
- Tema08 RadiactividadDocument12 pagesTema08 RadiactividadSaraNo ratings yet
- Relojes GeologicosDocument21 pagesRelojes GeologicosFabián Andrés JarabaNo ratings yet
- Quimica NuclearDocument24 pagesQuimica NuclearJeremy SstNo ratings yet
- Física Nuclear 4Document31 pagesFísica Nuclear 4Dick RodriguezNo ratings yet
- 1 Principios Fisicos de Medicina NuclearDocument28 pages1 Principios Fisicos de Medicina NuclearIngrid ReyesNo ratings yet
- Evolución Histórica Del ÁtomoDocument21 pagesEvolución Histórica Del ÁtomoVivian ÁlvarezNo ratings yet
- ISOTOPOS Tabla Calcio y WolframioDocument10 pagesISOTOPOS Tabla Calcio y WolframioMaria Vega04No ratings yet
- QUIMICADocument42 pagesQUIMICAconsueloNo ratings yet
- Radioactividad NaturalDocument19 pagesRadioactividad NaturalCarlos Sánchez BoneNo ratings yet
- Características de Las Partículas Del ÁtomoDocument10 pagesCaracterísticas de Las Partículas Del ÁtomoAbner TzejNo ratings yet
- UTP Atomos y MoléculasDocument14 pagesUTP Atomos y MoléculasFacu DxNo ratings yet
- SolDocument30 pagesSolaurens janmaNo ratings yet
- Apuntes Física y Química 3º Eso Tema 4 ArrregladoDocument11 pagesApuntes Física y Química 3º Eso Tema 4 ArrregladoMaría Jesús Payo BoullosaNo ratings yet
- Estructura AtomicaDocument11 pagesEstructura AtomicaACADEMIA DE MECANOGRAFIANo ratings yet
- Technical Writing Styles TrainingDocument4 pagesTechnical Writing Styles TrainingFederico MarzulloNo ratings yet
- CEMITEC-Memoria - EFQM - Caso de EstudioDocument111 pagesCEMITEC-Memoria - EFQM - Caso de EstudioFederico Marzullo0% (1)
- ProcesoDocument1 pageProcesoFederico MarzulloNo ratings yet
- Manchon TornoDocument1 pageManchon TornoFederico MarzulloNo ratings yet
- Articulo Cuidado Con DescarrilarDocument1 pageArticulo Cuidado Con DescarrilarFederico MarzulloNo ratings yet
- Rutina de GluteosDocument1 pageRutina de GluteosFederico MarzulloNo ratings yet
- Art Menazzi RSE ISO 9004 2008Document3 pagesArt Menazzi RSE ISO 9004 2008Federico MarzulloNo ratings yet
- Brasil (Ico-Icex) 2010Document258 pagesBrasil (Ico-Icex) 2010Federico MarzulloNo ratings yet
- Bonos Verdes CertificadosDocument20 pagesBonos Verdes CertificadosFederico MarzulloNo ratings yet
- 8SCM Distribucion 97-03Document45 pages8SCM Distribucion 97-03Federico MarzulloNo ratings yet
- Reglamento SantosDocument8 pagesReglamento SantosGuixo Dos SantosNo ratings yet
- La Incorporación de La Generación Y Al Mercado Laboral. El Caso de Una Entidad Financiera de La Ciudad de ResistenciaDocument27 pagesLa Incorporación de La Generación Y Al Mercado Laboral. El Caso de Una Entidad Financiera de La Ciudad de ResistenciaJordan Alexnnader GarzonNo ratings yet
- Rutina de Pecho Alta IntensidadDocument1 pageRutina de Pecho Alta IntensidadFederico MarzulloNo ratings yet
- Herramienta TDocument4 pagesHerramienta TJohan NuñezNo ratings yet
- Te - Lista de Precios Particular Julio 2016 - Arribeños 2173Document4 pagesTe - Lista de Precios Particular Julio 2016 - Arribeños 2173Federico MarzulloNo ratings yet
- Automatización y control, química - cursos técnicosDocument1 pageAutomatización y control, química - cursos técnicosFederico MarzulloNo ratings yet
- Rutina Pecho Biceps Piernas TrapecioDocument1 pageRutina Pecho Biceps Piernas TrapecioFederico MarzulloNo ratings yet
- UTN - Tenicatura Superior en Química y Química AplicadaDocument1 pageUTN - Tenicatura Superior en Química y Química AplicadaFederico MarzulloNo ratings yet
- Técnico Superior Física y Física AplicadaDocument1 pageTécnico Superior Física y Física AplicadamamagansoNo ratings yet
- Prof. FisicaDocument3 pagesProf. FisicajoseNo ratings yet
- UNGS Tecnicatura Superior en Automatización y ControlDocument2 pagesUNGS Tecnicatura Superior en Automatización y ControlFederico MarzulloNo ratings yet
- Informacion ImportanteDocument1 pageInformacion ImportanteFederico MarzulloNo ratings yet
- UNGS Tecnicatura en QuimicaDocument2 pagesUNGS Tecnicatura en QuimicaFederico MarzulloNo ratings yet
- UNGS Licenciatura en SistemasDocument3 pagesUNGS Licenciatura en SistemasFederico MarzulloNo ratings yet
- Acta de Asamblea PDFDocument4 pagesActa de Asamblea PDFFederico MarzulloNo ratings yet
- Prof. MatematicaDocument3 pagesProf. MatematicajosemarazNo ratings yet
- UNGS Tecnicatura en QuimicaDocument2 pagesUNGS Tecnicatura en QuimicaFederico MarzulloNo ratings yet
- BrochureDocument29 pagesBrochureFederico MarzulloNo ratings yet
- Semana 8 - RepasoDocument6 pagesSemana 8 - RepasoKendrik Jhon Sanchez PortillaNo ratings yet
- Actividad-Equipos y Utensilios en Un Taller de Alimentos.Document3 pagesActividad-Equipos y Utensilios en Un Taller de Alimentos.Angel MartinNo ratings yet
- Contrato Administrativo de Medidas de MitigaciónDocument16 pagesContrato Administrativo de Medidas de MitigaciónAbel Antonio Santos JacintoNo ratings yet
- Informe Quimica 4Document9 pagesInforme Quimica 4Felipe Ignacio �lvarezNo ratings yet
- Fisica II Examen Final Industrial 20 IIDocument2 pagesFisica II Examen Final Industrial 20 IIJAVIER MINCHOLA SANCHEZNo ratings yet
- Prevencion de IncendiosDocument36 pagesPrevencion de IncendiosLeonardo Omar Sanchez LinaresNo ratings yet
- Examen Principal - FisicoquímicaDocument2 pagesExamen Principal - FisicoquímicaMishell Heredia BenalcázarNo ratings yet
- Analogia Hombre MaquinaDocument12 pagesAnalogia Hombre MaquinaDaniel CervantesNo ratings yet
- 01-Joel A. Barker - Paradigmas - El Negocio de Descubrir El FuturoDocument25 pages01-Joel A. Barker - Paradigmas - El Negocio de Descubrir El FuturoMikel100% (4)
- Tema 1,2 y 3 ViedmaDocument8 pagesTema 1,2 y 3 ViedmaRocío Martinez TreintaNo ratings yet
- Expo Ciencia 5° CDocument10 pagesExpo Ciencia 5° CVictor MaytaNo ratings yet
- Talleres Investigación de OperacionesDocument1 pageTalleres Investigación de OperacionesMateo SotoNo ratings yet
- Procediimiento Poda de ArbolesDocument13 pagesProcediimiento Poda de ArbolesLibrito0983% (6)
- Recibo EnelDocument2 pagesRecibo EnelHernan AstoNo ratings yet
- Optimización de la producción en campos maduros de BoliviaDocument45 pagesOptimización de la producción en campos maduros de BoliviaMagaly Nicol Quispe MansillaNo ratings yet
- Factores RadiologicosDocument4 pagesFactores RadiologicosAnonymous ob44qN70ogNo ratings yet
- Electroválvula MFH-5-1/4 hoja datosDocument2 pagesElectroválvula MFH-5-1/4 hoja datosHugo GonzalezNo ratings yet
- Solucionario Configuracion de Instalaciones ElectricasDocument64 pagesSolucionario Configuracion de Instalaciones ElectricasPedro100% (2)
- Trabajo de MotoresDocument20 pagesTrabajo de MotoresReyder CiezaNo ratings yet
- Tabla de Carga Tablero Principal (TP)Document2 pagesTabla de Carga Tablero Principal (TP)Leonardo vivasNo ratings yet
- El Motor HdiDocument21 pagesEl Motor HdiRafael H Juliao BolañoNo ratings yet
- Peiper Rele 87Document4 pagesPeiper Rele 87Lennin Pascal Granda100% (1)
- Catálogo de Válvulas Tuberias-Bombas: ParkerDocument19 pagesCatálogo de Válvulas Tuberias-Bombas: ParkerRodri MVNo ratings yet
- Preguntas BrigidozzzDocument7 pagesPreguntas BrigidozzzJose Gilberto Apodaca100% (2)
- Ciclo Binario de Mercurio y VaporDocument2 pagesCiclo Binario de Mercurio y VaporArturo AmbrocioNo ratings yet
- Compresor tornillo mantenimientoDocument38 pagesCompresor tornillo mantenimientoEmy Marcillo100% (2)
- Pasteurizadores de PlacaDocument4 pagesPasteurizadores de PlacanoheliaNo ratings yet
- Liquidacion Financiera Arapa 2017 - FinalDocument68 pagesLiquidacion Financiera Arapa 2017 - FinalManuel QuispeNo ratings yet
- Construccion Sostenible Leed EspañaDocument4 pagesConstruccion Sostenible Leed EspañaNicolasArevaloGutierrezNo ratings yet
- Alarma en P.F. (B)Document2 pagesAlarma en P.F. (B)Leopoldo Jerez RochaNo ratings yet