Professional Documents
Culture Documents
Dipolo
Uploaded by
oseas_ls60520 ratings0% found this document useful (0 votes)
13 views5 pagesOriginal Title
dipolo
Copyright
© © All Rights Reserved
Available Formats
DOC, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOC, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
13 views5 pagesDipolo
Uploaded by
oseas_ls6052Copyright:
© All Rights Reserved
Available Formats
Download as DOC, PDF, TXT or read online from Scribd
You are on page 1of 5
Polaridade das Ligaes Covalentes
At o momento, a ligao covalente foi definida como sendo o compartilhamento de
eltrons entre dois ncleos, sem levar-se em conta a natureza deles. Existe, no entanto,
diferenas marcantes neste compartilhamento.
Se for considerada a molcula do hidrognio, onde dois !tomos de hidrognio
compartilham um par de eltrons, tem-se este par sendo atra"do com a mesma intensidade
pelos dois ncleos. # mesmo acontece no caso da molcula de cloro.
$or outro lado, %uando !tomos diferentes esto ligados, nem sempre este
compartilhamento ser! feito de forma simtrica. $or exemplo, considere-se a molcula do
!cido clor"drico. &esta molcula tem-se um !tomo de hidrognio ligado a um !tomo de cloro,
sendo o par de eltrons atra"do por am'os os ncleos. A grande diferena na
eletronegatividade destes !tomos resulta numa maior fora de atrao do par de eltrons pelo
ncleo de cloro. (esta maneira, a nuvem eletr)nica %ue forma a ligao estar! distorcida,
gerando uma falta de eltrons *ou carga parcial positiva+ em torno ao hidrognio e um excesso
deles *ou carga parcial negativa+ em torno ao cloro.
$ode-se ento classificar as liga,es covalentes em dois tipos- a%uelas onde a nuvem
eletr)nica no est! polarizada, formada com !tomos com eletronegatividades semelhantes, e
a%uelas onde ela encontra-se polarizada, no caso de ncleos com eletronegatividades
marcadamente diferentes. Estes dois tipos de ligao covalente so conhecidos como ligao
polar e apolar.
.omo resultado da polarizao de liga,es covalentes, tem-se a formao de dipolos
eltricos. &o caso do !cido clor"drico, pode-se representar a formao deste dipolo eltrico
conforme a figura a'aixo.
A formao de dipolos eltricos em molculas, como no caso do /.l, pode facilmente
ser verificado experimentalmente. Ao aplicar um campo eltrico, as molculas iro girar de
forma a alinhar-se com este campo, conforme mostrado no es%uema a'aixo.
/.l
.onsidere-se, por exemplo, a molcula do .#
0
. &este composto, o car'ono apresenta
duas liga,es com cada oxignio, uma atravs de um or'ital h"'rido do tipo sp e a outra com
um or'ital p puro. (esta maneira, a geometria da molcula linear, com 1ngulo de 234
o
entre
as duplas liga,es. (ada a maior eletronegatividade do oxignio em relao ao car'ono, sero
formados nesta estrutura dois dipolos eltricos, conforme o es%uema a'aixo. Se os vetores
%ue representam estes dipolos forem somados, ver-se-! %ue a resultante nula. Em outras
palavras, a molcula do .#
0
, mesmo sendo formada por liga,es polares, ser! apolar.
&a molcula da !gua, /
0
#, o !tomo de oxignio possui uma hi'ridizao do tipo sp
5
,
onde dois or'itais h"'ridos esto com um par de eltrons e os outros dois formam liga,es
com !tomos de hidrognio. A geometria da molcula ento triangular planar, com um 1ngulo
de 246,7
o
. (ois dipolos so ento formados devido a grande diferena de eletronegatividade
entre estes dois !tomos. # somat8rio destes dipolos no nulo, o %ue significa %ue a molcula
da !gua apresenta uma polaridade resultante, conforme pode ser visualizado no es%uema
a'aixo.
# somat8rio dos momentos de dipolo so realizados utilizando vetores. $ara tal, deve-
se transpor todos os vetores %ue representam os dipolos eltricos existentes na molcula,
mantendo-se a inclinao original, de tal forma %ue o in"cio de um coincida com o final do
outro. # vetor somat8rio, %ue representa a polarizao resultante na molcula, ento o'tido
unindo-se o in"cio do primeiro vetor da soma com o final do ltimo. &a figura a'aixo, esta
operao exemplificada para a molcula da !gua.
Foras de Interao Intermoleculares
A formao de dipolos eltricos em molculas covalentes tem como conse%9ncia o
surgimento de foras eletrost!ticas entre elas. #u se:a, os dipolos eltricos iro atrair-se
mutuamente, mantendo as molculas unidas. Alm deste tipo de interao, considerada fraca
%uando comparada com a ligao covalente, existem muitas outras foras entre compostos
%u"micos, as %uais so respons!veis pela existncia dos estados condensados da matria
*s8lido e l"%uido+. Entre as foras de interao intermolecular pode-se identificar dois tipos
'!sicos- as de Van der Walls e a ligao de hidrognio.
Foras de Van der Walls
As foras de van der ;alls atuam entre "ons, molculas e !tomos, sendo os principais
tipos conhecidos como foras "on-dipolo, dipolo-dipolo, dipolo induzido e de <ondon. =
extremamente complicado explicar matematicamente, via mec1nica %u1ntica, estas intera,es.
$orm, pode-se descrev-las de forma %ualitativa, considerando-as como foras de atrao
eletrost!ticas, como ser! feito a seguir.
a) Foras on-dipolo: %uando um dipolo eltrico, por exemplo a molcula da !gua, sofre
influncia do campo eltrico gerado por um "on, por exemplo o c!tion de s8dio, ele ir!
alinhar-se ao campo e manter-se unido a fonte geradora. #u se:a, neste caso, o
oxignio da !gua, onde est! localizada a carga parcial negativa, une-se ao c!tion de
s8dio e os hidrognios afastam-se o m!ximo poss"vel, conforme mostrado a'aixo.
b) Foras dipolo-dipolo: %uando duas molculas polares, como o metanol e .lorof8rmio,
se aproximam, surgem foras de atrao eletrost!tica entre elas. = importante notar
%ue estas foras so direcionais, orientando os dipolos espacialmente, como mostrado
na figura a'aixo.
c) Foras dipolares induzidas: %uando uma molcula apolar se aproxima a outra polar,
ocorre uma distoro da sua nuvem eletr)nica gerando um dipolo eltrido. Entre este
dipolo formado, conhecido como dipolo induzido, e o indutor, ocorre ento o
surgimento de foras de atrao semelhantes >s verificadas entre molculas polares.
&a figura a'aixo, este processo de induo aparece es%uematizado.
d) Foras de London: este tipo de interao surge entre molculas apolares. Admite-se
%ue a interao originada pela aproximao destas espcies leva a formao de dipolos
induzidos, os %uais iro se atrair mutuamente. Este tipo de fora tam'm conhecida
como disperso.
Ligao de Hidrognio
As liga,es de hidrognio *ou $onte de /idrognio+ so dif"ceis de serem definidas, uma
vez %ue so 'em mais fortes %ue as foras de van der ;alls, porm mais fracas %ue uma
ligao de valncia. $ode-se dizer %ue, %uando ligado a um grupo fortemente eletronegativo
*A+, como os !tomos de flor, oxignio e nitrognio, o hidrognio pode apresentar uma
segunda ligao, mais fraca %ue a anterior, com um segundo !tomo *?+. Esta segunda ligao
dita ento ligao de hidrognio, e representada com um trao descont"nuo, como
mostrado na figura a'aixo.
A-/ .......?
So conhecidas liga,es de hidrognio formadas com !tomos pertencentes a outra
molcula, como as verificadas na !gua pura ou na soluo de metanol em !gua, como
ilustrado a'aixo.
$ontes de /idrognio entre as molculas de !gua
$ontes de /idrognio entre molculas de metanol e !gua
Bibliografia
2. S#<#@#&S, A.;.B. Cu"mica #rg1nica. <ivros Acnicos e .ient"ficos. Dol. E
0. @c@FGGH, I. Qumica Orgnica. <A., Gio de Ianeiro, GI, 2JJK. vol.E
5. http-LLMMM.%mcMe'.orgL
6. NE<AGE, Gicardo. Cu"mica Beral. Dol. 0
You might also like
- Gerador Síncrono: Princípio de Operação e ComponentesDocument13 pagesGerador Síncrono: Princípio de Operação e Componentesoseas_ls6052100% (1)
- TrabalhoDocument8 pagesTrabalhooseas_ls6052No ratings yet
- NBR 6022 ArtigoDocument5 pagesNBR 6022 ArtigoAndréNo ratings yet
- 6+cronograma TcciDocument2 pages6+cronograma Tccioseas_ls6052No ratings yet
- Gerador Síncrono: Princípio de Operação e ComponentesDocument13 pagesGerador Síncrono: Princípio de Operação e Componentesoseas_ls6052100% (1)
- Prova 22 - Técnico (A) de Manutenção Júnior - Área Elétrica PDFDocument19 pagesProva 22 - Técnico (A) de Manutenção Júnior - Área Elétrica PDFoseas_ls6052No ratings yet
- Documents - Tips 805155cf986a550346d0339784ccDocument7 pagesDocuments - Tips 805155cf986a550346d0339784ccoseas_ls6052No ratings yet
- Resenha CriticaDocument1 pageResenha Criticaoseas_ls6052No ratings yet
- TDE15 Exercícios+Tipos+de+GeraçãoDocument3 pagesTDE15 Exercícios+Tipos+de+Geraçãooseas_ls6052No ratings yet
- Prova 26 - Técnico (A) de Manutenção Júnior - Área ElétricaDocument15 pagesProva 26 - Técnico (A) de Manutenção Júnior - Área ElétricaNathalia CarballoNo ratings yet
- Redes Tele II - 20-09Document1 pageRedes Tele II - 20-09oseas_ls6052No ratings yet
- Prova 2 - Redes de ComputadoresDocument4 pagesProva 2 - Redes de Computadoresoseas_ls6052No ratings yet
- Exercicios Com Respostas PDFDocument8 pagesExercicios Com Respostas PDFoseas_ls6052100% (1)
- 201-207-Agente Unidades Consumidoras-ServiçosDocument26 pages201-207-Agente Unidades Consumidoras-ServiçosLuciana Alessandra de SouzaNo ratings yet
- Tecnico EletricaDocument13 pagesTecnico EletricatodocorpNo ratings yet
- Relatorio Praticas Arquitetura de ComputadoresDocument21 pagesRelatorio Praticas Arquitetura de Computadoresoseas_ls6052No ratings yet
- Computação EvolucionariaDocument14 pagesComputação Evolucionariaoseas_ls6052No ratings yet
- Aula Pratica4Document2 pagesAula Pratica4oseas_ls6052No ratings yet
- Questões RedesDocument5 pagesQuestões Redesoseas_ls6052No ratings yet
- Exercícios 01Document3 pagesExercícios 01oseas_ls6052No ratings yet
- Prova 1 - Inteligência ComputacionalDocument6 pagesProva 1 - Inteligência Computacionaloseas_ls6052No ratings yet
- Prova 1 - Redes de ComputadoresDocument4 pagesProva 1 - Redes de Computadoresoseas_ls6052No ratings yet
- Prova 2 - Inteligência ComputacionalDocument5 pagesProva 2 - Inteligência Computacionaloseas_ls6052No ratings yet
- Tel FixaDocument74 pagesTel FixaandreCOST100% (2)
- Abracopel - EstatísticasDocument8 pagesAbracopel - Estatísticasoseas_ls6052No ratings yet
- Carl Nagel - Os Selos Negros de Salomão O ReiDocument27 pagesCarl Nagel - Os Selos Negros de Salomão O Reioseas_ls605289% (19)
- Oração para Trazer A Pessoa Amada em 24hDocument1 pageOração para Trazer A Pessoa Amada em 24hoseas_ls6052No ratings yet
- As Vias AlquimicasDocument3 pagesAs Vias AlquimicasHeimdall_sentinelaNo ratings yet
- Iniciação aos Arcanos Maiores do TarotDocument28 pagesIniciação aos Arcanos Maiores do TarotGabrielVasconcelosNo ratings yet
- Feng Shui NumerologiaDocument62 pagesFeng Shui NumerologiaAndré Tredicci Tredicci100% (1)
- Teste3 - 2P - 9ºano (Fev21)Document3 pagesTeste3 - 2P - 9ºano (Fev21)Sónia PereiraNo ratings yet
- RELATORIO - Magnetostrição de Chapa Metálica de FeSiDocument31 pagesRELATORIO - Magnetostrição de Chapa Metálica de FeSiPatrick Lobo PadulaNo ratings yet
- MRUV: Relatório de prática experimentalDocument8 pagesMRUV: Relatório de prática experimentaldiego garciaNo ratings yet
- Catalogo de Peças MWM NGD 3.0eDocument126 pagesCatalogo de Peças MWM NGD 3.0eRick AlvesNo ratings yet
- Manualir 6000Document1 pageManualir 6000Alexandre Da Silva PintoNo ratings yet
- Apostila de OplatDocument59 pagesApostila de OplatTania Barbosa50% (2)
- Rochas, Solos e IntemperismoDocument17 pagesRochas, Solos e IntemperismoBerdasfreitada25% (4)
- Ficha V - Cinetica Quimica - Parte II - Equacao de ArrheniusDocument2 pagesFicha V - Cinetica Quimica - Parte II - Equacao de ArrheniusAngelique ViannyNo ratings yet
- Scratch e o Pensamento SistêmicoDocument5 pagesScratch e o Pensamento SistêmicoOmero AlvesNo ratings yet
- Relatório Buck e Boost MCCDocument32 pagesRelatório Buck e Boost MCCKaio FreitasNo ratings yet
- Exercício Sobre A Linguagem Dos Mapas e Os Erros Da Cartografia TemáticaDocument1 pageExercício Sobre A Linguagem Dos Mapas e Os Erros Da Cartografia TemáticaMarcus Vinicius Figueiredo GomesNo ratings yet
- Abnt NBR 13523 2005Document26 pagesAbnt NBR 13523 2005falmeida_62967100% (1)
- Análise de Sistemas LinearesDocument38 pagesAnálise de Sistemas LinearesVictorNo ratings yet
- Análise de Esperando GodotDocument8 pagesAnálise de Esperando GodotPepaSilvaNo ratings yet
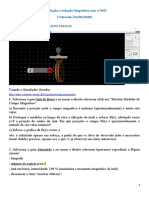
- Lei de Lenz Transformador Gerador ExpFaraday PhET Tomaz 17 06 20Document4 pagesLei de Lenz Transformador Gerador ExpFaraday PhET Tomaz 17 06 20Kelly CrysNo ratings yet
- Apostila AV - Basica - Hottec PDFDocument42 pagesApostila AV - Basica - Hottec PDFAmanda GamaNo ratings yet
- Programas de Curso - Villa-Lobos 2021Document11 pagesProgramas de Curso - Villa-Lobos 2021Vanessa Antunes Terra PassosNo ratings yet
- Atuacao Fisico MedicoDocument42 pagesAtuacao Fisico MedicoSamuel MartiniNo ratings yet
- Estudo de Confiabilidade - Preditiva VALE X Engenharia SKFDocument30 pagesEstudo de Confiabilidade - Preditiva VALE X Engenharia SKFdaniel atachaguaNo ratings yet
- Funções de mais de duas variáveisDocument11 pagesFunções de mais de duas variáveisPaulo SampaioNo ratings yet
- Relatorio Emulsão EscabicidaDocument6 pagesRelatorio Emulsão EscabicidaSegundo ChavesNo ratings yet
- Eletrólise e estequiometria em exercíciosDocument24 pagesEletrólise e estequiometria em exercíciosPaulo VictorNo ratings yet
- Conjuntos numéricos e intervalosDocument4 pagesConjuntos numéricos e intervalosJean Zanchettin Dutra0% (1)
- 3 Estabilidade Estatica Latero DirecionalDocument46 pages3 Estabilidade Estatica Latero DirecionalLeandro BarbosaNo ratings yet
- Ensino Estruturas Aço Engenharia ArquiteturaDocument171 pagesEnsino Estruturas Aço Engenharia ArquiteturapeanutfilNo ratings yet
- Ciclo Cardíaco: Etapas da Excitação e Contração do CoraçãoDocument9 pagesCiclo Cardíaco: Etapas da Excitação e Contração do CoraçãoSabrina XavierNo ratings yet
- Exercícios Química ElementarDocument15 pagesExercícios Química ElementarESCOLA CETECNo ratings yet
- Pedro IiDocument176 pagesPedro Iiliherberth moraesNo ratings yet
- Dimensionamento de Condutores2 PDFDocument24 pagesDimensionamento de Condutores2 PDFCrisanto Jimmy100% (1)
- Registrador de dados LogBox-AADocument9 pagesRegistrador de dados LogBox-AAEverson DantasNo ratings yet