Professional Documents
Culture Documents
Informe Grupo Del Cobre
Uploaded by
Deyvi Montañez CadilloOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Informe Grupo Del Cobre
Uploaded by
Deyvi Montañez CadilloCopyright:
Available Formats
UNIVERSIDAD NACIONAL
SANTIAGO ANTNEZ DE MAYOLO
FACULTAD DE INGENIERA DE MINAS, GEOLOGA Y METALURGIA
ESCUELA PROFESIONAL DE INGENIERA DE MINAS
QUMICA ANALTICA
INFORME DE LABORATORIO 03
SEPARACIN E IDENTIFICACIN DE CATIONES DEL GRUPO 2-A
GRUPO DEL COBRE
DOCENTE :
Ing. M.Sc. EDSON YUPANQUI TORRES
ALUMNO :
FIGUEROA TORRES FERNANDO
CDIGO :
101.0802.432
HUARAZ MAYO DEL 2012
INTRODUCCIN
El presente informe, respectivo a la segunda prctica de laboratorio
denominado Separacin e Identificacin de cationes del grupo 2-A grupo del
cobre, se refiere a las experimentaciones realizadas en el laboratorio de
Qumica Analtica
La marcha analtica de cationes es una tcnica de anlisis cualitativo que
permite la separacin e identificacin de los cationes presentes en una
muestra. Consiste en una serie de pasos sistemticos basados en reacciones
qumicas las cuales nos permiten en primer lugar separar cada catin
constituyente de la muestra aprovechando ciertas propiedades particulares
como lo es la solubilidad y el pH, y en segundo lugar identificarlos mediante
reacciones especficas de cada catin.
La separacin e identificacin de cationes del grupo 2-A, se realiz
cuidadosamente segn lo que indica el procedimiento del manual de
laboratorio, con la muestra dada por el docente. La marcha analtica se hizo
con la finalidad principal de obtener y reconocer si la muestra contena los
cationes de Hg
+2
; Pb
2+
; Bi
+3
; Cu
+2
y Cd
+2
obtenindose resultados satisfactorios
explicados en el informe.
Este informe es de gran importancia para nosotros los estudiantes de
qumica analtica, ya que se parte de la disolucin de muestras para realizar los
anlisis qumicos de muestras. Para la experimentacin cabe sealar que se
realiz cuidadosamente y en forma activa de todos los miembros del grupo; y
con los conocimientos adquiridos durante la explicacin de la prctica por el
docente.
I.OBJETIVOS
OBJETIVOS GENERALES:
Lograr la identificacin de los cationes del grupo del Cobre en la solucin preparada
por el docente, mediante la marcha analtica sistemtica.
OBJETIVOS ESPECFICOS:
Distinguir los distintos precipitados, colores, y factores que ayudan al reconocimiento
de los compuestos formados, que se obtienen mediante reactivos que producen
reacciones con los iones del Cu
+2
, Pb
+2
, Hg
+2
, Cd
+2
y Bi
+3
.
Reconocer la presencia de mercurio en una muestra, observando las caractersticas
fsicas del precipitado que forma, en este caso observaremos un precipitado de color
blanco o gris que es el Hg en presencia de Hg2Cl2. pero al final comprobaremos que en
nuestra muestra no hay presencia de mercurio.
Reconocer la presencia de Plomo en una muestra, observando las caractersticas
fsicas del precipitado que forma, en este caso observaremos un precipitado de color
negro que es el Bi. pero al final comprobaremos que en nuestra muestra no hay
presencia de Plomo.
Reconocer la presencia de Cobre en una muestra, observando las caractersticas fsicas
del precipitado que forma, en este caso observaremos un precipitado de color blanco
o gris que es el Cu2[Fe(CN)6]. al final comprobaremos que en nuestra muestra si hay
presencia de Cu.
Reconocer la presencia de cadmio en una muestra, observando las caractersticas
fsicas del precipitado que forma, en este caso observaremos un precipitado de color
amarillo que es el CdS en presencia de Hg2Cl2. pero al final comprobaremos que en
nuestra muestra no hay presencia de mercurio.
II.- FUNDAMENTO TEORICO:
Como se sabe en el anlisis cualitativo tiene por objeto identificar los componentes de una
sustancia, mezcla de sustancias o soluciones, y en forma el elemento componente o
grupos de elementos estn combinados entre si.
En la identificacin de una sustancia implica su transformacin, por lo regular con la ayuda
de otra sustancia de composicin conocida, en un compuesto nuevo que posee
propiedades caractersticas.
Para fines del anlisis cualitativo los iones de los metales o cationes ms comunes se
dividen en grupos. Estos grupos estn dado un orden y dependen del reactivo precipitante
que les corresponda, se puede establecer tambin que la clasificacin se basa en las
distintas solubilidades de los cloruros, sulfuros, hidrxidos, y carbonatos. Es por eso los
grupos ms comunes del anlisis de cationes son:
1.- Grupo de la plata
2.- Grupo del cobre
3.- Grupo del arsnico
4.- Grupo del hierro
5.- Grupo del Zinc
6.- Grupo del calcio
7.- Grupo de los metales alcalinos
Reacciones de los Cationes del Grupo del Cobre:
Cationes: Cu
+2
, Pb
+2
, Hg
+2
, Cd
+2
y Bi
+3
.
Reactivo del grupo: Sulfuro de hidrgeno en presencia de cido clorhdrico diluido.
REACCIONES DEL ION COBRE: Cu.
Se utiliza una solucin de sulfato de cobre, CuSO4.
1.- Con sulfuro de hidrogeno: se forma un pp negro de sulfuro de cobre. CuS, soluble en acido
nitrico diluido caliente y en solucin de cianuro de potasio
CuSO4 + H2S CuS +H2SO4
3CuS+8HNO3 3Cu(NO3)2 +4H2O +2NO +3S
2.- Con solucin de hidrxido de sodio: se forma un pp azul de hidrxido de cuprico Cu(OH)2
.p or ebullicin se transforma en oxido cuprico de color negro.
CuSO4 +2NaOH Cu(OH)2 + Na2SO4
Cu(OH)2 + Calor CuO + H2O
3.- Con solucin de hidrxido de amonio: se obtiene un pp celeste de sal bsica de cobre,
CuSO4 .Cu(OH)2, soluble en exceso de reactivo formndose el complejo sulfato
tetramincuprico [Cu(NH3)4]SO4 de color azul intenso .
2CuSO4 + 2NH4OH CuSO4.Cu (OH) 2 + (NH4)2SO4
CuSO4.Cu (OH)2 + (NH4)2SO4 + 6NH4OH 2[Cu(NH3)4]SO4 + 8H2O
4.- Con solucin de ferrocianuro de potasio: con soluciones neutras o cidas se forma un pp
pardo rojizo de ferrocianuro cprico, Cu2]Fe(CN)6], soluble en cidos minerales diluidos .
2CuSO4 + K [Fe(CN)6] Cu2[Fe(CN)6] + 2K2SO4
5.- Con solucin de cianuro de potasio: se forma un pop amarillo de cianuro cuprico Cu(CN),
que se descompone rpidamente en cianuro cuproso, Cu(CN) y ciangeno, (CN), el cianuro
cuproso se disuelve en exceso de reactivo formando una solucin incolora de la sal compleja,
cuprocianuro de potasio, K]Cu(CN)], cuya concentracin de iones cobre es tan pequea que
resulta insuficiente para dar, con sulfuro de hidrogeno, un pp (diferencia con el cadmio).
2CuSO4 + 4KCN 2Cu (CN)2 + 2K2SO4
2Cu (CN)2 Cu2 (CN)2 + (CN)2
Cu2 (CN)2 + 6KCN 2K3 [Cu (CN)4]
6.- Con solucin de yoduro de potasio: precipita yoduro cuproso se produce de color blanco,
CuI. Sin embargo, el yodo liberado tie de pardo toda la mezcla.
2CuSO4 + 4KI Cu2I2 + 2K2SO4
7.- Con solucin de sulfocianuro de potasio o amonio: se produce un pp de color negro
sulfocianuro cuprico, Cu (CNS), que pasa lentamente o inmediatamente por adicin de
solucin de acido sulfuroso a sulfocianuro cuproso, Cu (CNS), color blanco.
CuSO4 + 2NH4CNS Cu (CN) 2 + (NH4)2SO4
2Cu (CNS) 2 + H2SO3 + H2O Cu2 (CNS)2 + 2HCNS + H2 SO4
8.- Con hierro, sise introduce un clavo de hierro en una solucin de sal cprica, se obtiene un
deposito de color rojo de cobre.
CuSO4 + Fe FeSO4 + Cu
ENSAYOS POR VIA SECA:
1.- Ensayo al soplete: cuando los compuesto de cobre se calientan con carbonato de
sodio sobre carbn, se obtiene cobre metlico rojo sin oxido visible.
2.- Ensayo a la perla: calentando en llama oxidante es verde, en caliente, y azul en frio,
en llama reductora es roja.
3.- Ensayo a la llama: verde, especialmente en presencia de halogenuros.
REACCIONES DEL ION MERCURIO: Hg
+2
Se utiliza una solucin de cloruro mercrico: HgCl2
1.- Con sulfuro de hidrogeno: Inicialmente da un pp blanco de clorosulfuro de mercurio,
Hg3S2Cl2, luego cambia a amarillo i finalmente a negro de sulfuro mercrico, HgS, insoluble en
acido ntrico diluido caliente y en soluciones de hidrxidos alcalinos y de sulfuro de amonio. Es
soluble en agua regia.
3HgCl2 + 2H2S Hg3S2Cl2 + 4HCl
Hg3S2Cl2 + H2S 3HgS + 2HCl
3HgS + 2HNO3 + 6HCl 3HgCl2 + 2NO + 3S + 4H2O
2.- Con solucin de cloruro estannoso: Se produce un pp blanco de cloruro mercurioso, HgCl,
soluble en exceso de de reactivo con desprendimiento de mercurio metlico finamente
dividido de color gris.
2HgCl2 + SnCl2 Hg2Cl2 + SnCl4
Hg2Cl2 + SnCl2 2Hg + SnCl4
3.- Con solucin de hidrxido de sodio: Inicialmente se obtiene un pp de color rojizo de
cloruro bsico que luego se convierte, por exceso de reactivo, en oxido mercrico de color
amarillo.
HgCl2 + 2NaOH Hg + HgO + 2NaCl + H2O
4.- Con solucin de hidrxido de amonio: Se obtiene un pp blanco de cloruro aminomercurico,
Hg (NH2) Cl llamando pp blanco infusible porque se volatiza sin fundir.
HgCl2 + 2NH4OH Hg(NH2)Cl + NH4Cl + 2H2O
5.- Con solucin de yoduro de potasio: Se forma un pp de yoduro mercrico, HgI, soluble en
exceso de reactivo dando la sal compleja de mercuriyoduro de potasio.
HgCl2 + 2KI HgI2 + 2KCl
HgI2 + 2KI K2 [HgI4]
6.- Con cobre metlico: Al introducir una lmina de cobre en una solucin de cloruro
mercrico, esta se cubre de una pelcula gris de mercurio que adquiere, al frotarlo, una
apariencia plateada.
HgCl2 + Cu Hg + CuCl2
ENSAYOS POR VIA SECA:
Accin del calor: Todos los compuestos del mercurio cuando se caliente en un
pequeo tubo de ensayo con un exceso de carbonato de sodio anhidro, dan un espejo
gris, constituido por finas gotas de mercurio, en la parte superior del tubo.
REACCIONES CON EL ION BISMUTO: Bi
+3
Se utiliza una solucin de nitrato de bismuto: Bi(NO3)3
1.- Con sulfuro de hidrogeno: Se produce un pp pardo de sulfuro de bismuto, Bi2S3,
Insoluble en cidos diluidos en frio y en solucin de sulfuro de amonio, soluble en acido ntrico
diluido caliente y en acido clorhdrico concentrado a ebullicin.
2 Bi(NO3)3 + 3H2S Bi2S3 + 6HNO3
Bi2S3 + 8HNO 2 Bi(NO3)3 + 2NO + 3S + 4H2O
2.- Con solucin de hidrxido de sodio: Se produce un pp de hidrxido de bismuto, Bi(OH)3,
soluble en cidos. Por ebullicin se torna blanco- amarillento debido a la deshidratacin
parcial. Si a este pp se le agrega perxido de hidrogeno, se produce acido bismutico de color
pardo.
Bi2S3 + 3NaOH Bi(OH)3 + 3NaNO3
Bi(OH)3 + Calor Bi(OH) + H2O
BiOH + H2O2 HBiO3 + H2O
3.- Con solucin de hidrxido de amonio: Se obtiene un pp blanco de sal bsica de bismuto
(BiO) NO3, insoluble en exceso de reactivo en exceso de reactivo a diferencia del cobre y del
cadmio.
Bi2S3 + 2NH4OH (BiO)NO3 + 2NH4NO3 + H2O
4.- Con solucin de yoduro de potasio: Se obtiene un pp pardo de yodurote bismuto, BiI,
soluble en exceso de reactivo, dando una solucin amarilla de sal compleja de tetrayoduro de
bismuto y potasio, K {BiI4]. El complejo se descompone por dilucin dando primero un pp de
yoduro y luego un pp anaranjado de yoduro bsico, (BiO) I
Bi(NO3)3 + 3KI BiI3 + 3KNO3
BiI 3 + KI K [BiI4]
K [BiI4] BiI3 + KI
BiI3 + H2O (BiO) I + 2HI
5.- Con solucin de estannito de sodio: En soluciones fras se obtiene un pp negro de bismuto
finamente dividido. El reactivo se prepara agregando una solucin de hidrxido de sodio a una
solucin de hidrxido se sodio a una solucin de cloruro estannoso hasta que se disuelva el pp
inicial blanco de hidrxido estannoso.
Sn(OH)2 2NaOH Na2SnO2 + 2H2O
2Bi(NO3)3 + 6NaOH + 3Na2SnO2 2Bi + 3Na2SnO2 + 6NaNO3 +3H2O
6.- Con agua: las soluciones de sales de bismuto al vertirse sobre gran volumen de agua se
produce un pp blanco de una sal bsica de bismuto, soluble en cidos minerales diluidos e
insolubles en cido trtrico (diferencia del antimonio) y en soluciones de hidrxidos
alcalinos(diferencia del estao).
Bi(NO3)3 + H2O (BiO)NO3 + 2HNO3
BiCl3 + H2O (BiO)Cl + 2HCl
ENSAYOS POR VIA SECA:
Ensayo al soplete: Cuando un compuesto de bismuto se calienta sobra carbn con
carbonato de sodio, en la llama de un soplete, se obtiene un regulo quebradizo de
bismuto metalico, rodeado por una incrustacin amarilla de oxido.
REACCIONES DEL ION CADMIO: Cd
+2
Se utiliza una solucin de sulfato de cadmio: CdSO4.
1.- Con sulfuro de hidrogeno: Se obtiene un pp amarillo de sulfuro de cadmio, CdS, soluble en
cidos ntricos y sulfricos diluidos y en caliente (diferencia con el cobre); es insoluble en
solucin de cianuro de potasio (diferencia con el cobre).
CdSO4 + H2S CdS H2SO4
2.- Con solucin de hidrxido de sodio: Se obtiene un pp. Blanco de hidrxido de cadmio,
Cd(OH)2, insoluble en exceso de reactivo.
CdSO4 + 2NaOH Cd(OH)2 + Na2SO4
3.- Con solucin de hidrxido de amonio: Se obtiene un pp blanco de hidrxido de cadmio,
Cd(OH)2, soluble en exceso de reactivo dando una sal compleja de sulfato tetra amn cdmico,
[Cd(NH3)4]SO4 (diferencia del plomo y bismuto).
CdSO4 + 2NH4OH Cd(OH)2 + (NH4)2SO4
Cd(OH)2 + (NH4)2SO4 + 2NH4OH [Cd(NH3)4]SO4 + 4H2O
4.- Con solucin de cianuro de potasio: Se obtiene un pp blanco de cianuro de cadmio,
Cd(CN)2, soluble en exceso de reactivo dando el complejo de cadmiocianuro de potasio. K2
[Cd(CN)4]. Por disociacin del complejo, se produce una concentracin suficiente grande de
iones de cadmio dando con el sulfuro de hidrogeno un pp amarillo de sulfuro de cadmio
(diferencia del cobre).
CdSO4 + 2KCN Cd(CN)2 + K2SO4
Cd (CN) 2 + 2KCN K2 [Cd(CN)4]
K2 [Cd (CN)4] + H2S CdS + 2KCN + 2HCN
5.- Con solucin de sulfocianuro de amonio: No se produce ningn pp (diferencia con el
cobre).
ENSAYOS POR VIA SECA:
Ensayo al soplete: Todos los compuestos de cadmio, cuando se calienta sobre carbn
con carbonato de sodio, dan una incrustacin parda de oxido de cadmio, CdO.
DESCRIPCIN DE LA MARCHA
Los iones Cu
+2
, Pb
+2
, Hg
+2
, Cd
+2
y Bi
+3
. Precipitan por accin del sulfuro de hidrogeno, en
forma de sulfuros: CuS, PbS, HgS, CdS y Bi2S3. La separacin y reconocimiento de ellos se basa
en los siguientes hechos:
1.- El HgS es insoluble en HNO3 diluido, los sulfuros de plomo, cobre, bismuto y cadmio se
disuelven con formacin de nitratos.
3PbS + 8HNO3 3Pb(NO3)2 + 2NO + 3S + 4H2O
Bi2S3 + 8HNO3 2Bi(NO3)3 + 2NO + 3S + 4H2O
2.- Una reaccin que confirma la presencia de mercurio, se basa en la transformacin de HgS,
mediante agua regia, en HgCl2, y la reduccin de este ultimo con solucin de SnCl2. La
formacin de un pp blanco o gris confirma la presencia de mercurio.
3HgS + 2HNO3 + 6HCl 3HgCl2 + 3S + 2NO + 4H2O
2HgCl2 + SnCl2 Hg2Cl2 + SnCl4
Hg2Cl2 + SnCl2 2Hg + SnCl4
3.- El filtrado del tratamiento con acido ntrico contiene los nitratos de plomo, bismuto, cobre
y cadmio.
Pb(NO3)2, Bi(NO3)3, Cu(NO3)2 y Cd(NO3)2.
4.- La adicin de un exceso de solucin concentrada de hidrxido de amonio, conduce a la
precipitacin del Pb(OH)2 y Bi(OH)3 y la formacin de sales complejas solubles de
[Cu(NH3)4](NO3)2 y [Cd(NH3)4](NO3)2.
Pb(NO3)2 + 2NH4OH Pb(OH)2 + 2NH4NO3
Bi(NO3)3 + 3NH4OH Bi(OH)3 + 3NH4NO3
2Cu(NO3)2 + 2NH4OH Cu(NO3)2.Cu(OH)2 + 2NH4NO3
Cu(NO3)2.Cu(OH)2 + 2NH4NO3 + 6NH4OH 2[Cu(NH3)4](NO3)2+ 8H2O
Cd(NO3)2 + 2NH4OH Cd(OH)2 + 2NH4NO3
Cd(OH)2 + 2NH4NO3 2NH4OH [Cd(NH3)4](NO3)2 + 4H2O
5.- El filtrado del tratamiento con exceso de NH4OH, se puede contener los complejos
amoniacales de cobre y cadmio. Si la solucin es incolora est ausente el cobre. El pasaje de
H2S por la solucin compleja precipita CdS de color amarillo.
[Cd(NH3)4](NO3)2 + H2S + 2H2O CdS + 2NH4NO3 + 2NH4OH
Si el cobre esta presente la solucin de es color azul intenso. Se divide en dos
porciones desiguales. A la porcin menor la adicin de cido actico descompone el complejo
en Cu (NO3)2 y CH3COONH4; la solucin de K4 [Fe (CN)6] produce un pp pardo rojizo de
Cu2 [Fe (CN)6].
[Cu (NH3)4](NO3)2 + 4CH3COOH Cu (NO3)2 + 4CH3 COONH4
K4 [Fe (CN)6] + 2Cu (NO3)2 Cu2 [Fe (CN)6] + 4KNO3
La adicin de un exceso de solucin de KCN, a la porcin mayor del complejo
amoniacal, convierte los complejos amoniacales en los cianuros complejos, incoloros: cupro-
cianuro de potasio, K3 [Cu (CN)4] y cadmio-cianuro de potasio, K2 [Cd (CN)4].
2[Cu (NH3)4] (NO3)2 + 10KCN + 8H2O 2K [Cu (CN)] + 4KNO + (CN) + 8NHOH
[Cd (NH3)4](NO3)2 + 4KCN + 4H2O K2 [Cd (CN)4] + 2KNO3 + 4NH4 OH
Con el cupro-cianuro de potasio, la concentracin de los iones cuprosos producidos
por la ionizacin secundaria del ion complejo, [Cu(CN)] , es insuficiente para alcanzar el
producto de solubilidad del CuS en solucin de HS, y por tanto no hay precipitacin. Por otra
parte, el cadmiocianuro de potasio es relativamente inestable, y la concentracin de los iones
cadmio que proviene de la disociacin secundaria del [Cd(CN)] es suficiente para sobre pasar el
producto de solubilidad del CdS cuando se hace pasar por la solucin HS logrndose su
precipitado.
K3 [Cu (CN)4] 3K
+
+ [Cu (CN4)
-3
] 3K
+
+ Cu
+
+ 4CN
-
K2 [Cd (CN) 4] 2K
+
+ [Cd (CN) 4]
-2
2K
+
+ Cd
+2
+ 4CN
-
6.- El residuo del tratamiento con exceso de NH4OH puede contener Pb(OH)2 y Bi(OH)3. El
calentamiento con 5ml de solucin de NaOH conduce a la solubilizacin del Pb(OH)2
formndose plmbito de sodio incoloro, mientras que el Bi(OH)3 permanece inalterable. La
adicin, al filtrado incoloro, de acido actico y luego solucin de K2CrO4 precipita PbCrO4 de
color amarillo.
Pb(OH)2 + 2NaOH Na2PbO2 + 2H2O
Na2PbO2 + 4CH3COOH Pb(CH3OO)2 + 2CH3COONa + 2H2O
Pb(CH3OO)2 + K2CrO4 PbCrO4 + 2CH3COOK
La adicin, al residuo de Bi(OH)3, de solucin de estannito de sodio reduce el Bi(OH)3
a bismuto metalico y oxidndose el estao a estannato de sodio.
2Bi(OH)3 + 3Na2SnO2 2Bi + 3Na2SnO3 +3H2O
III.- MATERIALES, INSTRUMENTOS, EQUIPOS Y
REACTIVOS UTILIZADOS:
MATERIALES:
- 02 Vasos de precipitacin de 150ml.
- 02 Matraces Erlenmeyer de 150ml.
- 04 tubos de ensayo
- 01 Agitador de vidrio.
- 01 Embudo.
- 01 gradilla de tubos
- 01 Cocina elctrica.
- 01 Pipeta graduada de 10ml
- 01 Frasco lavador
- Papel filtro
REACTIVOS
- HCl cc
- NH4OH 2N
- NH4OH 3N
- HNO3 CC
- KI AL 0.5N
- CH3COOH
- K2CrO4
- H2SO4 cc
- K4(Fe(CN)6)
- Na2S
- Na2HPO4
- H2S
- NH4Cl
- NaOH 3N
- HNO3
- SnCl2 0.2M
- CH3COONH4 cc
- CH3COOH 6M
- Na2SnO2 (SnCl2 + NaOH )
- HNO3 2N
- Na2HPO4
- KCNa
- H2O2 al 3%
IV, PROC E DlMlE NTO
I Ajuste le la ncicfez:
' '' : , ' r'' . , . . ' ! . .'. .' '
, ! . , ! , .! '. ! ,
- mis- ' ' ' , ' ! ' ' . ' , .
' . ! . , ! ) . : - . ' . , L ' .. '' '_ , ''' " ' :
.// Precipitacin de los cntioncs Jet grupo ll
[SrCl,"] + 2S'-- 6Cl + SnS, pp artarillo
2H AsO + SS ' + 12H.O" m 20H O + S + As_S., pj ar arillu
Observe las reacciones de forrtacin le los sulfuros del sbgrupo II B, a
partir dc complejos. todcs stos con su mxima valencia. debiJo n la oxidacin
cun H.O_ pcru al pusar H;S (agente redrctoi ) retuce al Sb y As' a Sb" y
/\ ' ie peclivur ente, en cnnbo el Sn no es afectaJc por el poder reductor del
H,S, debiJo a que el medio clebe ser dbilrtenle cido y no fuertemente cido
(debido BI carctB'f i3f\ ftcro del Sn).
La solucin filtrado se hierve inmediatamente pam expulsar el exceso de
H S y para concentrar la sclucin que contiene los ca tiones del grupo III al
V, si la muestra solo contiene ca tiones del grupc ll, sta filtrado se elimina
Si no se elimina el H 5 por ebullicin, este puede oxiJarsc a SO' y
;recipitnr inmediatamente el Oa, Ba y Sr.
Puede ocurrir que al concentrar el filtrado, se formen precipitadas amarillos
de As S que haya pasarlo, esto ocurre con frecuencia, entonces se aade
2 gotas de HCl cc. y se pasa una corriente de H.S y se contina la
ebullicin hasta precipitacin total del As,S y expulsin Jet H,S. Se flllra el
precipitado y se comprueba el /\s conforme se indicnr en el subgrtpo II B.
el lillriIu Jxorto rl' lurLidez y precipila1s se ginra en un fris:D
rotulaJo (solucin -cgrrpus III al V)
Lavnr los prccipitraJos con agia silfldricada (se prepara satrrando con
H..S, aqu.n lcrviJr y NHNO o NHCI), por 3 4 veces, cn ste liq iJ le
lavaJc se inpicJc la uxidacir a sulfnls cte los prccipilads y se evita la
fornacin dc cluiJcs
3, Separacin do los subgrupos del Cobre y del Arsnico
Los precipitaJs insolubles son sulfuros del subgrupo del Ccbre que
dobon ai lizarsc ul momento. por que ci contacte con cl oxigcu Jet
aire se oxiJan a sulfatos, si so guardan hacerlo fuera del contacto clel
aire (tubo tapaJo)
. s el i,) s . en i,i . i..,
Preparacin del (NH ),S,.
Iclcntific.a c ion Jet su bgrupo II-A o su bgrupo dcl cobre
4 Separacin del HgS le los restantes s ulfros
Rec oi1ocii11icnl o lot Ug'
<'
(]||j| C)f] .||J |i(((| . 3f]||( . (! ' ' (!| y'( f f)|. f) '||| f ' t() | ( .|| , . '. |
( j: ].| !.. (.'(J:t!t'..]!|() |(t]1jCjtJ|L f !, ' C j[;L ,9[l t".?J 'X|?!|| 'i.|||f'':*| f!|. v'.|
, ! . ) . , . . , . .! . . ,
, ! . . ' ) ! '
. .
. . ' -
f Sc j.3rncion Jcl [loi1o clcl lisr1uto, cohrc y cnclnJio
C.J NCJ . i I l, O , . lO: + ?'l INO , s..ltir.il i
/' lJertificucion o rcconocim icrto del plomo
". Sc jar.a cin dcl Lisinuto, Jet coLrc y cadnio
IcJcntific.a cin o reconociri iento del bismuto
10. Idettificacin o reconocimiento del cobre
5.CONCLUSIONES:
Se determin la separacin e identificacin de los cationes del sub grupo
II-A (Cd
+2
;Cu
+2
; Hg
+2
; Pb
+2
; Bi
+3
)
Se lleg a comprobar los colores de identificacin de cada uno de los
cationes, con la cual se puede determinar a presencia o ausencia de cada
uno de los cationes.
Cada uno de los cationes tienen una forma diferente de reaccionar con
cada elemento precipitante, o mediante la combustin ya que algunos de
ellos son voltiles.
Evitar los excesos y las prdidas de muestra y reactivos, ya que se
pueden perder elementos.
Mayor observacin en los colores de los precipitados y las soluciones, ya
que mediante cada uno de los colores mostrados se puede percibir la
presencia o ausencia de cada catin.
6.RECOMENDACIONES
No se debe utilizar los reactivos en exceso
Debemos seguir en forma sistemtica todos los pasos de la marcha
analtica.
Se deben utilizar los reactivos con mucho cuidado, especialmente los
cidos concentrados.
1. BIBLIOGRAFA:
- Arribas S., MJ. lvarez. . Inst. Qumica
Analitica. 1988. Madrid, Espaa.
- Burriel F.F. Lucena, S. Arribas Qumica Analtica
cualitativa. Ed. Paraninfo, Madrid 1979
- Burriel F. Hernndez Mndez... Qumica Analtica
cualitativa. XV Ed. Madrid 1992.
- Harvey E.D... Qumica Analtica
Moderna. Ed.Mc Graw Hill S.A. 2002.
APENDICE
2 6
3
4
+
+
8.CUESTIONARIO:
1. Establezca las reacciones qumicas de separacin e identificacin de los
cationes del sub grupo II-A, anotando las observaciones realizadas en cada
caso.
a) Ajuste de acidez:
1. 2H
2
O
2
+ calor 2H
2
O + O
2
La reaccin de oxidacin del Sn
+2
Sn
+4
, por accin del H O , es:
2 2
2. 4H
3
O + Sn
+2
+ O
2
+ 6Cl
SnCl
2
+ 6H
2
O
El calentamiento con HCl destruye los iones NO
, y reduce al
Cr
+6
Cr
+3
:
3. 16H
3
O + 2CrO
2
+ 6Cl
2Cr
+3
+ 3Cl
2
+ 24H
2
O
Papel de tornasol: azul (alcalina)
b) Precipitacin de cationes del grupo II:
Al agregar Na
2
S forman los siguientes sulfuros:
1. Hg
+2
+ S
2
HgS
2. Pb
+2
+ S
2
PbS
pp. Negro.
pp. Negro.
6
2 3
3. 2Bi
+3
+ 3S
2
Bi S
4 . Cu
+2
+ S
2
CuS
pp. Pardo.
5 . Cd
+2
+ S
2
CdS
pp. Negro.
pp. Amarillo.
6. 2(SbCl
1
) + 3S
2
6Cl
+ Sb
2
S
3
|
2
|
2
pp. Amarillo.
7. SnCl
6
+ 2S 6Cl
+ SnS
2
pp. Amarillo.
2 4
+
8. 2H AsO
+ 5S
2
+12H
3
O 20H
2
O + S + As
2
S
3
pp. Amarillo.
c) Separacin del HgS :
1. 3PbS + 8HNO
3
3Pb(NO
3
)
2
+ 2NO + S + 4H
2
O
2. Bi
2
S
3
+ 8HNO
3
2Bi(NO
3
)
3
+ 2NO + S + 4H
2
O
3 . 3CuS + 8HNO
3
3Cu(NO
3
)
2
+ 2NO + S + 4H
2
O
4 . 3CdS + 8HNO
3
3Cd(NO
3
)
2
+ 2NO + S + 4H
2
O
d) Reconocimiento del Hg
+2
:
1. 3HgS + 2HNO
3
+ 6HCl 3HgCl
2
+ 2NO + 3S + 4H
2
O
Se le agrega una moneda:
2. HgCl
2
+ Cu Hg + CuCl
2
La moneda presenta un color plateado brillante, quiere decir que existe
presencia de mercurio.
Se le agrega SnCl
2
:
3. SnCl
2
+ 2HgCl
2
Hg
2
Cl
2
+ SnCl
4
En exceso de SnCl
2
:
4. SnCl
2
+ Hg
2
Cl
2
2Hg + SnCl
4
e) Separacin del plomo, bismuto y cadmio:
1. Pb(NO
3
)
2
+ H
2
SO
4
PbSO
4
+ 2HNO
3
pp. Blanco.
2. 2Bi(NO
3
)
3
+ 3H
2
SO
4
Bi
2
(SO
4
)
3
+ 6HNO
3
Solucin.
3. Cu(NO
3
)
2
+ H
2
SO
4
CuSO
4
+ 2HNO
3
Solucin.
4 . Cd(NO
3
)
2
+ H
2
SO
4
CdSO
4
+ 2HNO
3
f) I dentificacin del plomo:
Solucin.
1 . PbSO
4
+ 2CH
3
COONH
4
Pb(CH
3
COO)
2
+ (NH
4
)
2
SO
4
2 . Pb(CH
3
COO)
2
+ K
2
CrO
4
PbCrO
4
+ 2CH
3
COOK
pp. Amarillo.
g) Separacin del bismuto, cobre y cadmio:
1. Bi
2
(SO
4
)
3
+ 6NH
4
OH 2Bi(OH)
3
+ 3(NH
4
)
2
SO
4
pp. Blanco coposo.
2. 2CuSO
4
+ 2NH
4
OH CuSO
4
.Cu(OH )
2
+ (NH
4
)
2
SO
4
3 . CuSO
4
.Cu(OH)
2
+ (NH
4
)
2
SO
4
+ 6NH
4
OH 2|Cu(NH
3
)
4
|SO
4
+ 8H
2
O
Complejo soluble azul.
4. CdSO
4
+ 2NH
4
CH Cd (OH )
2
+ (NH
4
)
2
SO
4
6
6
5. Cd(OH)
2
+ (NH
4
)
2
SO
4
+ 2NH
4
OH |Cd(NH
3
)
4
|SO
4
+ 4H
2
O
h) I dentificacin del bismuto:
Complejo soluble incoloro.
1 . Na
2
SnO
2
+ Bi(OH)
3
2Bi + Na
2
SnO
3
+ H
2
O
pp. Negro.
2 . Bi(NO
3
)
3
+ Na
2
HPO
4
BiPO
4
+ NaNO
3
+ H
2
O
pp. Blanco cristalino.
3. Bi(NO
3
)
3
+ 3H
2
S Bi
2
S
3
+ 6HNO
3
i) I dentificacin del cobre:
pp. Pardo.
1. K
4
|Fe(CN )
6
| 4K
+
+ Fe(CN )
4
2. Fe(CN )
4
+ 2Cu
+2
Cu
2
|Fe(CN )
6
|
pp. Pardo rojizo.
3 4
4
j) I dentificacin del cadmio:
| |
+2 2
1. Cd (NH
3
)
4
SO
4
Cd (NH
3
)
4
+ SO
4
2. Cd (NH )
+2
Cd
+2
+ 4NH
3
3. Cd
+2
+ S
2
CdS
pp. Amarillo.
2. Qu otras reacciones de identificacin puede sugerir para cada catin?
1. 3HgS + 2NHO
3
+ 6HCl 3HgCl
2
+ 2NO + 3S + 4H
2
O
2. Sn(OH )
2
+ 2NaOH Na
2
SnO
2
+ 2H
2
O
3 . Bi(NO
3
)
3
+ Na
2
HPO
4
BiPO
4
+ NaNO
3
+ H
2
O
4 . Cd(CN)
2
Cd
+2
+ 4CN
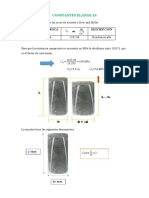
3. haga un resumen esquematico de la marcha analtica del subgrupo I I A
MARCHA ANALTICA DE CATIONES DEL GRUPO II-A DEL COBRE
Aproximadamente 75 ml de solucin
preparada.
MUESTRA
(Hg
+2
; Pb
2+
; Bi
+3
; Cu
+2
; Cd
+2
; As
+3
; Sb
+3
; Sn
+2
).
+
Agregar 3-5 gotas de H2O2 al 3% - hervir hasta volumen.
+
Agregar 3-5 gotas HCl cc herbir 10 minutos.
+
NH4OH 2N-(solucion alcalina).
+
HCl cc( 1 gota de HCl cc/mL soluc muestra)(ph=0.5).
Calentar la muestra prxima as ebullicin .
+
H2s(Na2S) hasta precipitacin completa.
+
H2O destilada fra igual al volumen de la muestra.
+
H2S (Na2S) hasta precipitacin completa-filtrar.
Precipitado Solucin
Grupo II
Subgrupo II-A: HgS; PbS; Bi2S3; CuS; CdS
Subgrupo II-B: Sb2S3; SnS2; As2S3
Lavar 3 veces los pp con agua sulfurada(Na2S) y
NH4Cl
+
5mL NaOH 3N-calentar y filtrar
Muestra general:_ III,IV,V-hervir 10 min-guardar
La solucin se desecha (comprobar si la precipitacin
fue completa)
Precipitado Solucin
Subgrupo II-A: HgS; PbS; Bi2S3; CuS; CdS
Lavar el pp con agua sulfurada(Na2S) y NH4Cl
+
10 mL HNO3 (1:2)-hervir 1 min y filtrar
Subgrupo II-B: Sb2S3; SnS2; As2S3(guardar)
HgS
Pasar a un vaso
+
1 mL Agua regia- hervir
+
2 mL Agua destilada
HgCl2
Pb(NO3)2; Bi(NO3)3; Cu(NO3)2; Cd(NO3)2
+
2-5 gotas H2SO4 cc
Hervir 5 min (aparicin de humos blancos)-
filtrar
Precipitado
Solucin
A) HgCl2-fria
+
Gotas SnCl2 0.2 M
Hg-H g2Cl2
Pp. Blanco-Gris-negro
B)HgCl2 (vaso)
+
Moneda de cobre
limpia-calentar
Hg moneda plateada
+2
+2
+2
+2
Precipitado Solucin
PbSO4(pp blanco)
Labar el pp con agua
acidulada de H2SO4
Pasar a un vaso
+
1 mL CH3COONH4 cc
Calentar hasta
disolucin del pp
+
3-4 otas CH3COOH 6 M
+
Bi2(SO4)3; CuSO4;CdSO4;
+
NH4OH 3N(solucin alcalina)-filtrar
Bi(OH3) (pp blanco gel)
Cu(NH3)4 ;
Cd(NH3)4
Gotas K2CrO4
A)BiOH3frio
+
Na2SnO2
B) BiOH3
+
Analisis del Cu
Cu(NH3)4
Analisis del Cd
Cd(NH3)4
PbCrO4 pp amarillo
(SnCl2+NaOH)
Bi pp negro
A) BiOH3
+
Gotas Na2HPO4
BiPO4 pp blanco
cristalino
HNO3 2N
(disolucin del pp
Bi(NO3)3
B) BiOH3
+
Na2S
Bi2S3 pp pardo
+
Gotas CH3COOH 6M
(Solucin acida)
+
K4[Fe(CN)6]
Cu2[Fe(CN)6] pp
A) sin Cu
+
Na2S
Calentar
CdS pp
b)con Cu
+
KCNa
De color
azul
+
Na2S
CdS pp
amarillo
You might also like
- CUESTIONARIODocument3 pagesCUESTIONARIOMelisa DanisiNo ratings yet
- Informe de Quimica Analitica 3Document24 pagesInforme de Quimica Analitica 3Max Gerson Fer Fernandez100% (1)
- Lab 4 Subgrupo Del CobreDocument7 pagesLab 4 Subgrupo Del CobreMendoza RomeroNo ratings yet
- Informe - Reacciones de Los Cationes Del Grupo Del CobreDocument27 pagesInforme - Reacciones de Los Cationes Del Grupo Del Cobreraul6819100% (1)
- Informe Delaboratorio #05Document12 pagesInforme Delaboratorio #05FernandoJonathan Figueroa TorresNo ratings yet
- Informe N..4Document25 pagesInforme N..4Junior MirandaNo ratings yet
- Cationes Del 2do GrupoDocument15 pagesCationes Del 2do GrupoLeninDelPinoAlvarezNo ratings yet
- LABoratorio Analisis Quimico UNIDocument26 pagesLABoratorio Analisis Quimico UNIKenny SalazarNo ratings yet
- Test 7 Acidimetria...........................Document2 pagesTest 7 Acidimetria...........................Jhonatan EGNo ratings yet
- 2° PC-2021-2-MinasDocument3 pages2° PC-2021-2-MinasJohn BMNo ratings yet
- Análisis Del Grupo I de CationesDocument6 pagesAnálisis Del Grupo I de CationesElayne GomezNo ratings yet
- Marcha de Cationes Del Grupo IIIDocument13 pagesMarcha de Cationes Del Grupo IIILuz Vanessa CasalloNo ratings yet
- Cuestionario 7 y 8 Analisis QuimicoDocument6 pagesCuestionario 7 y 8 Analisis QuimicoSamir LimaNo ratings yet
- Sexto LaboratorioDocument18 pagesSexto LaboratorioFabrizioNo ratings yet
- Informe de ElectroquimicaDocument59 pagesInforme de ElectroquimicaJimmy Jiménez33% (3)
- 2do Examen Parcial de Quimica UNMSMDocument5 pages2do Examen Parcial de Quimica UNMSMFLAVIO EDUARDO DE LA CRUZ QUISPENo ratings yet
- Ensayo A La Perla de BoraxDocument9 pagesEnsayo A La Perla de Boraxjoneshnad211094No ratings yet
- Informe de Laboratorio N°7 Y 8de Quimica Analitica InstrumentalDocument18 pagesInforme de Laboratorio N°7 Y 8de Quimica Analitica InstrumentalSheyla Maybee Yantas Espiritu0% (1)
- Identificación analítica del segundo grupo de cationesDocument23 pagesIdentificación analítica del segundo grupo de cationesDiegoNo ratings yet
- 7mo Informe de Analisis QuimicoDocument15 pages7mo Informe de Analisis QuimicoSamir Lima100% (1)
- TEST 5 Cationes Del Grupo IVDocument3 pagesTEST 5 Cationes Del Grupo IVJhonatan EGNo ratings yet
- Informe de Laboratorio 7Document3 pagesInforme de Laboratorio 7KatyEscaleraNo ratings yet
- Separación e Identificación de Cationes Del Sub Grupo Ii A o Sub Grupo Del CobreDocument5 pagesSeparación e Identificación de Cationes Del Sub Grupo Ii A o Sub Grupo Del CobrePatricia Inocente MorenoNo ratings yet
- Precipitacion de Sulfuros MetalicosDocument5 pagesPrecipitacion de Sulfuros Metalicoskatiavilac50% (2)
- Laboratorio 6 Analisis QuimicoDocument20 pagesLaboratorio 6 Analisis QuimicoAbath Vlandimir100% (1)
- Laboratorio 4 de Fisica 3 FIGMMDocument15 pagesLaboratorio 4 de Fisica 3 FIGMMRoger Cubas100% (2)
- Informe 6 Análisis QuímicoDocument27 pagesInforme 6 Análisis QuímicoAntony Walter Maximiliano CusiNo ratings yet
- Analisis de Aniones Del Grupo IVDocument4 pagesAnalisis de Aniones Del Grupo IVYonar Shmit Gallo QuispeNo ratings yet
- Determinación de cloruros y cianuros en muestras de sal, agua y materiales usando los métodos de Mohr y LiebigDocument29 pagesDeterminación de cloruros y cianuros en muestras de sal, agua y materiales usando los métodos de Mohr y LiebigJorman Iván Barrera VergaraNo ratings yet
- Analisis Del Grupo IVDocument25 pagesAnalisis Del Grupo IValexNo ratings yet
- Análisis cualitativo de cationesDocument8 pagesAnálisis cualitativo de cationeswilder condori choque0% (2)
- Rayos GamaDocument9 pagesRayos GamaJuan CarlosNo ratings yet
- Remoción de Metales PesadosDocument14 pagesRemoción de Metales PesadosBrayan Rodriguez Medina100% (1)
- Disolución de muestras sólidasDocument13 pagesDisolución de muestras sólidasRosember Romero AcuñaNo ratings yet
- Lab 5 Analisis Quimico 18 1Document19 pagesLab 5 Analisis Quimico 18 1juan ramirez huamanNo ratings yet
- Examen de Analitica UnasamDocument1 pageExamen de Analitica UnasamCristian V'pNo ratings yet
- Preparacion de Pulpas de MineralesDocument4 pagesPreparacion de Pulpas de MineralesyordhyNo ratings yet
- 7°informe de LaboratorioDocument31 pages7°informe de LaboratorioANGEL DAVID MAMANI GUARDIANo ratings yet
- Marcha de cationes Pb, Ag y HgDocument13 pagesMarcha de cationes Pb, Ag y HgSantos Anibal Raico CusquisibanNo ratings yet
- Informe-Laboratorio N°03-Analisis QuímicoDocument9 pagesInforme-Laboratorio N°03-Analisis QuímicoBRYAN MORI AREVALO100% (1)
- Informe 02Document14 pagesInforme 02Cielo Azul0% (1)
- Informe N°2 Quimica AnaliticaDocument13 pagesInforme N°2 Quimica AnaliticaMax Gerson Fer FernandezNo ratings yet
- Determinacion Del CobreeeDocument10 pagesDeterminacion Del CobreeeJorge AyalaNo ratings yet
- Informe 3 Aniones CorregidoDocument23 pagesInforme 3 Aniones CorregidoDenis Garcia GarciaNo ratings yet
- SEPARACIÓN Y RECONOCIMIENTO DE CATIONES IIADocument6 pagesSEPARACIÓN Y RECONOCIMIENTO DE CATIONES IIAPatricia Inocente MorenoNo ratings yet
- Laboratorio Informe Análisis Químico Tema 2 Uni Figmm 2017Document10 pagesLaboratorio Informe Análisis Químico Tema 2 Uni Figmm 2017Joel Mamani100% (1)
- 6to Laboratorio de Análisis Químico Reconocimiento de AnionesDocument21 pages6to Laboratorio de Análisis Químico Reconocimiento de AnionesRaúl Berrospi Rodriguez100% (1)
- Informe - Grupo de La Plata FherDocument6 pagesInforme - Grupo de La Plata FherGC FernandoNo ratings yet
- UPTC: 2.1% humedad en carbónDocument8 pagesUPTC: 2.1% humedad en carbónPaula A FernandezmjNo ratings yet
- Cuestionario Labo Nro 3Document4 pagesCuestionario Labo Nro 3Brayan CondoriNo ratings yet
- Analisis 7 8 InformeDocument21 pagesAnalisis 7 8 InformeDante MontañezNo ratings yet
- Marcha Analítica de Separación de Los Cationes Del Subgrupo Del Arsenico y Del Subgrupo Del CobreDocument13 pagesMarcha Analítica de Separación de Los Cationes Del Subgrupo Del Arsenico y Del Subgrupo Del CobreLuisQuiñones100% (1)
- Análisis químico de aniones mediante reacciones cualitativasDocument17 pagesAnálisis químico de aniones mediante reacciones cualitativasJimmy FiestasNo ratings yet
- 7 Informe de Analisis QuimicoDocument20 pages7 Informe de Analisis QuimicowillyballNo ratings yet
- Análisis Tercer Grupo CationesDocument16 pagesAnálisis Tercer Grupo CationesSamir LimaNo ratings yet
- Determinacion de CalcioDocument10 pagesDeterminacion de CalcioAnonymous JHU0OjLOdNo ratings yet
- 9no Informe 2Document15 pages9no Informe 2Marcelo TorresNo ratings yet
- Comportamiento del capacitor planoDocument10 pagesComportamiento del capacitor planoDaniel GiraldoNo ratings yet
- Informe #8-Química General A1Document25 pagesInforme #8-Química General A1Andres Arturo Lee Sanchez Castillo75% (8)
- MARCHA GRUPO II-A O DEL COBRE Informe....Document20 pagesMARCHA GRUPO II-A O DEL COBRE Informe....manuelNo ratings yet
- Metodos de Estudio de Los Yacimientos-ADocument23 pagesMetodos de Estudio de Los Yacimientos-ADeyvi Montañez CadilloNo ratings yet
- Jm20100225 Geomecanica RosauraDocument75 pagesJm20100225 Geomecanica RosauraFrank Mauricio LuceroNo ratings yet
- Procesos Formación Minerales MagmáticDocument13 pagesProcesos Formación Minerales MagmáticDeyvi Montañez CadilloNo ratings yet
- Teoria de Las Placas Tectonicas (2013-I)Document11 pagesTeoria de Las Placas Tectonicas (2013-I)Deyvi Montañez CadilloNo ratings yet
- Yacimientos y MineralesDocument21 pagesYacimientos y MineralesCristian QuilicheNo ratings yet
- Metodos de Estudio de Los Yacimientos-ADocument23 pagesMetodos de Estudio de Los Yacimientos-ADeyvi Montañez CadilloNo ratings yet
- Yaciminetos Minerales PDFDocument12 pagesYaciminetos Minerales PDFRo SuarezNo ratings yet
- Info de Salida de Campo MontereyDocument12 pagesInfo de Salida de Campo MontereyDeyvi Montañez CadilloNo ratings yet
- BibliografíaDocument2 pagesBibliografíaDeyvi Montañez CadilloNo ratings yet
- Capitulo IVDocument6 pagesCapitulo IVDeyvi Montañez CadilloNo ratings yet
- Teoria de WegenerDocument19 pagesTeoria de WegenerMaría Luz AvilaNo ratings yet
- PsicrómetroDocument6 pagesPsicrómetroDeyvi Montañez CadilloNo ratings yet
- Geologia GeneralDocument13 pagesGeologia GeneralDeyvi Montañez CadilloNo ratings yet
- Deriva Continental Parte 2Document4 pagesDeriva Continental Parte 2Deyvi Montañez CadilloNo ratings yet
- CAMIONESDocument64 pagesCAMIONESDeyvi Montañez CadilloNo ratings yet
- Mecanica de RocasDocument1 pageMecanica de RocasDeyvi Montañez CadilloNo ratings yet
- Análisis de SuelosDocument32 pagesAnálisis de SuelosDeyvi Montañez CadilloNo ratings yet
- Solo SilicosisDocument14 pagesSolo SilicosisDeyvi Montañez CadilloNo ratings yet
- Brechas HidrotermalesDocument9 pagesBrechas Hidrotermalesedizor_66220100% (1)
- Ventilacion UltimoDocument12 pagesVentilacion UltimoDeyvi Montañez CadilloNo ratings yet
- Trabajo de Ventilacion de MinasDocument14 pagesTrabajo de Ventilacion de MinasDeyvi Montañez CadilloNo ratings yet
- Portafolio II UnidadDocument10 pagesPortafolio II UnidadDeyvi Montañez CadilloNo ratings yet
- Mecanica de RocasDocument1 pageMecanica de RocasDeyvi Montañez CadilloNo ratings yet
- Monografía de VentilaciónDocument22 pagesMonografía de VentilaciónDeyvi Montañez CadilloNo ratings yet
- Esfuerzo UniaxialDocument2 pagesEsfuerzo UniaxialDeyvi Montañez CadilloNo ratings yet
- Minado ProfundoDocument32 pagesMinado ProfundoAlfredo Fabian ToledoNo ratings yet
- Proyecto de Nevado de HuandoyDocument6 pagesProyecto de Nevado de HuandoyDeyvi Montañez CadilloNo ratings yet
- INTROCUCCIONDocument1 pageINTROCUCCIONDeyvi Montañez CadilloNo ratings yet
- Promoción del Bien Común mediante ayuda solidariaDocument4 pagesPromoción del Bien Común mediante ayuda solidariaDeyvi Montañez CadilloNo ratings yet
- Clase 5 PROPIEDADES DE LOS MATERIALES PETREOSDocument8 pagesClase 5 PROPIEDADES DE LOS MATERIALES PETREOSAarón Harold CollasNo ratings yet
- El Arma InvencibleDocument2 pagesEl Arma Invenciblealexa sandovalNo ratings yet
- Resumen de Escándalo en BohemiaDocument3 pagesResumen de Escándalo en BohemiaJocelyn Amanda Sepulveda MuñozNo ratings yet
- Magdalena AbakanowiczDocument124 pagesMagdalena AbakanowiczNatália RezendeNo ratings yet
- Tradiciones Del Estado MéridaDocument2 pagesTradiciones Del Estado MéridaMelody ArteagaNo ratings yet
- Guia Lengua IndigenaDocument3 pagesGuia Lengua IndigenaJESSICA AGUAYO100% (2)
- JoJo ReseñaDocument7 pagesJoJo ReseñaMisael Santiago ValdiviesoNo ratings yet
- Composición de 150 Palabras para El ViernesDocument3 pagesComposición de 150 Palabras para El ViernesNegrito MatatanNo ratings yet
- Plan Diario de Clases Sandra SuárezDocument21 pagesPlan Diario de Clases Sandra SuárezYoleima Victoria MolinaNo ratings yet
- Comparacion Entre Apple y MicrosoftDocument7 pagesComparacion Entre Apple y MicrosoftSebastian ArcilaNo ratings yet
- Maquina Sur AntologiaDocument996 pagesMaquina Sur AntologiaAldo Luis Novelli100% (1)
- Especificaciones Tecnicas Todo ConstruccionDocument842 pagesEspecificaciones Tecnicas Todo ConstruccionFREDDYNo ratings yet
- Actividad 3Document6 pagesActividad 3Stanley RodríguezNo ratings yet
- El MokelembembeDocument5 pagesEl MokelembembeRafael castroNo ratings yet
- El Existencialismo Es Un HumanismoDocument19 pagesEl Existencialismo Es Un HumanismoGutierrez Sebas100% (2)
- La Musica en El Siglo XXDocument26 pagesLa Musica en El Siglo XXHARUOrhNo ratings yet
- PastelDocument13 pagesPastelGuillermo BarrozoNo ratings yet
- Los 7 Contrastes - Johannes IttenDocument35 pagesLos 7 Contrastes - Johannes IttenCarlos César GianaNo ratings yet
- Música de IquitosDocument4 pagesMúsica de IquitosThomCooler100% (1)
- Acción de Gracias en La TribulaciónDocument5 pagesAcción de Gracias en La TribulaciónGerizim11No ratings yet
- Programa de Desarrollo Socioafectivo para Alumnos Con Problemas de ConductaDocument33 pagesPrograma de Desarrollo Socioafectivo para Alumnos Con Problemas de ConductaAntonieta NunesNo ratings yet
- Inferir El Significado de Palabras A Partir Del ContextoDocument13 pagesInferir El Significado de Palabras A Partir Del ContextoAna Victoria Fonseca SotoNo ratings yet
- Entramado Ligero de MaderaDocument3 pagesEntramado Ligero de MaderaMagnolia TucNo ratings yet
- Guía para lograr terminaciones perfectas con VolcanDocument18 pagesGuía para lograr terminaciones perfectas con VolcanDannyInostrozaNo ratings yet
- Examen SATV: Revisión 10 preguntasDocument3 pagesExamen SATV: Revisión 10 preguntasJairo Camacho BriceñoNo ratings yet
- Freud El Poeta y Los Suenos DiurnosDocument6 pagesFreud El Poeta y Los Suenos DiurnosHeraldo Glez0% (1)
- Log. Matemat. Iii BimDocument43 pagesLog. Matemat. Iii BimNancy Alvines TavaraNo ratings yet
- GRAMATICADocument22 pagesGRAMATICAGrace RB50% (2)
- Coliqueo PDFDocument8 pagesColiqueo PDFWillie BatterollaNo ratings yet
- Extractos de GuiónDocument7 pagesExtractos de GuiónDaniel GarciaNo ratings yet
- HP Lo Que El Viento Se LlevoDocument7 pagesHP Lo Que El Viento Se LlevomarisalledoNo ratings yet