Professional Documents
Culture Documents
Electrodeposito de Cobre de Alta Pureza - Ingenieria Electrica, Materiales, Etc
Uploaded by
Fernando Eloy Huanca ParquiOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Electrodeposito de Cobre de Alta Pureza - Ingenieria Electrica, Materiales, Etc
Uploaded by
Fernando Eloy Huanca ParquiCopyright:
Available Formats
1
2. TTULO: ELECTRODEPSITO DE COBRE DE ALTA PUREZA1
3. RESUMEN
El presente trabajo de investigacin experimental apoya a la 2 Unidad Industria
minero metalrgica, del programa de estudio de la asignatura de Qumica III.
Cuando un metal se encuentra en contacto con sus propios iones por ejemplo: dos
placas de Cu0 (electrodos nodo y ctodo) introducidos en una disolucin acuosa
de CuSO4 0.05 M ligeramente cida p. ej.)2 Una de las placas se rodear de una
pelcula llamada (doble capa de Helmholtz) 3 de iones orientados (contra iones) y
cuyo espesor es de una micra (10-4 cm), aproximadamente. Este fenmeno est
relacionado por: a) El establecimiento de un equilibrio de xido-reduccin, y por b)
El surgimiento de un potencial elctrico en los electrodos (nodo y ctodo), hacia
formar los sistemas (Mo/M+2) y (M+2/Mo), metal-ion y ion-metal. Por ejemplo la
oxidacin se lleva a cabo en la interface de la placa, metal-disolucin (Mo/M+2),
que est determinada por la relacin entre la tendencia del metal (Mo) a
disolverse, para pasar a la forma inica (M+2), y la reduccin se presenta con la
tendencia de los iones de la disolucin de (M+2) a la forma (M0), por lo tanto habr
un equilibrio de iones entre las placas metlicas con la medio de la disolucin Cu
SO4 0.05 M, entonces: Oxidacin; M0 - 2 e-
M+2
Reduccin; M+2 + 2 e-
Mo
Ahora bien, en este sentido el presente trabajo de investigacin experimental
intitulado: Electrodepsito de cobre de alta pureza, muestra este fenmeno
electroqumico de obtencin de metales de alta pureza, barato y sostenible, as
como didctico para propiciar la comprensin del concepto de reaccin qumica
por xido-reduccin. Esto significa que se mont una celda electroqumica (pila),
con un electrodo negativo (nodo interno) conectado al polo (-) de la fuente de
poder, y un electrodo positivo (ctodo interno) conectado al polo (+) de la fuente.
Es importante aclarar que se obtuvo un electrodepsito de Cu de alta pureza en el
ctodo de 0.08 g.
Actividad diseada por la profesora: Sols Snchez Susana.
Villarreal Enrique D. Fuentes electroqumicas de corriente; Teora y Prctica. Editorial Limusa-Wiley, S. A. Mxico. 1990.
Cap. 1 y 2.
3
Shaw, D. Introduction to cooid and surface chemistry. Butlerworths, Londres, 1966.
2
4. INTRODUCCIN
4.1 Marco terico
La electroqumica es la rama de la qumica que estudia la transformacin entre la
energa elctrica y la energa qumica 4. Los procesos electroqumicos son
reacciones redox (oxidacin- reduccin), en donde la energa liberada por una
reaccin qumica espontnea se transforma en electricidad, o bien la electricidad
se utiliza para inducir una reaccin qumica.
Las aplicaciones prcticas de la electroqumica son variadas, desde las bateras y
las clulas de combustible como fuente de energa elctrica, hasta la obtencin de
productos qumicos, el refinamiento de metales y los mtodos para controlar la
corrosin5. Estos usos se dividen en dos, los industriales y los aplicados a la vida
cotidiana.
Dentro de la industria de los metales, se podra mencionar la refinacin
electroltica, esto quiere decir que se lleva a cabo la electrlisis de soluciones
acuosas, produciendo como resultado metales de alta pureza. Se utiliza para la
purificacin completa de la mayora de los metales no ferrosos. La refinacin con
nodos solubles implica la disolucin del nodo de los metales a ser purificada y la
deposicin de los metales puros en el ctodo, en este proceso, los electrones del
circuito externo son capturados por iones del metal principal6. Por ejemplo la
electrolisis del Cu. En la que el cobre se deposita en el ctodo, los metales nobles
no se disuelven sino que se depositan en el fondo de la celda electroltica como
una suspensin, y metales con potenciales de electrodo negativas se acumulan en
el electrolito, que se limpia peridicamente.
As como algunos mtodos para
controlar la corrosin, utilizados en la industria para evitar prdidas. Por ejemplo el
Chang, Raymond. Qumica. (Dcima edicin). Editorial McGraw Hill. China.2010 p.838
Petrucci, Ralph H.; Harwood, William S., y Herring, F. Geoffrey. Qumica general. (Octava edicin). Pearson Educacin,
S.A., Madrid, 2003.p.p 283-284
6
Internet 1 www.itescam.edu.mx/principal/sylabus/fpdb/recursos/r90833.DOCX
5
uso de aleaciones que forman recubrimiento de xidos para proteger e impedir la
corrosin de los metales7.
Es un hecho que en la vida cotidiana se depende en gran medida de la obtencin
de energa elctrica a partir de reacciones qumicas. Un ejemplo de la aplicacin
en la vida cotidiana son las celdas electroqumicas, llamadas pilas o bateras
(su nombre depende de la cantidad de celdas que este contenga). En cuanto a su
uso es bastante variado, va desde el funcionamiento de un reloj, pasando por
cualquier aparato electrnico (celulares, computadoras, radios, etc.) hasta la
batera de un automvil, necesaria para convertir energa qumica en energa
cintica (energa del movimiento.
Adems de las ms importantes aplicaciones tericas como, el estudio de
relaciones entre qumica y electricidad, el cual nos permite profundizar en las
reacciones en las que se transfieren electrones, las reacciones de oxidacin y
reduccin6.
En el estudio de la electroqumica8 se denomina electrodo a una pieza de metal,
M. Un electrodo sumergido en una disolucin que contiene iones del mismo metal
Mn+, se denomina semiclula. Un electrodo como trmino se utiliza para el
conjunto completo de una semiclula. Entre los tomos metlicos del electrodo y
los iones metlicos en disolucin pueden darse dos tipos de interacciones:
1. Un ion metlico Mn+ de la disolucin puede chocar con el electrodo, tomar
de l n electrones y convertirse en un tomo metlico M. El ion se reduce.
2. Un tomo metlico M de la superficie puede ceder n electrones al electrodo
e incorporarse a la disolucin como un ion Mn+. El tomo metlico se oxida.
El equilibro entre el metal y la disolucin se puede representar como:
S. Zumdahl Steven, Fundamentos de Qumica, 1ra Edicin, Editorial McGraw-Hill Mxico, 1992.
p.589
8
Petrucci, Ralph H.; Harwood, William S., y Herring, F. Geoffrey. Qumica general. (Octava edicin). Pearson Educacin,
S.A., Madrid, 2003. Cap. 21
M0(s)n
Oxidacin
Mn+ (aq) + ne-
Reduccin
Los cambios que se producen en el electrodo o la disolucin como consecuencia
de este equilibrio son demasiado pequeos para poder ser medidos. Los
electrodos se clasifican segn tenga lugar en ellos la oxidacin o la reduccin, si
tiene lugar la oxidacin el electrodo se denomina nodo y si tiene lugar la
reduccin, ctodo. Los aniones emigran haca el nodo y los cationes haca el
ctodo.
Los dos electrodos deben de estar conectados a una fuente de poder y deben de
estar sumergidos en una disolucin acuosa, en este caso CuSO 4 0.05 M con 4
gotas de H2SO4. El electrodo conectado al lado negativo de la fuente se denomina
ctodo y es aquel por el cual entran los electrones a la solucin procedentes de la
fuente, por ejemplo, una fuente de poder naranja. Al mismo tiempo, el electrodo
conectado al lado positivo de la batera se denomina nodo, por el cual salen los
electrones de la solucin y regresan a la batera 9. A este sistema se le denomina
clula electroqumica o celda electroqumica. Una celda electroqumica es un
dispositivo experimental por el cual se puede generar electricidad mediante una
reaccin qumica (celda Galvnica). O por el contrario, se produce una reaccin
qumica al suministrar una energa elctrica al sistema (celda Electroltica). Una
celda galvnica es aquella que permite obtener energa a partir de un proceso
qumico, dicho proceso se realiza de manera espontnea, este tipo de celdas son
las llamadas pilas voltaicas o bateras. Por el contrario las celdas electrolticas no
se obtiene energa, sino que en ellas se aplica energa externa para poder llevar a
cabo la reaccin qumica.
Se debe de entender por electrodo como un sistema metal-ion en solucin.
En este caso se supone que existe una reduccin M+2 + 2 e- Mo se entiende
que este fenmeno es termodinmicamente reversible, como existe una reduccin
Internet 2 http://galeon.hispavista.com/melaniocoronado/ELECTROQUIMICA.pdf
se van a manifestar dos fenmenos; un flujo de iones de la solucin a la interfase
y por consecuencia el trabajo preciso, tambin, un flujo de carga elctrica
asociada a los iones en flujo, y as hay un trabajo elctrico. Ambos trabajos son
dos aspectos del mismo fenmeno10.
Cuando la solucin est diluida, como es en este caso, su comportamiento es
parecido al de los gases.
Para que se pueda realizar el recubrimiento de Cu de alta pureza, aparte de que
se necesita la intervencin de una fuente de poder, tambin se requiere de la
intervencin de las reacciones xido-reduccin, y esto se presenta en el nodo
ya que fue el agente reductor (donador de electrones) y el ctodo fue el agente
oxidante (aceptador de electrones).
Semireacciones:
Ctodo Cu+2 +2e-
Cu0 Red
nodo Cu0 -2e-
Cu+2 Ox
Por lo tanto, se genera un paso de electrones por medio de la disolucin acuosa y
por consecuencia el flujo de iones genera que se complete el circuito.
Y se genere una reaccin redox provocada por la energa elctrica de las cargas
que lo atraviesan11.
10
11
Villarreal Enrique D. Fuentes electroqumicas de corriente; Teora y Prctica. Editorial Limusa-Wiley, S. A. Mxico. 1990.
Cap. 1 y 2.
S. Zumdahl Steven, Fundamentos de Qumica, 1ra Edicin, Editorial McGraw-Hill Mxico,1992, Cap. 21
El potencial estndar de electrodo12 E, mide la tendencia que tiene un
electrodo a generar un proceso de reduccin. Para determinar el valor de E de un
electrodo estndar de cualquier semireaccin, se le compara con el electrodo
estndar de hidrgeno (EEH); el cual implica un equilibrio entre iones H3O+ ,de
una disolucin y molculas de H2 en estado gaseoso a 1 bar de presin, equilibrio
establecido sobre la superficie de un metal inerte como el Cu.
La diferencia en el potencial elctrico se mide en unidades llamadas voltios. El
voltaje que produce un generador o una batera puede considerarse como una
presin elctrica.13 El voltaje de una clula tambin se denomina fuerza
electromotriz (fem) o potencial de clula y se representa como Ecel14.
El potencial estndar de una clula, Ecel, es la diferencia de potencial o voltaje
de una clula por dos electrodos estndar. La diferencia se toma siempre del
siguiente modo:
Ecel= E (derecha) E (izquierda)
Ecel= E (ctodo) - E (nodo)
(reduccin) (oxidacin)
En este caso sera:
Reduccin
(ctodo) Cu+2 +2e-
Cuo
EoCu+2, Cuo = + 0.337 volts
Oxidacin
(nodo) Cuo -2 e-
Cu+2 Eo Cuo, Cu+2 = - 0.337 volts
Ecel= ECu+2/Cu0 ECu0/Cu+2
Ecel= +0.337 (-0.337)
Ecel= +0.674 v
12
Petrucci, Ralph H.; Harwood, William S., y Herring, F. Geoffrey. Qumica general. (Octava edicin). Pearson Educacin,
S.A., Madrid, 2003. Cap. 21
13
Price, Jack; Smoot, Robert C.; Smith, Richard G.Qumica: Un curso moderno. Publicado por: Merril Publishing Company.
Estados Unidos de Amrica. 1988. p.529
14
Petrucci, Ralph H.; Harwood, William S., y Herring, F. Geoffrey. Qumica general. (Octava edicin). Pearson Educacin,
S.A., Madrid, 2003. Cap. 21
Consecuencias de la minera al ambiente
La minera metlica resulta notablemente ms impactante sobre unidad
econmica en el entorno natural donde se desarrolla:
Los gases emitidos que colaboran en el efecto invernadero son ms
importantes en la metlica, debido fundamentalmente a un movimiento de
tierras y al gran consumo elctrico.
La acidificacin de la atmsfera; posee como en el primer caso, consumo
de electricidad que se lleva a cabo en la planta, en los procesos de
molienda con el elevado desmonte para obtener una tonelada de mineral
til, que podra obtener un elevado precio, pero eso no compensa el
esfuerzo ambiental producido. Tambin se cuenta con la agresividad de los
residuos de planta y mina como fruto de los sulfuros acompaantes de las
especies metlicas aprovechadas tales como: generacin de aguas acidas
y liberacin de metales pesados.
La minera subterrnea tambin genera considerables impactos, ya que en
ella aumenta la selectividad en la extraccin, y por lo general tambin se ve
acompaada de una inversin en el tratamiento de estas extracciones, pues
se dirige a minerales que necesitan verdaderos procesos de concentracin,
flotacin, sobre todo.
La produccin de polvo es muy notable en la minera. Sin embargo las
medidas para controlarla son muy eficaces.
El estudio de los componentes del proceso minero metalrgico con el
suficiente detalle puede conducir a la eleccin de sistemas menos
contaminantes y rutas ms eficientes en los procesos, y que con su relacin
con el rendimiento energtico podra significar incrementos en los valores
econmicos15.
15
Obis, Joaqun, y otros autores, La industria extractiva no energtica y el medio ambiente en el marco del desarrollo
sustentable, Madrid, Instituto Geolgico y Minero de Espaa, 2005, p. 336.
4.2 Objetivos de la investigacin
a) Obtener en el laboratorio un electrodepsito de cobre de alta pureza como
proceso industrial.
b) Comprender las reacciones qumicas de oxidacin y reduccin a partir de la
obtencin del cobre de alta pureza.
c) Comprender el funcionamiento de una celda electroqumica y los conceptos
como: de ctodo, nodo, reduccin, oxidacin, ganancia y prdida de
electrones, potencial de la celda, potencial electrodo o elctrico.
d) Valorar con esta actividad el ambiente y sus consecuencias.
4.3 Problema
Cmo se obtienen los metales?
Los metales tienen una gran importancia para nuestra sociedad desarrollada de
hoy en da. Sin los metales y los recursos minerales seguramente no podramos
tener muchos de los lujos de los que disponemos, puesto que ya todo muestro
entorno existen objetos de uso cotidiano, que son producidos gracias a la
extraccin de los metales como lo son:
Celulares, computadoras, televisiones, automviles e incluso construcciones, en el
caso de la salud sirven para los utensilios quirrgicos o en los aparatos que
utilizan para los tratamientos.
Pocos de los metales que se extraen, se encuentran de forma nativa en la
naturaleza; estos pueden encontrarse qumicamente combinados formando
diversos compuestos minerales, tales como xidos, carbonatos, sulfuros, etc.
Estos compuestos se hallan en los yacimientos formando la mena, que es toda
materia de origen natural de la cual se puede extraer uno o ms metales.
10
Las menas, generalmente contienen cantidades variables de materias extraas,
piedras o tierras, que se denominan gangas. La combinacin de la mena y la
ganga es lo que constituye el mineral.
Ahora bien, en este sentido el una vez obtenida la mena se somete a un proceso y
posteriormente a un proceso qumico de obtencin del metal en estado puro como
en el caso particular del presente trabajo de investigacin experimental intitulado:
Electrodepsito de cobre de alta pureza, que muestra este fenmeno
electroqumico de obtencin de metales de alta pureza, barato y sostenible.
4.4 Hiptesis
De acuerdo a la investigacin terica creemos:
Se llevar a cabo la reduccin en el electrodo (ctodo) con ganancia de
electrones y un electrodepsito de cobre de alta pureza.
Se llevar la oxidacin en el electrodo (nodo) con prdida de electrones y un
desgaste de la placa.
5. DESARROLLO
5.1 Material y sustancias
Material
Sustancias
1 fuente de poder naranja.
2 caimanes.
1 multmetro.
1 balanza granataria.
1 esptula.
1 piseta con agua destilada.
1 vaso de precipitados de 250 mL.
1 matraz aforado de 100 mL.
2 placas de cobre del mismo tamao y grosor.
-Disolucin de CuSO4 a una
concentracin (0.05 M).
-cido sulfrico concentrado.
-Agua destilada
11
5.2 Metodologa
1. Limpiar muy bien, pesar y medir, las placas metlicas de cobre o electrodos
(ctodo y nodo).
2. En seguida preparar 100 ml de una disolucin 0.05 M de CuSO4 con 4 gotas
de H2SO4 concentrado:
Clculos:
Molaridad=
PM de CuSO4 = 63.54 gr + 32.064 gr + 4(15.999 gr)= 159.6 gr
de CuSO4
De acuerdo a los clculos anteriores, luego entonces, ha que pesar 0. 79805 g de
CuSO4 y vaciarlos en un matraz aforado de 100 mL, luego agregarle 4 gotas de
H2SO4 y finalmente aforar a 100 mL con agua destilada.
12
3. Preparacin de la celda electroqumica:
Instalar la celda electroqumica de acuerdo a la imagen siguiente:
4. Encender la fuente de poder y calibrar el multmetro a un voltaje de de 0.674
volts.
5. Esperar 10 minutos para apagar la fuente de poder y observar el
electrodepsito de cobre de alta pureza.
13
6. Secar el ctodo en una estufa a 30oC por un espacio de 2 hrs, dejar enfriar y
posteriormente pesarlo y registrar los resultados obtenidos del electrodepsito
de Cu. Nota: se recomienda no tocar el ctodo del electrodepsito
directamente con las manos, ya que puede incrementar el peso del depsito de
Cu.
En la siguiente imagen se observan los resultados del electrodepsito de Cu de
alta pureza en el (ctodo) y el desgaste muy leve del (nodo).
7. Finalmente barnizar el ctodo para proteger el electrorecubrimiento de Cu de
alta pureza.
14
6. RESULTADOS
A) Cmo se prepararon los 100 mL de la disolucin acuosa 0.05 M de CuSO4
para la celda electroqumica?
Los clculos qumicos fueron:
Molaridad=
PM de CuSO4 = 63.54 gr + 32.064 gr + 4(15.999 gr)= 159.6 gr
de CuSO4
De acuerdo al resultado anterior, se pesaron 0.79805 g. de CuSO4 y ya en el
matraz se afor a 100 mL con agua destilada, esta disolucin acuosa se vaci en
un vaso de precipitados de 250 mL.
Cabe sealar que con dicha disolucin de CuSO4 0.05 M se prepar la pila o
celda electroltica como un sistema espontneo de xido-reduccin, en la cual se
introdujeron las dos placas metlicas de Cu como electrodos (nodo y ctodo) y
se hizo pasar una corriente elctrica de 0.674 v. Esto signific el acoplamiento de
dos sistemas metal-ion e ion-metal, dando como resultado un electrodepsito
(recubrimiento) de cobre de alta pureza en un electrodo (ctodo). Como
consecuencia, entre los electrodos (nodo y ctodo) se gener una diferencia de
potencial a la que se le llama fuerza electromotriz (Ec). En base a la estructura de
la celda o pila, la fuerza electromotriz16 de la misma estuvo dada por la expresin
general siguiente:
Ec =Eored Eoox
Ec = EoCu+2, Cuo - Eo Cuo, Cu+2
De donde; Eo= potencial estndar de los pares xido-reduccin a 25oC y para
disoluciones acuosas en medio cido.
16
Villarreal Enrique D. Fuentes electroqumicas de corriente; Teora y Prctica. Editorial LimusaWiley, S. A. Mxico. 1990. Cap. 1 y 2.
15
Reaccin qumica catdica y andica:
Reaccin completa CuSO4 + Cuo
Cuo + CuSO4
Reduccin
(ctodo) Cu+2 +2e-
Cuo
EoCu+2, Cuo = + 0.337 volts
Oxidacin
(nodo) Cuo -2 e-
Cu+2 Eo Cuo, Cu+2 = - 0.337 volts
Ec= Eored Eoox
Ec= 0.337- (-0.337)
Ec= 0.337 + 0.337= 0.674 volts de la celda
Con este voltaje de 0.674 V de la celda, en el laboratorio se llev a cabo el
recubrimiento electroltico de Cu de alta pureza en el ctodo, mismo que duro 10
minutos. En este proceso de xido-reduccin se observ tambin que en el nodo
se presenciaba un desgaste muy leve.
Tabla de resultados:
Electrodos
Volts
Tiempo de Peso inicial
exposicin
Ctodo de Cu
0.674 v. 10 min
nodo de Cu
0.674 v. 10 min
Peso
final
Recubrimiento
de Cuo en el
ctodo.
130.82 g.
130.90 g.
0.08 g.
130.85 g.
129.90 g.
-------
Cabe sealar que al retirar los electrodos de la celda electroqumica claramente se
observ que en el ctodo haba un recubrimiento de cobre de alta pureza y que el
nodo estaba levemente desgastado:
En esta imagen se distingue el electrodepsito de Cu
de alta pureza en el (ctodo), obsrvese la diferencia de
color entre las placas.
16
7. ANLISIS DE RESULTADOS
Pudimos darnos cuenta que un electrodepsito de cobre de alta pureza es muy
sencillo de reproducir, sin embargo, lo difcil fue hacer diferentes pruebas a
diferentes concentracin de disolucin CuSO4, as como de encontrar el tiempo de
exposicin adecuado del electrodepsito sobre las placas. Finalmente se encontr
la concentracin adecuada y tiempo de exposicin necesario para obtener un
electrodepsito de calidad.
Tambin se probaron diferentes tamaos y grosores de las placas metlicas o
electrodos de Cu, ya que es de suma importancia la fuerza electromotriz que se
genera en los electrodos dentro de una celda electroqumica, pues as como fue
importante comprender el proceso de oxidacin y reduccin, tambin fue muy
importantes comprender las siguientes cuestiones para el logro de los objetivos
del trabajo de investigacin experimental:
a) La naturaleza de los electrodos (placas metlicas),
b) Los clculos qumicos cuantitativos para la concentracin de las
disoluciones,
c) Las condiciones externas de temperatura,
d) El tiempo de exposicin de las placas dentro de la celda y,
e) El paso de corriente a un voltaje adecuado de la celda o fuerza
electromotriz Ec.
17
8. CONCLUSIONES
La reaccin que se presenci dentro de nuestro electrodepsito fue de tipo oxidoreduccin (Redox). El nodo del electrodeposito fue nuestro donador de
electrones, tambin llamado agente reductor (aquel que se oxid). Nuestro ctodo
fue el receptor de electrones, tambin llamado agente oxidante (aquel que se
redujo). De este modo pudimos experimentar que el proceso de xido-reduccin
es un conjunto de dos reacciones simultneas de oxidacin y reduccin.
En este sentido se logr comprender en el laboratorio el funcionamiento de las
celdas electroqumicas como un proceso industrial de obtencin a gran escala de
metales puros. Al mismo tiempo se aprendi a organizar informacin tcnica
indispensable para adquirir el conocimiento fundamental y bases de las reacciones
qumicas por xido-reduccin. Por otra parte, con el desarrollo del trabajo se logr
satisfacer una necesidad en el dominio de habilidades y destrezas experimentales
de laboratorio, as como conocer las dificultades que se tienen para realizar la
investigacin terica, pues existe un mar de informacin el cual se tuvo que
seleccionar y resumir para el estudio de este tema.
El trabajo experimental nos llev a comprender como es la investigacin en las
ciencias, que se basa tanto en investigacin documental y en resultados, por
ejemplo, aprendimos que para comprender la qumica necesitamos primero
comprender los principios en los que se basa la electroqumica y su
funcionamiento en el dispositivo o celda electroqumica utilizada.
Si algn mrito hay en este trabajo, fue el haber puesto nuestra confianza y
esfuerzo para adquirir la experiencia y por consecuencia cumplir con los objetivos
propuestos al inici del proyecto.
18
9. FUENTES DE INFORMACIN
Chang, Raymond, Qumica, McGraw-Hill, China, (dcima edicin), 2010.
Obis, Joaqun, y otros autores, La industria extractiva no energtica y el medio
ambiente en el marco del desarrollo sustentable, Madrid, Instituto Geolgico y
Minero de Espaa, 2005.
Petrucci, Ralph H.; Harwood, William S., y Herring, F. Geoffrey. Qumica
general. (Octava edicin). Pearson Educacin, S.A., Madrid, 2003.
Price, Jack; Smoot, Robert C.; Smith, Richard G.Qumica : Un curso moderno.
Publicado por: Merril Publishing Company. Estados Unidos de Amrica. 1988.
S. Zumdahl Steven, Fundamentos de Qumica, 1ra Edicin, Editorial McGrawHill Mxico, 1992.
Shaw, D. Introduction to cooid and surface chemistry. Butlerworths, Londres,
1966.
Villarreal Domnguez Enrique, Bello de Villarreal Silvia, Fuentes
Electroqumicas de Corrientes,1ra Edicin, Editorial Limusa-Wilney, 1971.
Pginas electrnicas:
Internet 1http://www.itescam.edu.mx/principal/sylabus/fpdb/recursos/r90833.DOCX
ACCESO: 22 de febrero del 2014, 20:09 horas.
Internet 2 http://galeon.hispavista.com/melaniocoronado/ELECTROQUIMICA.pdf
ACCESO: 20 de febrero del 2014, 17:40 horas.
You might also like
- Utilización de La Semilla de PaltaDocument7 pagesUtilización de La Semilla de PaltaFernando Eloy Huanca ParquiNo ratings yet
- Jaarabe de GomaDocument14 pagesJaarabe de GomaFernando Eloy Huanca ParquiNo ratings yet
- Enzimas OxalatosDocument2 pagesEnzimas OxalatosFernando Eloy Huanca ParquiNo ratings yet
- Antiglutinantes en La Industria Del ChocolateDocument5 pagesAntiglutinantes en La Industria Del ChocolateFernando Eloy Huanca ParquiNo ratings yet
- Marshmallows FormulacionDocument4 pagesMarshmallows FormulacionFernando Eloy Huanca ParquiNo ratings yet
- FODA CacaoDocument3 pagesFODA CacaoFernando Eloy Huanca ParquiNo ratings yet
- Yana CornetaDocument2 pagesYana CornetaFernando Eloy Huanca ParquiNo ratings yet
- Historial MollebayaDocument7 pagesHistorial MollebayaFernando Eloy Huanca ParquiNo ratings yet
- Practica N 4 Ensayo de Determinacion de Acidez en Harinas y Metodo Volumetrico y Determinacion de PH en HarinasDocument7 pagesPractica N 4 Ensayo de Determinacion de Acidez en Harinas y Metodo Volumetrico y Determinacion de PH en HarinasJesus David Sandoval DelgadoNo ratings yet
- Elaboracion de Embutidos Cocidos Queso de ChanchoDocument7 pagesElaboracion de Embutidos Cocidos Queso de ChanchoFernando Eloy Huanca ParquiNo ratings yet
- Windows 7 (PPD) - 01 PDFDocument5 pagesWindows 7 (PPD) - 01 PDFFernando Eloy Huanca ParquiNo ratings yet
- ArtemisiaDocument11 pagesArtemisiaFernando Eloy Huanca ParquiNo ratings yet
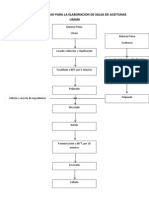
- Diagrama de Flujo para La Elaboracion de Salsa de Aceitunas UmariDocument1 pageDiagrama de Flujo para La Elaboracion de Salsa de Aceitunas UmariFernando Eloy Huanca ParquiNo ratings yet
- Cerradura ElectrónicaDocument24 pagesCerradura ElectrónicaJbhNo ratings yet
- Sistema Puesta A Tierra - Trabajo de Laboratorio - Flores Anselmo Carlos y Suclupe Inoñan LuisDocument29 pagesSistema Puesta A Tierra - Trabajo de Laboratorio - Flores Anselmo Carlos y Suclupe Inoñan LuisCarlosNo ratings yet
- Untitled - 3. Ficha Técnica ANDRIS LUX ECODocument1 pageUntitled - 3. Ficha Técnica ANDRIS LUX ECOalexNo ratings yet
- Medida de Potencia y Factor de PotenciaDocument5 pagesMedida de Potencia y Factor de PotenciaJuan Bances RamosNo ratings yet
- Motor Paso A PasoDocument4 pagesMotor Paso A PasoRoger EduinNo ratings yet
- Lab 3Document3 pagesLab 3Juan camilo Cañas tiradoNo ratings yet
- Formatos ConsolidadosDocument40 pagesFormatos ConsolidadosValentina Sánchez MoreraNo ratings yet
- 13 Causas Comunes Del Fallo Del MotorDocument19 pages13 Causas Comunes Del Fallo Del MotorGeorge QuijijeNo ratings yet
- Informe. Lección 3 CIRCUITOS 2018 FinalDocument3 pagesInforme. Lección 3 CIRCUITOS 2018 Finalangel vivasNo ratings yet
- Trabajo Con Alta, Media y Baja TensiónDocument12 pagesTrabajo Con Alta, Media y Baja TensiónLeidy BermúdezNo ratings yet
- Fe2008 PDFDocument176 pagesFe2008 PDFOscar Sacases PlanasNo ratings yet
- CE83 - Lab06 - Tarjeta de ProcedimientoDocument2 pagesCE83 - Lab06 - Tarjeta de ProcedimientoMichael MendozaNo ratings yet
- Corrección Del Factor de Potencia PDFDocument12 pagesCorrección Del Factor de Potencia PDFDieguito Sánchez0% (1)
- W-13 Pro NorDocument1 pageW-13 Pro NorJuan Miguel Heredia CalderonNo ratings yet
- Perdidas VariablesDocument10 pagesPerdidas VariablesMarco Antonio Veranza VazquezNo ratings yet
- Práctica 3. Análisis de Circuitos ResistivosDocument4 pagesPráctica 3. Análisis de Circuitos ResistivosCarlos Andres Aragon FlorezNo ratings yet
- Experimento 8Document15 pagesExperimento 8userpro115No ratings yet
- Cepillo Eléctrico Bosch Gho 40 82 C Manual 238790Document174 pagesCepillo Eléctrico Bosch Gho 40 82 C Manual 238790Daniel Fernández SánchezNo ratings yet
- Informe Practica 3 Logica SecuencialDocument3 pagesInforme Practica 3 Logica SecuencialJulian David Criollo AguirreNo ratings yet
- Taller 2 - Circuitos 1 - RespuestasDocument4 pagesTaller 2 - Circuitos 1 - RespuestasDiego Alejandro Becerra MartinezNo ratings yet
- Programación Didáctica Subestaciones EléctricasDocument19 pagesProgramación Didáctica Subestaciones EléctricasAntonio Zorrilla JiménezNo ratings yet
- Lab02 - Medición Tensión y Resistencia GRUPO 8Document17 pagesLab02 - Medición Tensión y Resistencia GRUPO 8Javier Marcial Mamani AmpueroNo ratings yet
- Vazquez Cuamatla Fernando: Rmu: 56643 05-03-20 XAXX-010101 693 CFEDocument2 pagesVazquez Cuamatla Fernando: Rmu: 56643 05-03-20 XAXX-010101 693 CFEVazquez FernandoNo ratings yet
- Ejercicios de MagnetismoDocument4 pagesEjercicios de MagnetismoJeff HuckleberryNo ratings yet
- Iec 60502 2 EspañolDocument13 pagesIec 60502 2 Españolmartin100% (4)
- Tecle y PrensaDocument7 pagesTecle y PrensaLennert Hubert Huaman Palomino100% (1)
- Manual Central Doble Bbs MotionDocument4 pagesManual Central Doble Bbs MotionCristian OsmikNo ratings yet
- Tr1 Trabajo FinalDocument7 pagesTr1 Trabajo FinalBelhiz Sare67% (3)
- Paper Fisicoquimica 2Document9 pagesPaper Fisicoquimica 2Alonso Dominguez MendozaNo ratings yet
- Problemas de Conmutación en Maquinas RealessubrDocument2 pagesProblemas de Conmutación en Maquinas RealessubrIvan8823100% (2)