Professional Documents
Culture Documents
PRACTICA 9 Proteasa 2014
Uploaded by
Ricardo PinillosCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
PRACTICA 9 Proteasa 2014
Uploaded by
Ricardo PinillosCopyright:
Available Formats
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
E.A. P. INGENIERIA AGROINDUSTRIAL
ASIGNATURA: BIOQUIMICA
SEMESTRE 2014-I
PRACTICA 9
ESTUDIO DE LA ACTIVIDAD ENZIMATICA DE UNA PROTEASA ACIDA
I.
OBJETIVOS
Evaluar la actividad de la pepsina y evaluar el hidrolizado de protenas.
II.
INTRODUCCIN TEORICA
Las proteasas cidas se denominan as porque actan a bajo pH. La pepsina fue la
primera al que se dio la denominacin de proteasas por Schwann 1825, otros miembros son la
quimosina (renina) que se usa en la fabricacin de queso. La catepsina (que est implicada en
el ablandamiento post morten de la carne)
PEPSINA
La pepsina est constituida por una cadena poli peptdica sencilla que contiene 327 restos de
aminocidos con un PM de 34,644 daltons. La Ser-68 est fosforilada pero este fosfato se
puede eliminar sin que se alteren significativamente las propiedades catalticas del enzima. Al
igual que en otras proteasas, el sitio activo es un rea extensa que se puede acomodar como
mnimo cuatro a cinco y quizs hasta siete, restos de aminocidos. El enzima presenta una
preferencia por los aminocidos hidrofbicos en cualquiera de los lados del enlace escindible.
La hidrolisis de las protenas demuestra que tiene especificidad por la Leu, Phe, Trp y Glu en el
sitio S1 y por Trp, Tir, Iso y Phe en el sitio S1.
La pepsina se segrega como un zimgeno precursor, el pepsingeno por las clulas
principales gstricas. El cido gstrico activa el pepsingeno activo segregado, siendo 2 el pH
ptimo.
La pepsina contina actuando en el estmago cido y slo se inactiva tras el paso del quimo al
duodeno, donde se produce la neutralizacin. El cido activa la pepsina.
ENDOPEPTIDASA DIGESTIVAS
3.4.21.n
3.4.23.n
Proteinasas de serina (especialmente las enzimas pancreticas: tripsina y
quimotripsina)
Proteinasas cidas o aspartato proteinasas grupo en el que se sitan la
mayor parte de las enzimas utilizadas para la coagulacin de la leche:
enzimas de origen animal (quimosina 3.4.23.4; pepsina 3.4.23.1)
MECANISMO DE ACCIN
En la pepsina hay dos residuos catalticos activos, el Asp-32 y el Asp-215. Sus
ionizaciones se observan en el perfil de actividad frente al pH (2-3) y que depende de la forma
cida de un grupo de pKa cercano a 4.5 y de la forma bsica de un grupo de pKa de alrededor
de 1.1
Mg.Rosario Calixto Cotos
Las pepsinas contienen fsforo mientras que la quimosina carece de l. Se encuentran de 1 a 3
tomos de fsforo en la pepsina II y de 0 a 2 en la pepsina I, Cuando se examina por
electroforesis a la pepsina II se observa la presencia de 5 a 6 componentes pero tras la
desfosforilacin enzimtica aparece slo uno. La pepsina bovina II es estable a un pH ms
elevado que la pepsina de cerdo.
La actividad proteoltica es a pH 2. Se inhibe a pH superiores a 6.6 por ello no coagula las
leches frescas.
ALGUNAS PROPIEDADES DE LAS ENZIMAS DIGESTIVAS
Quimosina
Pepsina bovina
II(B)
II(A)
pH
ptimo
de 3.4
7.0
<2
actividad proteoltica
sobre la Hb
pH para un 50% de 8.15
7.45
7.85
inactivacin
Peso molecular
34,400
30,000(?) 33,400
Datos de Antonini Ribadeau (1971) (1)
Pepsina
porcina
<2
7
34,500
QUIMOSINA
Es el componente principal de los cuajos. Se secreta en el abomaso (cuajar) bajo una
forma inactiva, la proquimosina. Se transforma en enzima activa por un proceso autocataltico
acelerado por los iones H+ como en el caso del pepsingeno. La activacin es instantnea a pH
2. En el curso de la activacin, de la parte N-terminal de la proenzima se separan pepidos
bsicos.
La quimosina A es ms activa que la quimosina B, de la que slo se distingue por una
sustitucin Asp/Gli en la posicin 290 de su cadena peptdica; la forma B es siempre
predominante. La tercera forma C es un componente menor. La quimopsina es una
holoprotena y no contiene tomos de fsforo (ni de metal, ni de glcidos). El pH ptimo cuando
el sustrato es la casena de vaca, se acerca a 4.
La actividad enzimtica se medir por la desaparicin del substrato (disminucin de la
turbidez en los tubos que contiene albmina), y la lectura se puede realizar entre 420-460 nm.
La hidrolisis de la albmina produce aminocidos libres, pptidos de cadena corta y larga.
Estos productos pueden ser evaluados mediante el reactivo de Biuret el cual puede ser medido
por colorimetra a una long. de onda a 545 nm.
III. PARTE EXPERIMENTAL
III.1. MATERIALES Y REACTIVOS
Gradilla, pipetas de 1, 2 y 5 mL, tubos de ensayo y probetas 50 ml
Bombilla, bao de agua 37C, espectrofotmetro
Agua destilada, ovoalbmina, pepsina, HCl 0.1N, NaOH 0.1N
III.2. PROCEDIMIENTO
EFECTO DE LA CONCENTRACION DE LA ENZIMA
Fundamento: La velocidad de una reaccin enzimtica a concentraciones saturantes
de sustrato, dependen linealmente de la concentracin de la enzima.
Mg.Rosario Calixto Cotos
Preparar la siguiente batera de tubos:
Tubos
ml agua destilada
2.7
2.4
2.1
1.5
0.3
ml HCl 1N
0.3
0.3
0.3
0.3
0.3
ml albmina
Pepsina preincubada por 5 minutos en otro tubo A
1. Preincubar a 37C por 5 min los tubos del 1 al 5, e inmediatamente.
aadir la pepsina preincubada a los tubos del 2 al 5, segn el siguiente esquema:
Tubos
1
2
3
4
5
Pepsina 1%
-----0.3
0.6
1.2
2.4
Incubar a 37C por 7 min. Detener la reaccin colocando los tubos en bao
de agua helada.
Observar la turbidez de los tubos
IV. REPORTE DE RESULTADOS
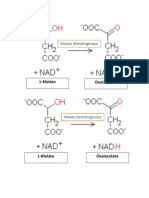
1. Realiza la ecuacin enzimatica que se desarrolla en la reaccin., en los tubos 1,2 y 5
1.
2. ..
3. ..
.
2. Al terminar la reaccin enzimtica, que significa mayor turbidez y menor turbidez
La presencia de turbidez indica: ..
3. Explique si los productos constituyen hidrolizados de protenas.
4. Conclusiones :
V.
VI.
2.
CUESTIONARIO
1. Establezca mediante un cuadro 5 diferencias entre la pepsina y la quimosina.
2. Cul es el mecanismo de accin de la quimosina?
3. Mencione 4 inhibidores alimentarios de la pepsina.
4. La actividad enzimatica se puede expresar por formacin de productos, explique cmo lo
realizara, explique el mtodo.
REFERENCIAS BIBLIOGRAFICAS
1. Alais Charles. Ciencias de la leche. Principios de la Tcnica lechera. Ed. Reverte S.A 2005.
Fenema Qumica de los alimentos Ed.Acribia. 3era edicin, p.374, 2007
3. Robinson David. Bioqumica y valor nutritivo de los alimentos. 2da edicin. Editorial
Acribia 1991. Zaragoza.
Mg.Rosario Calixto Cotos
Mg.Rosario Calixto Cotos
You might also like
- Practica 11 BioquimicaDocument5 pagesPractica 11 BioquimicaCcallo Quispe Edwin JoseNo ratings yet
- Ciencias Naturales 8 PDFDocument41 pagesCiencias Naturales 8 PDFAmabilis Sequera Galindez0% (1)
- Actividad PrácticaDocument2 pagesActividad PrácticaMauro MurrietaNo ratings yet
- BLT m7000 EspañolDocument2 pagesBLT m7000 EspañolDaniel GalindoNo ratings yet
- Determinacion de La Actividad Enzimatica de La Amilasa SalivalDocument13 pagesDeterminacion de La Actividad Enzimatica de La Amilasa SalivalHector Johnny Armas RodriguezNo ratings yet
- Estudios de Caso Medicina 2019 I - Prof. LeyvaDocument8 pagesEstudios de Caso Medicina 2019 I - Prof. LeyvahenryNo ratings yet
- Resumen Introducción A La Química Clínica y EspectrofotometríaDocument5 pagesResumen Introducción A La Química Clínica y EspectrofotometríajeiselllaNo ratings yet
- Ejercicio Integración Metabolismo Anaeróbico y AeróbicoDocument7 pagesEjercicio Integración Metabolismo Anaeróbico y AeróbicoMeylin CastroNo ratings yet
- Practica 9 ACIDO URICO BIOquimica CompletaDocument10 pagesPractica 9 ACIDO URICO BIOquimica CompletaAnthony H-m100% (1)
- Compuestos NitrogenadosDocument14 pagesCompuestos NitrogenadosCaroline TW0% (1)
- PDF Pruebas Gram Fundamento Revelador Control Positivo y Negativo Observaciones - CompressDocument6 pagesPDF Pruebas Gram Fundamento Revelador Control Positivo y Negativo Observaciones - CompressAna Karen Patiño SimbrónNo ratings yet
- Cromatografia en Papel y CFDocument36 pagesCromatografia en Papel y CFByron Alexander PerezNo ratings yet
- Informe 5 Reconocimiento de Vitaminas Helber Rojas, Danny Bautista.Document10 pagesInforme 5 Reconocimiento de Vitaminas Helber Rojas, Danny Bautista.Helber Fernando Rojas BarajasNo ratings yet
- Tema 4. Carotenoides y LicopenoDocument50 pagesTema 4. Carotenoides y LicopenoPedro SanchezNo ratings yet
- Seminario IV AminasDocument22 pagesSeminario IV AminasMonserrat VilaNo ratings yet
- GLUCOGENOGENESISDocument2 pagesGLUCOGENOGENESISMARGARITA MOO CHANNo ratings yet
- Informe Metabolismo de GlucosaDocument12 pagesInforme Metabolismo de GlucosaDaniel Sevilla Nakazaki0% (1)
- Tema 2. ANTIGENOS - ODfffDocument24 pagesTema 2. ANTIGENOS - ODfffwalito2100% (2)
- Biosintesis de Nucleotidos de NovoDocument8 pagesBiosintesis de Nucleotidos de NovoMARIA FERNANDA JAIME CORREANo ratings yet
- P4. Extracción de ARNDocument6 pagesP4. Extracción de ARNPamelaNo ratings yet
- Bromatología - Proteinas (Esquemas)Document7 pagesBromatología - Proteinas (Esquemas)Jhonny LópezNo ratings yet
- Extraccion de Lipidos de Cerebro Brain LDocument4 pagesExtraccion de Lipidos de Cerebro Brain LJosue AlvarezNo ratings yet
- Catabolismo de AminoacidosDocument20 pagesCatabolismo de AminoacidosXimena Véliz DaudNo ratings yet
- Resumen Coenzimas y Vitaminas LehningerDocument4 pagesResumen Coenzimas y Vitaminas LehningerLesly Maribel Rodríguez PernilloNo ratings yet
- La Enzima Malato DeshidrogenasaDocument2 pagesLa Enzima Malato DeshidrogenasaKaren Torres JuárezNo ratings yet
- Sistemas y Aparatos Del Cuerpo HumanoDocument37 pagesSistemas y Aparatos Del Cuerpo HumanoGisela Pino PizáNo ratings yet
- Virus ARN de Importancia ClínicaDocument27 pagesVirus ARN de Importancia ClínicaLauraMartínez100% (2)
- Strectococcus DiapositivaDocument17 pagesStrectococcus DiapositivaMONICA IBARRA CUELLARNo ratings yet
- Tincion de GramDocument4 pagesTincion de GramYirem SanchezNo ratings yet
- v8n1 A02Document24 pagesv8n1 A02Belii HezNo ratings yet
- Inhibidores de La GlucolisisDocument9 pagesInhibidores de La Glucolisisingjuferdima2240100% (1)
- GASTROSEMIODocument18 pagesGASTROSEMIOMaria Segura RivagueroNo ratings yet
- Nava, 2017. Glucosinolatos de MoringaDocument63 pagesNava, 2017. Glucosinolatos de MoringaJUDITHNo ratings yet
- Toxicologia Del ArsenicoDocument3 pagesToxicologia Del ArsenicoNicolas Gabriel Gutierrez MedinaNo ratings yet
- Reporte de Laboratorio #7Document3 pagesReporte de Laboratorio #7Mario Rodolfo Utrera Salazar100% (1)
- Esofago y EstomagoDocument6 pagesEsofago y EstomagoCarlos ValenzuelaNo ratings yet
- INFORME NorfloxacinaDocument14 pagesINFORME NorfloxacinaMafer VerdugaNo ratings yet
- ProteinasDocument6 pagesProteinasNataliaNo ratings yet
- Taller de Lipidos ResueltoDocument5 pagesTaller de Lipidos ResueltoAngelica SuarezNo ratings yet
- Inhibicion de Cadena Transportadora de ElectronesDocument4 pagesInhibicion de Cadena Transportadora de ElectronesAaron Llerena ArroyoNo ratings yet
- Metabolismo y Excreción de Farmacos (Informe)Document9 pagesMetabolismo y Excreción de Farmacos (Informe)FalconHC100% (2)
- 4 - Lipidos IiDocument14 pages4 - Lipidos Iibetincarlos3010No ratings yet
- Enfermedad de Cory Forbes Tipo IIIDocument10 pagesEnfermedad de Cory Forbes Tipo IIIEmmanuel PaniaguaNo ratings yet
- Práctica 7. Digestión de ProteínasDocument5 pagesPráctica 7. Digestión de ProteínasSelvis Rivera CerezoNo ratings yet
- Unid.3.B. Principios de Cromatografia de Gases (CG)Document31 pagesUnid.3.B. Principios de Cromatografia de Gases (CG)Elmer Fernández RamosNo ratings yet
- Amortiguadores o Tampones Biologicos 1Document2 pagesAmortiguadores o Tampones Biologicos 1maria martinezNo ratings yet
- Formacion y Transporte de AmoniacoDocument4 pagesFormacion y Transporte de AmoniacoMariela MaldonadoNo ratings yet
- Metabolismo de Acidos Grasos.Document7 pagesMetabolismo de Acidos Grasos.Mariel AybarNo ratings yet
- Metabolismo de Acidos NucleicosDocument30 pagesMetabolismo de Acidos NucleicosHernàn RV0% (1)
- Compuestos Nitrogenados No ProteicosDocument2 pagesCompuestos Nitrogenados No ProteicosPrinci P Real50% (2)
- Examen de Bioquimica3Document2 pagesExamen de Bioquimica3Jose Eduardo Salazar SandovalNo ratings yet
- Catabolismo LipidosDocument34 pagesCatabolismo LipidosJackeline Villanueva SalinasNo ratings yet
- Vitamina B2 RiboflavinaDocument11 pagesVitamina B2 RiboflavinaArturo PizuornoNo ratings yet
- Carotenoides 2011Document31 pagesCarotenoides 2011Ruben Kapa TiconaNo ratings yet
- Practica 01. Bioseguridad e Instrumentacion en El LaboratorioDocument3 pagesPractica 01. Bioseguridad e Instrumentacion en El LaboratorioChristianNo ratings yet
- EnantiomerosDocument6 pagesEnantiomerosyadhira olivera floresNo ratings yet
- Actividad de Las GrasasDocument4 pagesActividad de Las Grasasclaudia marcela rubio rojasNo ratings yet
- BioquimmicaDocument8 pagesBioquimmicaZENAIDA ALEXANDRA CCAMA CCAHUANANo ratings yet
- Practica 04 Digestion de Las Proteinas e Inhibicion de Las Enzimas Digestivas ProteicasDocument11 pagesPractica 04 Digestion de Las Proteinas e Inhibicion de Las Enzimas Digestivas ProteicasCARLOS ALBERTO PEREZ PEREZNo ratings yet
- Digestion de La AlbuminaDocument8 pagesDigestion de La AlbuminaAlfredo EscobarNo ratings yet
- P2 - BioquimicaDocument46 pagesP2 - BioquimicaJuan CNo ratings yet
- Alfa Aa y Proteínas IND AGRICOLASDocument3 pagesAlfa Aa y Proteínas IND AGRICOLASNAYITNo ratings yet
- Alimentacion Del Coati de Colla AnlilladaDocument105 pagesAlimentacion Del Coati de Colla AnlilladaRicardo PinillosNo ratings yet
- Torres Aguinaga Karla LizetDocument123 pagesTorres Aguinaga Karla LizetRicardo PinillosNo ratings yet
- Simulacion DiDocument4 pagesSimulacion DiRicardo PinillosNo ratings yet
- Formato I Postulacion Emprendimientos Innovadores - Cerveza ArtesanalDocument8 pagesFormato I Postulacion Emprendimientos Innovadores - Cerveza ArtesanalRicardo PinillosNo ratings yet
- Fermentacion de Cacao y CafeDocument49 pagesFermentacion de Cacao y CafeRicardo PinillosNo ratings yet
- 325 Proyectos de Tesis AGODocument11 pages325 Proyectos de Tesis AGORicardo PinillosNo ratings yet
- Precio de Malta y LupuloDocument3 pagesPrecio de Malta y LupuloRicardo PinillosNo ratings yet
- RHE10734986963E00115Document1 pageRHE10734986963E00115Ricardo PinillosNo ratings yet
- Regiones Lambayeque, Piura y TumbesDocument59 pagesRegiones Lambayeque, Piura y TumbesRicardo PinillosNo ratings yet
- Metodo Dicromato de Potasio 1Document1 pageMetodo Dicromato de Potasio 1Ricardo PinillosNo ratings yet
- SOLANINADocument20 pagesSOLANINARicardo PinillosNo ratings yet
- Formato para Imprimir en Papel MilimetradoDocument3 pagesFormato para Imprimir en Papel MilimetradoRicardo PinillosNo ratings yet
- Alvarez Burga Daniel MartinDocument172 pagesAlvarez Burga Daniel MartinRicardo PinillosNo ratings yet
- Tarea N 04Document10 pagesTarea N 04Ricardo PinillosNo ratings yet
- Síndrome de PickwickDocument33 pagesSíndrome de PickwickGreciaNo ratings yet
- ElectrocardiogramaDocument24 pagesElectrocardiogramaricardesc3527No ratings yet
- Tesis Flexibilidad CognitivaDocument195 pagesTesis Flexibilidad CognitivaLourdes FloresNo ratings yet
- Base y Bóveda Grupo 3Document11 pagesBase y Bóveda Grupo 3Jessica Paola ErasNo ratings yet
- Neurodesarrollo (1 Parte) - Fundamentos. Consideraciones Neurofisiológicas Básicas y Funcional. Madurez Cortical. Crecimiento, Maduración y Desarrollo.Document10 pagesNeurodesarrollo (1 Parte) - Fundamentos. Consideraciones Neurofisiológicas Básicas y Funcional. Madurez Cortical. Crecimiento, Maduración y Desarrollo.Euge BeltranNo ratings yet
- EndocrinofoniasDocument5 pagesEndocrinofoniasfernanda cespedesNo ratings yet
- La RespiraciónDocument9 pagesLa RespiraciónZuli HernandezNo ratings yet
- Manual Pilates Reformer 2017 3Document231 pagesManual Pilates Reformer 2017 3camila100% (1)
- Implementacion de Un Laboratorio de Control de CalidadDocument21 pagesImplementacion de Un Laboratorio de Control de Calidadmary_ely29_91955No ratings yet
- Accidentes Durante La PBMDocument11 pagesAccidentes Durante La PBMLuz Aquino apazaNo ratings yet
- Trabajo Reino AnimaliaDocument12 pagesTrabajo Reino AnimaliaYefimovich GrigoriNo ratings yet
- Metabolismo de Los CarbohidratosDocument24 pagesMetabolismo de Los CarbohidratosHuaygua colque Shirley cathiaNo ratings yet
- Informe Internado PDFDocument259 pagesInforme Internado PDFTreisy Alvarez CardenasNo ratings yet
- EtilenoDocument42 pagesEtilenolebiatan89100% (1)
- Micro ClasesDocument13 pagesMicro Clasesjosue alvaradoNo ratings yet
- Sistemas ArterialesDocument20 pagesSistemas ArterialesJarell VidalNo ratings yet
- Artritis Reumatoide y JuvenilDocument29 pagesArtritis Reumatoide y JuvenilJaviercito BlackNo ratings yet
- Postura y DiafragmaDocument4 pagesPostura y DiafragmaJennifer CastilloNo ratings yet
- Aaaa Recuperatorio Era 1 2022Document18 pagesAaaa Recuperatorio Era 1 2022maria trentinNo ratings yet
- Capitulo 31. FisioDocument22 pagesCapitulo 31. FisioAna Castro MondacaNo ratings yet
- Via Aerea EmbarazadaDocument5 pagesVia Aerea EmbarazadaBrenda FloresNo ratings yet
- Hormonas Presentes en El Ciclo Estral CaninoDocument10 pagesHormonas Presentes en El Ciclo Estral CaninoJHOAN MANUEL BARRERO MELENDRONo ratings yet
- Macrosomia FetalDocument8 pagesMacrosomia FetalJeancarlos QuispeNo ratings yet
- Taller KinesiologiaDocument71 pagesTaller KinesiologiaJuan José Vicente Baños100% (1)
- Célula Animal y VegetalDocument44 pagesCélula Animal y VegetalNekkthor RhoudalesNo ratings yet
- BRAZODocument32 pagesBRAZOMédecin Adrian TGNo ratings yet
- Sistema MuscularDocument36 pagesSistema MuscularAngie HerreraNo ratings yet