Professional Documents
Culture Documents
Bateria de Problemas para El Extraordinario Completo-2
Uploaded by
Hector Sanchez SolorzanoOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Bateria de Problemas para El Extraordinario Completo-2
Uploaded by
Hector Sanchez SolorzanoCopyright:
Available Formats
Batera de problemas
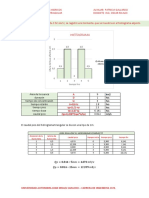
1. Una solucin que contiene 10 % de NaCl; 3 % de KCl y 87 % de agua se alimenta al
proceso mostrado en la figura a la velocidad de 18400 Kg/h. las composiciones de las
corrientes son como se indica. Producto del evaporador: (P): NaCl 16,8 %; KCl 21,6 % y
H2O 61,6 %
Recirculacin: (R): NaCl 18,9 %; KCl 12.3%; H 2O 68.8%. Calclese los Kg/h de (P) y
(R), tambin complete las composiciones de cada corriente.
2. Puede
portador,
agua pura
recuperase acetona de un gas
disolvindola en una corriente de
en
una
unidad
llamada
absorbedor. El diagrama de flujo
de
la
figura siguiente, 2000 lbm/h de
una corriente con 20% de acetona se tratan con 1000 lb/h de una corriente de agua
pura, lo que produce un gas de descarga libre de acetona y una solucin de acetona en
agua. Supngase que el gas portador no se disuelve en el agua
Gas
20% Acetona
80% Gas
Agua
Solucin
Acetona - Agua
Calcule todas las variables de corrientes desconocidas
1.
Una corriente A (en Kg/min.) que contiene 30% m de etanol y 70% m de agua se
mezcla con otra corriente B (en Kg/min.) que contiene 60m %m de etanol y el resto
de agua. La corriente de mezcla C (a la salida de la unidad mezcladora) contiene
35%m de etanol. Calcular:
a) La proporcin entre las corrientes A y B, esto es (A/B)
b) Si la corriente de salida C es 4500 Kg/h Cul es la relacin entre las corrientes A
y B? Esta relacin ha cambiado o no?
2.
En la figura siguiente se muestra una unidad de separacin de compuestos en 2
etapas. Dado el flujo de entrada F de 855 Kg/h calcular todas las corrientes
desconocidas y la composicin de la corriente B.
0.950Tolueno 0.050 Benceno
0.010 Tolueno 0.990 Benceno
C
F
0.400 Tolueno 0.400 Benceno 0.200 Xileno
3.
Tolueno
Xileno
Para el proceso de la siguiente figura, se desea determinar el caudal y la
composicin (%) m de la disolucin de la recirculacin R. Se conoce que :
F=10,000.00 lb/h de una disolucin acuosa 20% m de KNO
M=? lb/h de una disolucin 50% m de KNO
W=? lb/h HO pura
R=? lb de disolucin saturada 0.600 lb KNO/lb HO
C=? lb cristales con 4% de HO
Diagrama de flujo del proceso con mltiples unidades
W ? lb HO /h
4.
10000 lb/h
Evaporador
Cristalizador
El proceso industrial para la produccin
de H 2SO4 a partir de disulfuro de hierro
R
(trivialmente llamado pirita) se representa por el siguiente sistema de reacciones
consecutivas cuyas ecuaciones son:
4FeS2 + 11 O2
2SO2 + O2
SO3 + H2O
2FeO3 + 8SO2
2SO3
H2SO4
Las condiciones de reaccin determinadas experimentalmente para cada reactor
fueron las siguientes: con 10% ms de masa como exceso de O 2 la reaccin (1)
alcanza una conversin de 94 %; la reaccin de la ecuacin (2) logra un
rendimiento del 95% si se adiciona 15% en masa como exceso de O 2 y 20% en
masa de H2O. Por su parte la reaccin resumida en la ecuacin (3) tiene una
eficiencia del 97%.
Con esta informacin haga el balance de masa y el diagrama de flujo con los
valores calculados para un rgimen de alimentacin de 600 kg/h de pirita
5.
Fluye vapor de manera estable por una turbina adiabtica a una tasa de 45000
lbm/h; entra a 1000 psia y 900 F y sale a 5 psia como vapor saturado. Si la potencia
generada por la turbina es de 4 MW, determine la tasa de prdida de calor del
vapor .
6.
Agua a 50 F y 5 psia es calentada en una cmara mezclndola con vapor de agua
saturado a 50 psia. Si ambas corrientes entran a la cmara de mezclado con la
misma tasa de flujo msico, determine la temperatura y la calidad de la corriente
que sale.
7.
Aire a 100 kPa y 280 K se comprime de manera estable hasta 600 kPa y 400 k. La
tasa de flujo msico del aire es de 0.02 kg/s y hay una prdida de calor de 16 kJ/kg
durante el proceso. Si se supone que los cambios de la energa cintica y potencial
son despreciables, determine la entrada de potencia necesaria para el compresor.
8.
Se calienta agua lquida a 300 kPa y 20 C en una cmara mezclndola con vapor
sobrecalentado a 300kPa y 300 c el agua fra entra a la cmara a una taza de 1.8
kg/seg. Si la mezcla sale de la cmara a 60 C, determine la tasa de flujo msico
requerida del vapor sobrecalentado.
9.
1500 kg/h de un fuel que contiene un 88% de c y un 12 % en peso de H se quema
en un horno dando un gas de chimenea que contiene 13.1% de CO2, 3.7 % de O2 ,
83.2 % de N2 en composicin molar y base seca. El aire y el fuel oil entran al horno
a 25C y el horno pierde por las paredes 4.5 X 106 kcal/h. Calcular:
A)
Los kmol de gas de chimenea producidos.
B)
Los kmol de agua de combustin en el gas de chimenea por cada 10 kmol de gas
de chimenea seco
C)
El exceso de aire empleado
D)
La temperatura de los gases de chimenea.
DATOS:
Calores especficos de los gases en Kcal/ kmol C :
CO2 = 10.2 ; O2= 7.3 ; N2= 7.9 ; H2O (g) = 8.3
Variacin entlpica de la reaccin: a 25 C : C + O2
CO2 + 94000 kcal/kmol
Hf (H2O)(l) a 25 C = -68320 kcal/kmol
Calor latente de vaporizacin del H2O a 25 C = 10600 kcal/kmol.
10.
En la regeneracin del amoniaco, en el proceso Solvay se hace por la reaccin cuya
ecuacin es:
2NH4Cl + CaO
2NH3 +CaCl2 + H2O
En una prueba piloto se hicieron reaccionar 10 g de cloruro de amonio con 6 g de xido
de calcio (ambos reactantes puros). De donde se obtuvieron 0.70 litros de amoniaco en
CNPT; determine:
a) Los reactantes limitantes y en exceso; b) El porcentaje de reactante en exceso; c) El
rendimiento porcentual de la reaccin; d) El balance de masa del proceso.
11.
Se lleva a cabo la deshidrogenacin de etanol para formar acetaldehido de acuerdo a
la siguiente reaccin en un reactor adiabtico:
C2H5OH(g)
CH3CHO(g) + H2(g)
Hr (25C)= +68.95KJ/mol
El reactor se alimenta con el vapor de etanol a 300C, y se obtiene una conversin del
30%. Calcule la temperatura final de salida usando las siguientes capacidades
calorficas:
C2H5OH(g): Cp=0.110 kJ/mol .C
CH3CHO (g): Cp=0.080 kJ/mol .C
Se consideran constantes
H2(g): Cp=0.029 kJ/mol .C
You might also like
- Lista Ejercicios Tipo ExamenDocument10 pagesLista Ejercicios Tipo ExamenAlee OsoresNo ratings yet
- Guía 5Document4 pagesGuía 5cruzsilvaNo ratings yet
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Problemas TEMA9Document4 pagesProblemas TEMA9Jairo Manuel Saavedra AcostaNo ratings yet
- Balance de EnergiaDocument6 pagesBalance de EnergiaCarlos GamarraNo ratings yet
- Problemas resueltos de Hidráulica de CanalesFrom EverandProblemas resueltos de Hidráulica de CanalesRating: 4.5 out of 5 stars4.5/5 (7)
- Repartido 1 - Balances de MasaDocument6 pagesRepartido 1 - Balances de MasaAnna RobbinsNo ratings yet
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Taller 2. Parcial 2 PDFDocument1 pageTaller 2. Parcial 2 PDFjuanNo ratings yet
- Problem As Masa EnergiaDocument37 pagesProblem As Masa EnergiaSarita PerezNo ratings yet
- Ejercicios de balance de materia y energíaDocument16 pagesEjercicios de balance de materia y energíajorge amaya0% (1)
- Balance masa energíaDocument22 pagesBalance masa energíaJesús Francisco Vidaňa DuronNo ratings yet
- 08 Problemas Balance de Materia y EnergiaDocument13 pages08 Problemas Balance de Materia y EnergiaAntonio Uicab Ventura0% (1)
- Problemas BmeDocument16 pagesProblemas BmeFrancisca Condori CarpioNo ratings yet
- Problemas Sobre Balance de MateriaDocument10 pagesProblemas Sobre Balance de MateriaMadelein GisselNo ratings yet
- EjerciciosDocument6 pagesEjerciciosDiego Robles Cariaga0% (1)
- Guia 4 Ppios 1 (Balance de Energía Sin Reacción)Document6 pagesGuia 4 Ppios 1 (Balance de Energía Sin Reacción)carlos hernandezNo ratings yet
- Taller 5 Total Balances - Con - Reaccion - QuimicaDocument7 pagesTaller 5 Total Balances - Con - Reaccion - QuimicaHugo ZeaNo ratings yet
- Guia IIIDocument5 pagesGuia IIIElioRaulSifontesNo ratings yet
- Termodinámica: Práctica N° 2 de termodinámica con 25 problemas resueltosDocument8 pagesTermodinámica: Práctica N° 2 de termodinámica con 25 problemas resueltosFernando OrellanaNo ratings yet
- Problemas Practica 2 PDFDocument3 pagesProblemas Practica 2 PDFAnderson GRNo ratings yet
- II Examen de Diseño de ReactoresDocument10 pagesII Examen de Diseño de ReactoresJosep LopezNo ratings yet
- Problemas de evaporación y destilaciónDocument3 pagesProblemas de evaporación y destilacióngonzaloNo ratings yet
- Ejemplos 7Document6 pagesEjemplos 7IngrithDayhanaTobarNo ratings yet
- Problem. Balances de EnergíaDocument3 pagesProblem. Balances de EnergíaJonathan Bruno0% (1)
- Practica 3,4 y 5 Balance de Masa y Energia 1-2022Document6 pagesPractica 3,4 y 5 Balance de Masa y Energia 1-2022Rocinela Herbas PerezNo ratings yet
- además de ser optimizado para al incluir palabras clave como reacciones químicas y reactoresDocument6 pagesademás de ser optimizado para al incluir palabras clave como reacciones químicas y reactoresNatali CondeñaNo ratings yet
- Guiatiii - 2020Document7 pagesGuiatiii - 2020yoNo ratings yet
- Fabricación ácido nítrico NO monóxidoDocument4 pagesFabricación ácido nítrico NO monóxidoLauraBuitragoCortésNo ratings yet
- Balance de energía sin reacción químicaDocument6 pagesBalance de energía sin reacción químicaIsaac RodriguezNo ratings yet
- Und1 TareaDocument10 pagesUnd1 TareaArvell VillaresNo ratings yet
- Taller de Estudio Unidad 2Document4 pagesTaller de Estudio Unidad 2Medellin Practicante Control CalidadNo ratings yet
- Practica 3 SimulaciónDocument2 pagesPractica 3 SimulaciónNikole Elizabeth SantaCruz CarrascoNo ratings yet
- Problemas ImprimirDocument13 pagesProblemas ImprimirJocelynNo ratings yet
- Clase 4 ProblemasDocument6 pagesClase 4 ProblemasMauricio Ramirez0% (2)
- Termo EjemplosDocument6 pagesTermo Ejemplossaul lozadaNo ratings yet
- Boletines Problemas 3,4 FIQDocument5 pagesBoletines Problemas 3,4 FIQmartinguiraodiazNo ratings yet
- Guía 7 - EntropiaDocument4 pagesGuía 7 - EntropiaCarolinaBadillaNo ratings yet
- Practica Dirigida 3ra FaceDocument5 pagesPractica Dirigida 3ra FaceCristian Jhunnior CNo ratings yet
- Guia 3 de Termodinamica IDocument5 pagesGuia 3 de Termodinamica IAlfredoJoséSoléCorderoNo ratings yet
- Semana 05 Problemas de Balances de Masa y Energia, y OtrosDocument13 pagesSemana 05 Problemas de Balances de Masa y Energia, y Otroskakjjsaka0% (1)
- Semana 3Document18 pagesSemana 3Cesar Augusto Buendia Baldeon0% (1)
- H3-EFECTOS_TERMICOS_EN_REACTORES_IDEALES-2014-2015 campusDocument5 pagesH3-EFECTOS_TERMICOS_EN_REACTORES_IDEALES-2014-2015 campusCenaida ColinaNo ratings yet
- Boletin de Problemas de Balances de MateriaDocument5 pagesBoletin de Problemas de Balances de Materiakingscorpio96No ratings yet
- Practica de Balance de Masa y Energia 2Document3 pagesPractica de Balance de Masa y Energia 2Sebas ValdezNo ratings yet
- Acv s04 Tarea Calificada 1 Ecv - CompressDocument7 pagesAcv s04 Tarea Calificada 1 Ecv - CompressFabianAlbertoGameroChàvezNo ratings yet
- Guia de Ejercicios Balances Macroscopicos de EnergiaDocument5 pagesGuia de Ejercicios Balances Macroscopicos de EnergiaRaul Estay RodríguezNo ratings yet
- GUIA 4 BALANCE 2017 - EnergíaDocument3 pagesGUIA 4 BALANCE 2017 - EnergíaCarlos GarridrupiNo ratings yet
- Chemistry Engineer Material BalanceDocument4 pagesChemistry Engineer Material BalanceZezy BlueNo ratings yet
- Problemas TermodinamicaDocument7 pagesProblemas Termodinamicacaflita100% (1)
- 04 Problemas Balance de Materia y EnergiaDocument9 pages04 Problemas Balance de Materia y EnergiaHoyesun Valle0% (1)
- Ejercicios y 2 Talleres de DestilaciónDocument2 pagesEjercicios y 2 Talleres de DestilaciónDaniel Andrés Ortiz MontoyaNo ratings yet
- Balance de Materia y EnergiaDocument4 pagesBalance de Materia y EnergiaCamilo Montoya GarciaNo ratings yet
- Simulación de Procesos Unidad 2Document50 pagesSimulación de Procesos Unidad 2Carlos Gabriel Simon FloresNo ratings yet
- Absorción y Destilación SimpleDocument3 pagesAbsorción y Destilación SimpleRaisa VargasNo ratings yet
- Problemas - 14 - de BM y BE Con RXN - ClásicoDocument5 pagesProblemas - 14 - de BM y BE Con RXN - ClásicoHarold Cardenas0% (1)
- TermodinamicaaDocument7 pagesTermodinamicaaMichaelEduardoGonzalezLopezNo ratings yet
- Estructura Cristalina-IPN (Reparado1)Document51 pagesEstructura Cristalina-IPN (Reparado1)Hector Sanchez SolorzanoNo ratings yet
- Presentación Trabajo Final Kaisen en Power Point Tesina.Document10 pagesPresentación Trabajo Final Kaisen en Power Point Tesina.Hector Sanchez SolorzanoNo ratings yet
- Estructura Cristalina-IPN (Reparado1)Document41 pagesEstructura Cristalina-IPN (Reparado1)Hector Sanchez SolorzanoNo ratings yet
- Control de Los Procesos II Alum. 2 2Document62 pagesControl de Los Procesos II Alum. 2 2Hector Sanchez SolorzanoNo ratings yet
- Taller de Plataformas de Desarrollo DigitalDocument21 pagesTaller de Plataformas de Desarrollo DigitalHector Sanchez SolorzanoNo ratings yet
- Capacidad Del ProcesoDocument3 pagesCapacidad Del ProcesoHector Sanchez SolorzanoNo ratings yet
- Taller de Plataformas de Desarrollo DigitalDocument36 pagesTaller de Plataformas de Desarrollo DigitalHector Sanchez SolorzanoNo ratings yet
- Aprender A Dibujar - Un Metodo Garantizado - Betty Edwards - Arte para CristoDocument208 pagesAprender A Dibujar - Un Metodo Garantizado - Betty Edwards - Arte para Cristojosmigori54No ratings yet
- Agua Oxigenada UomDocument13 pagesAgua Oxigenada UomHector Sanchez SolorzanoNo ratings yet
- Control de La Calidad - Apuntes UpiicsaDocument9 pagesControl de La Calidad - Apuntes UpiicsaHector Sanchez SolorzanoNo ratings yet
- Metodología Del DiseñoDocument8 pagesMetodología Del DiseñoHector Sanchez SolorzanoNo ratings yet
- Estructura Cristalina-IPN (Reparado1)Document41 pagesEstructura Cristalina-IPN (Reparado1)Hector Sanchez SolorzanoNo ratings yet
- Estructura Cristalina-IPN (Reparado1)Document41 pagesEstructura Cristalina-IPN (Reparado1)Hector Sanchez SolorzanoNo ratings yet
- Proyecto Administración HidroponiaDocument5 pagesProyecto Administración HidroponiaHector Sanchez SolorzanoNo ratings yet
- Comonaceunparadigma MiDocument12 pagesComonaceunparadigma MiHector Sanchez SolorzanoNo ratings yet
- Apuntes Plantas y Proceso UpiicsaDocument56 pagesApuntes Plantas y Proceso UpiicsaHector Sanchez Solorzano50% (2)
- LiasterDocument35 pagesLiasterHector Sanchez SolorzanoNo ratings yet
- Bateria de Problemas 2º Departamental PPI (Reparado)Document4 pagesBateria de Problemas 2º Departamental PPI (Reparado)Hector Sanchez SolorzanoNo ratings yet
- Ingenieria en MaterialesDocument4 pagesIngenieria en MaterialesHector Sanchez SolorzanoNo ratings yet
- Estructura Cristalina-IPN (Reparado1)Document41 pagesEstructura Cristalina-IPN (Reparado1)Hector Sanchez SolorzanoNo ratings yet
- Propuesta de Examen de Plantas y Procesos Ind.Document6 pagesPropuesta de Examen de Plantas y Procesos Ind.Hector Sanchez SolorzanoNo ratings yet
- Procesos Industriales Balance Materia EnergíaDocument3 pagesProcesos Industriales Balance Materia EnergíaHector Sanchez SolorzanoNo ratings yet
- Propuesta de Remedio Her Bola Rio para Desintoxicacion BioeleemntalDocument4 pagesPropuesta de Remedio Her Bola Rio para Desintoxicacion BioeleemntalHector Sanchez SolorzanoNo ratings yet
- Inovacion Tecnologica y Transfer.-IpnDocument51 pagesInovacion Tecnologica y Transfer.-IpnHector Sanchez SolorzanoNo ratings yet
- Doble SumyDocument2 pagesDoble SumyEdgar SoteloNo ratings yet
- Estudio Hidraulico y Control de Erosion Del PuenteDocument143 pagesEstudio Hidraulico y Control de Erosion Del PuenteJohnny Ccatamayo BNo ratings yet
- PropDocument2 pagesPropdfdfd 1qweNo ratings yet
- Nuevos avances en fluidos de perforación y técnicas de refuerzo de pozos mejoran la resistencia del pozo y mitigan las pérdidasDocument6 pagesNuevos avances en fluidos de perforación y técnicas de refuerzo de pozos mejoran la resistencia del pozo y mitigan las pérdidasDaniel BuitrónNo ratings yet
- Sistema de Agua Fria. DotaciónDocument16 pagesSistema de Agua Fria. DotaciónSheyla GaimesNo ratings yet
- Memoria RontoyDocument14 pagesMemoria RontoyOnerom Luar0% (1)
- Charflame - Ficha Técnica V1Document2 pagesCharflame - Ficha Técnica V1Obrex Rehabilitación de EdificiosNo ratings yet
- Antisepticos y DesinfectantesDocument79 pagesAntisepticos y DesinfectantesJuan Sebastián Varón Figueroa100% (1)
- Manual de Especialidades para AventurerosDocument1 pageManual de Especialidades para AventurerosRebe BlancoNo ratings yet
- Impacto de las actividades humanas en el medio ambienteDocument29 pagesImpacto de las actividades humanas en el medio ambienteapmedadminNo ratings yet
- Proyecto Del Agua Recurso VitalDocument5 pagesProyecto Del Agua Recurso VitalBarbara QuirozNo ratings yet
- Elaboracion de Pescado Salado en Pila Humeda y Pila Seca PDFDocument24 pagesElaboracion de Pescado Salado en Pila Humeda y Pila Seca PDFlui-An100% (1)
- INFORMEDocument42 pagesINFORMEmaria jose cubas toroNo ratings yet
- Ejercicios de FluidosDocument9 pagesEjercicios de FluidosLuis OroscoNo ratings yet
- Facultad de Ingeniería, Programa de Ingeniería Agroindustrial, Laboratorios de Ingeniería BioquímicaDocument25 pagesFacultad de Ingeniería, Programa de Ingeniería Agroindustrial, Laboratorios de Ingeniería BioquímicaCESAR LUIS PALENCIA GUSMANNo ratings yet
- Fester Acriton 12Document7 pagesFester Acriton 12Jose Luis Arteaga SNo ratings yet
- Especificaciones Concreto ArmadoDocument20 pagesEspecificaciones Concreto ArmadoBryan Chacaltana AstoraymeNo ratings yet
- Trabajo MezclasDocument24 pagesTrabajo MezclasMagaNo ratings yet
- LIMPIEZA Y DESINFECCIÓNbDocument15 pagesLIMPIEZA Y DESINFECCIÓNbMilagros Aguilar EspinozaNo ratings yet
- Hidrograma triangular ejercicio cuenca 900 haDocument3 pagesHidrograma triangular ejercicio cuenca 900 haHector Reynaldo Porco MamaniNo ratings yet
- Tarea 5Document2 pagesTarea 5Mangel GuerreroNo ratings yet
- Como Criar Peces en Nuestra ComunidadDocument40 pagesComo Criar Peces en Nuestra ComunidadLovera GroverNo ratings yet
- Ficha Técnica DL10Document2 pagesFicha Técnica DL10Armando DC100% (1)
- Hoja de Seguridad Glutamato MonosodicoDocument4 pagesHoja de Seguridad Glutamato MonosodicoJuan Corcuera AlvarezNo ratings yet
- La Geografía Como Ciencia SocialDocument3 pagesLa Geografía Como Ciencia SocialPedro Ramirez llenqueNo ratings yet
- MSDS H-75Document7 pagesMSDS H-75Alisohn Andrea Cutiño LimaNo ratings yet
- Formato de PagoDocument1 pageFormato de Pagoviro7403No ratings yet
- Quiz sobre ecosistemas y contaminación del aguaDocument5 pagesQuiz sobre ecosistemas y contaminación del aguaFabiana CubillanNo ratings yet
- Prueba de SedimentacionDocument5 pagesPrueba de SedimentacionJames MathisNo ratings yet