Professional Documents
Culture Documents
Fuerzas Intermoleculares
Uploaded by
cosmefulanito0 ratings0% found this document useful (0 votes)
21 views2 pagesfuerzas amiguitos les traigo fuerzas hijos de su rpmt dre!!
Original Title
Fuerzas intermoleculares
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this Documentfuerzas amiguitos les traigo fuerzas hijos de su rpmt dre!!
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
21 views2 pagesFuerzas Intermoleculares
Uploaded by
cosmefulanitofuerzas amiguitos les traigo fuerzas hijos de su rpmt dre!!
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 2
Fuerzas intermoleculares
Las fuerzas intermoleculares se definen como el conjunto de fuerzas atractivas y repulsivas
que se producen entre las molculas como consecuencia de la presencia o ausencia de
electrones.
Cuando dos o ms tomos se unen mediante un enlace qumico forman una molcula, los
electrones que conforman la nueva molcula recorren y se concentran en la zona del tomo
con mayor electronegatividad, definimos la electronegatividad como la propiedad que
tienen los tomos en atraer electrones. La concentracin de electrones en una zona
especfica de la molcula crea una carga negativa, mientras que la ausencia de los
electrones crea una carga positiva.
Denominamos dipolos a las molculas que disponen de zonas cargadas negativamente y
positivamente debido a la electronegatividad y concentracin de los electrones en las
molculas.
Podemos asimilar el funcionamiento de un dipolo a un imn con su polo positivo y su polo
negativo, de tal forma que si acercamos otro imn el polo positivo atraer al polo negativo
y viceversa, dando como resultado una unin.
Nota: La diferencia est entre que las Intramoleculares mantienen unidas a los tomos en
una molcula y las intermoleculares determinan su estado fsico.
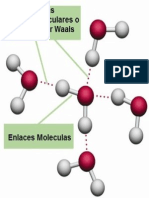
Fuerzas de Van der Waals
Estas interacciones ocurren cuando las molculas estn muy prximas. Todas las fuerzas de
van der Waals son cohesivas y varan con respecto a la distancia como 1/r6. Las fuerzas de
van der Waals son consideradas como la explicacin molecular para las energas cohesivas
de los lquidos y son semejantes en magnitud a las entalpas de vaporizacin de muchos
lquidos, su valor aproximado es de -41.84 kJ mol-1. Estas interacciones son dominantes en
reacciones en donde la proximidad es importante.
La energa almacenada por estos enlaces, sumada a la red molecular de todo el conjunto de
molculas que forma la sustancia, determina la estabilidad de estos enlaces.
En pocas palabras las fuerzas de van der Waals son fuerzas de estabilizacin molecular
(dan estabilidad a la unin entre varias molculas), tambin conocidas como atracciones
intermoleculares o de largo alcance y son las fuerzas entre molculas (fuerzas entre
molecula-molecula).
Son fuerzas ms dbiles que las internas que unen la molcula ya que dependen
exclusivamente del tamao y forma de la molcula pudiendo ser de atraccin o de
repulsin. Son tan dbiles que no se las puede considerar un enlace, como el enlace
covalente o inico, solo se las considera una atraccin.
You might also like
- Fuerzas IntermolecularesDocument4 pagesFuerzas IntermolecularescarolinaNo ratings yet
- Tipo de Fuerzas MolecularesDocument4 pagesTipo de Fuerzas MolecularesGuillermo FuentesNo ratings yet
- Fuerzas IntermolecularesDocument4 pagesFuerzas IntermolecularesMarcos Muñoz CardonaNo ratings yet
- Fuerzas de Van Der WaalsDocument7 pagesFuerzas de Van Der WaalsareacienciasNo ratings yet
- Fuerzas Intermoleculares Dipolo - DipoloDocument2 pagesFuerzas Intermoleculares Dipolo - DipoloLaura BazánNo ratings yet
- Fuerzas intermolecularesDocument11 pagesFuerzas intermolecularesirisevangelinajerezNo ratings yet
- Fuerzas Intermoleculares.Document6 pagesFuerzas Intermoleculares.EDGAR IVAN MORALES VALLESNo ratings yet
- Que Son Las Fuerzas IntermolecularesDocument7 pagesQue Son Las Fuerzas Intermolecularesjosbelis santoyoNo ratings yet
- Monografia de QuimicaDocument8 pagesMonografia de QuimicaJoa King Chaupis AdrianoNo ratings yet
- Muestra Tema 43Document8 pagesMuestra Tema 43LngNo ratings yet
- Tipos de Enlaces MolecularesDocument14 pagesTipos de Enlaces MolecularesCarlos CarranzaNo ratings yet
- Enlace CovalenteDocument10 pagesEnlace CovalenteLuis Carlos BautistaNo ratings yet
- Fuerzas IntermolecularesDocument10 pagesFuerzas IntermolecularesIvan JimenezNo ratings yet
- Fuerzas de Van Der WaalsDocument15 pagesFuerzas de Van Der WaalsRoberto ReyesNo ratings yet
- Practica 2 - Fuerzas Intermoleculares y SolubilidadDocument2 pagesPractica 2 - Fuerzas Intermoleculares y SolubilidadIsaac JuradoNo ratings yet
- Qué Son Las Fuerzas de Van Der WaalsDocument6 pagesQué Son Las Fuerzas de Van Der Waalsloren del portilloNo ratings yet
- Polaridad, Simetría, Propiedades Físicas y Química de Los Compuestos OrgánicosDocument10 pagesPolaridad, Simetría, Propiedades Físicas y Química de Los Compuestos OrgánicosEliezer TorresNo ratings yet
- Fuerzas IntermolecularesDocument4 pagesFuerzas IntermolecularesJuan Pedro Rivas TorresNo ratings yet
- Actividad 5 - Quimica - Cuadro ComparativoDocument6 pagesActividad 5 - Quimica - Cuadro ComparativoArmando MorenoNo ratings yet
- Fuerza de Van Der WaalsDocument10 pagesFuerza de Van Der WaalsJorgeNo ratings yet
- Fuerzas IntermolecularesDocument8 pagesFuerzas IntermolecularesElcira Alejandra Jaque JaqueNo ratings yet
- Fuerzas de Van Der WaalsDocument4 pagesFuerzas de Van Der WaalsSailly Johana Saurith CandelarioNo ratings yet
- Momento Dipolar y Fuerzas IntermolecularesDocument6 pagesMomento Dipolar y Fuerzas IntermolecularesJesusito Manuel RojasNo ratings yet
- INTRODUCCIONDocument9 pagesINTRODUCCIONDiego Hernandez CisnerosNo ratings yet
- Enlaces SecundariosDocument2 pagesEnlaces SecundariosEduardo Zavala50% (2)
- Fuerzas de Atracción de Sólidos y LíquidosDocument8 pagesFuerzas de Atracción de Sólidos y LíquidosJiancarlo O. HidalgoNo ratings yet
- Fuerzas IntermolecularesDocument7 pagesFuerzas IntermolecularesecmNo ratings yet
- T8 Cristian Uriel Cruz CarbarinDocument6 pagesT8 Cristian Uriel Cruz CarbarinCristian Uriel Cruz CarbarinNo ratings yet
- Cuestionario Previo 2 Brigada 3 LSQIDocument2 pagesCuestionario Previo 2 Brigada 3 LSQIasfb.americanistaNo ratings yet
- Fuerzas IntermolecularesDocument6 pagesFuerzas IntermolecularesVickyNo ratings yet
- Definiciones de términos químicosDocument7 pagesDefiniciones de términos químicosbrenda lopezNo ratings yet
- Tema 2: Interacciones MolecularesDocument4 pagesTema 2: Interacciones MolecularesVanesa SzaboNo ratings yet
- Numero 2Document4 pagesNumero 2skyfire aaNo ratings yet
- Estructura Molecular - Física ModernaDocument6 pagesEstructura Molecular - Física ModernaJuani BenitezNo ratings yet
- Practica 5Document1 pagePractica 5Rosaura Sántiz100% (1)
- Puentes de Hidrógeno 4,5,6Document4 pagesPuentes de Hidrógeno 4,5,6Juan Diego RujanoNo ratings yet
- LABORATORIO 4 UnionesDocument7 pagesLABORATORIO 4 UnionesDiego Hernandez0% (1)
- Seminario #3Document13 pagesSeminario #3Kristell QuezadaNo ratings yet
- Teoría Lewis, Ley de Octeto y OxidaciónDocument9 pagesTeoría Lewis, Ley de Octeto y OxidaciónMARIA MARCELA NOELLER SANDOVAL100% (1)
- Fabricio QuimicaDocument7 pagesFabricio QuimicaLesly Elena Honores TenorioNo ratings yet
- DocumentoDocument15 pagesDocumentoLuis A Hernandez MenesesNo ratings yet
- 2° Taller de Química OrgánicaDocument4 pages2° Taller de Química OrgánicaAldair ARNo ratings yet
- Fuerzas IntermolecularesDocument1 pageFuerzas IntermolecularesTritzi Amalin Ugueto AponteNo ratings yet
- P4 Antecedentes Efecto Del Disolvente en La Manifestación Del Carácter IónicoDocument2 pagesP4 Antecedentes Efecto Del Disolvente en La Manifestación Del Carácter IónicoCuervo AmbulanteNo ratings yet
- Trabajouu Quimica 1Document6 pagesTrabajouu Quimica 1Juan Camilo Cardenas DuranNo ratings yet
- Fuerzas IntermolecularesDocument6 pagesFuerzas IntermolecularesYuly Vanessa Caicedo PeñaNo ratings yet
- Qué Es Un Enlace QuímicoDocument3 pagesQué Es Un Enlace QuímicoNatalia campo ramirezNo ratings yet
- AntecedentesDocument17 pagesAntecedentesJosafat VidalNo ratings yet
- Definición y Clasificación Del Enlace QuimicoDocument9 pagesDefinición y Clasificación Del Enlace QuimicoCluisantony Jayco Dize100% (1)
- Fuerzas IntermolecularesDocument4 pagesFuerzas IntermolecularesAnna Paula Martinez AvilaNo ratings yet
- Termo 5 PDFDocument3 pagesTermo 5 PDFc3wwwww2No ratings yet
- Fuerzas intermoleculares Van der WaalsDocument6 pagesFuerzas intermoleculares Van der WaalsTayna RqpNo ratings yet
- Fuerzas intermoleculares: dipolo-dipolo, ion-dipolo, London y Van der WaalsDocument7 pagesFuerzas intermoleculares: dipolo-dipolo, ion-dipolo, London y Van der WaalsLuz Marina Peña MorajxkfjjkkzkfNo ratings yet
- Practica Laboratorio 4 - Villafuerte Duran Brigith ClarisaDocument14 pagesPractica Laboratorio 4 - Villafuerte Duran Brigith ClarisaClarisa Villafuerte DuranNo ratings yet
- Fuerzas de Van Der WaalsDocument3 pagesFuerzas de Van Der WaalsNycSandovalCandiaNo ratings yet
- Enlaces Químicos Informe 4Document4 pagesEnlaces Químicos Informe 4claudiaNo ratings yet
- Tema 5. Propiedades FísicasDocument51 pagesTema 5. Propiedades FísicasEdgar MedinaNo ratings yet
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseFrom EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseRating: 4.5 out of 5 stars4.5/5 (7)
- Características y aplicaciones de la espectroscopía molecularFrom EverandCaracterísticas y aplicaciones de la espectroscopía molecularNo ratings yet
- Unidad I Proyecto EmpresarialDocument39 pagesUnidad I Proyecto EmpresarialALVA PRODUCCIONES 4KNo ratings yet
- Res 412 2000Document9 pagesRes 412 2000lisethmcNo ratings yet
- Trabajo - Arbol de ProblemasDocument6 pagesTrabajo - Arbol de ProblemasJessi Casilla ApazaNo ratings yet
- Trabajo Final de Presupuesto 2Document32 pagesTrabajo Final de Presupuesto 2Dante Belmonth67% (3)
- Acuerdo transaccional lesionesDocument29 pagesAcuerdo transaccional lesionesvictor mayta cruzNo ratings yet
- Practica CalificadaDocument4 pagesPractica CalificadaRoder Arnol Torre Salvador100% (1)
- Punta lógica TTLDocument2 pagesPunta lógica TTLCristian Daniel Gonzalez RodriguezNo ratings yet
- BORDILLODocument5 pagesBORDILLOJavier Muñoz RomanNo ratings yet
- Guia Del GremioDocument9 pagesGuia Del GremioHéctor Rodríguez AntúnezNo ratings yet
- Catalogo Conectores Serie 451 441Document27 pagesCatalogo Conectores Serie 451 441carlos ricardoNo ratings yet
- Appolbook FINALDocument143 pagesAppolbook FINALCristian OrtizNo ratings yet
- Extraccion de Aceite de ZapalloDocument10 pagesExtraccion de Aceite de ZapalloKatheryne Paola Ochoa100% (1)
- PNL I Nivel 2022-2 InicialDocument5 pagesPNL I Nivel 2022-2 Inicialluis cruzNo ratings yet
- Exploración InicialDocument19 pagesExploración InicialAna Karina ZCNo ratings yet
- Los Indicadores y Su Construccion RizoDocument15 pagesLos Indicadores y Su Construccion RizoAdriana Escalante RojanoNo ratings yet
- Nivelacion Fisica 1P UndecimoDocument2 pagesNivelacion Fisica 1P UndecimoAndres CaipeNo ratings yet
- 200010S4 El Valor y La Equidad InternaDocument18 pages200010S4 El Valor y La Equidad InternaMaría piscoNo ratings yet
- El KerógenoDocument20 pagesEl KerógenoLuis Alberto Tupa CoilaNo ratings yet
- Propiedades de Las Operaciones Binarias de Los Numeros RealesDocument2 pagesPropiedades de Las Operaciones Binarias de Los Numeros RealesAlejandroo2797No ratings yet
- Codigo Tributario Libro IDocument18 pagesCodigo Tributario Libro IRichard Ramos CutimboNo ratings yet
- Disposiciones Complementarias FinalesDocument2 pagesDisposiciones Complementarias FinalesAdriana NicollNo ratings yet
- ¿Qué Es Ganoderma?Document22 pages¿Qué Es Ganoderma?EdgarBusiness100% (1)
- Unidad Didáctica #2-2021Document27 pagesUnidad Didáctica #2-2021Nicolás ManonniNo ratings yet
- Evolucion Historica y Antecedentes Del Mercado Laboral en VenezuelaDocument3 pagesEvolucion Historica y Antecedentes Del Mercado Laboral en VenezuelaRey SolitarioNo ratings yet
- Comisión EuropeaDocument47 pagesComisión EuropeaenologiacomNo ratings yet
- Electroforesis de PapelDocument16 pagesElectroforesis de PapelValle Zamorano Elaine NicoleNo ratings yet
- Preguntas de Preparación - Caso Dalia - LOS ESTRATEGASDocument2 pagesPreguntas de Preparación - Caso Dalia - LOS ESTRATEGASAndresAgüeroGonzales100% (1)
- Firma Electrónica Fallo - AFLUENTA S.A. C CELIZ MARIA S Cobro EjecutivoDocument21 pagesFirma Electrónica Fallo - AFLUENTA S.A. C CELIZ MARIA S Cobro EjecutivoLoana PonceNo ratings yet
- Rubrica para Evaluar Investigacin en WordDocument1 pageRubrica para Evaluar Investigacin en Wordapi-257093331No ratings yet
- Mcdonald Cultura OrganizacionalDocument2 pagesMcdonald Cultura OrganizacionalJhon Campoverde20% (5)