Professional Documents
Culture Documents
Importancia Biomedica
Uploaded by
Rosa Mariia Quezada Arteaga0 ratings0% found this document useful (0 votes)
65 views2 pagesOriginal Title
IMPORTANCIA BIOMEDICA.docx
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
65 views2 pagesImportancia Biomedica
Uploaded by
Rosa Mariia Quezada ArteagaCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 2
IMPORTANCIA BIOMEDICA
Desde el punto de vista qumico, la oxidacin se define como la eliminacin de electrones, en
tanto que la reduccin es la ganancia de electrones. De este modo, la oxidacin siempre se
acompaa de reduccin de un aceptor de electrn. Este principio de oxidacin - reduccin aplica
por igual a sistemas bioqumicos y es un concepto importante que fundamenta el entendimiento
de la naturaleza de la oxidacin biolgica. Note que muchas oxidaciones biolgicas pueden tener
lugar sin la participacin de oxigeno molecular. Por ejemplo: deshidrogenaciones. La vida de
animales superiores depende por completo de un aporte de oxgeno para la respiracin, el
proceso por medio del cual las clulas obtienen energa en forma de ATP a partir de la reaccin
controlada de hidrogeno con oxgeno para formar agua. Adems, el oxgeno molecular se
incorpora hacia diversos sustratos mediante enzimas llamadas oxigenasa, muchos frmacos,
contaminantes y carcingenos qumicos (xenobioticos) son metabolizados por enzimas de esta
clase, conocidas como el sistema de citocromo P450. La administracin de oxigeno puede salvar la
vida en el tratamiento de pacientes con insuficiencia respiratoria o circulatoria
LOS CAMBIOS DE ENERGIA LIBRE PUEDEN EXPRESARSE EN TERMINOS DE POTENCIAL DE REDOX
En reacciones que conllevan oxidacin y reduccin, el cambio de energa libre es proporcional a la
tendencia de los reactivos a donar electrones o aceptarlos. De esta manera, adems de expresar
cambio de energa libre en cuanto a 0, es posible, de un modo anlogo, expresarlo de manera
numrica como un potencial de oxidacin reduccin o redox (0 ). El potencial redox de un
sistema (0 ) por lo general se compara con el potencial del electrodo de hidrogeno (0.0 voltios a
pH de 0.0). sin embargo, para sistemas biolgicos, el potencial redox (0 ) por lo general se
expresa a pH de 7.0 al cual el potencial de electrodo de hidrogeno es de -0.42 voltios. El cuadro
12-1 muestra los potenciales redox de algunos sistemas redox de inters especial en bioqumica
de mamferos. Las posiciones relativas de los sistemas redox en el cuadro permiten predecir la
direccin de flujo de electrones desde una reja redox hacia otra.
Las enzimas comprendidas en oxidacin y reduccionreciben el nombre de oxidorreductasas y se
clasifican en cuatro grupos: oxidasas, deshidrogenasas, hidroperoxidasas y oxigenasas.
- LAS OXIDASAS USAN OXIGENO COMO UN ACEPTOR DE HIDROGENO
Las oxidasas catalizan la eliminacin de hidrogeno desde un sustrato usando oxigeno
como un aceptor de hidrogeno. Forman agua o perxido de hidrogeno como un producto
de reaccin (fig 12-1)
- ALGUNAS OXIDASAS CONTIENEN COBRE
La citocromo oxidasa es una hemoproteina ampliamente distribuida en muchos tejidos,
que tiene el grupo prosttico hem tpico presente en la mioglobina, hemoglobina y otros
citocromos. Es el componente terminal de la cadena de acarreadores respiratorios
encontrados en mitocondrias y transfiere electrones originados por la oxidacin de
molculas de sustrato por deshidrogenasas hacia su aceptor final, oxigeno. La enzima es
envenenada por monxido de carbono, cianuro y sulfuro de hidrogeno. Tambin se ha
denominado citocromo a. Empero, ahora se sabe que el hem a, se combina con otro
hem, el hem a, en una protena nica para formar el complejo de enzima citocromo
oxidasa y asi es ms correcto llamarlo citocromo aa3. Contiene dos molculas de hem,
cada una de las cuales tiene un tomo de Fe que oscila entre Fe3+ y Fe2+ durante oxidacin
y reduccin. Ms aun, hay dos tomos de Cu, cada uno relacionado con una unidad hem
- OTRAS OXIDASAS SON FLAVOPROTEINAS
Las enzimas flavoproteina contienen flavina mononucleotido (FMN) o flavina adenina
dinucleotido (FAD) como grupos prostticos. Las FMN y FAD se forman en el cuerpo a
partir de la vitamina riboflavina, por lo regular estn unidos de modo estrecho- aunque no
covalente - a sus protenas apoenzima respectivas. Las metaloflavoproteinas contienen
uno o ms metales como cofactores esenciales. Los ejemplos de enzimas flavoproteina
son: L-aminocido oxidasa, enzima enlazada a FMN que se encuentra en los riones con
especificidad general por la desaminacion oxidativa de los L-aminoacidos que existen de
manera natural; xantina oxidasa, que contiene molibdeno, es importante en la conversin
de bases purina en cido rico y tiene una particular importancia en animales uricotelicos
y aldehdo deshidrogenasa, enzima enlazada a FAD presente en hgados de mamferos,
que contiene molibdeno y hierro no hem, y acta sobre aldehdos y sustratos N-
heterocclicos. Los mecanismos de oxidacin y reduccin de estas enzimas son complejos.
La evidencia sugiere una reaccin de dos pasos
CUADRO: Algunos potenciales redox de inters especial en sistemas de oxidacin de
mamferos
SISTEMA Ee Voltios
+
H /H2 -0.42
NAD+/NADH -0.32
Lipoato; ox/red -0.29
Acetoacetato/3-hidroxibutirato -0.27
Piruvato/lactato -0-19
Oxaloacetato/malato -0-17
Fumarato/ succinato +0.03
Citocromo b; Fe3+/Fe2+ +0.08
Ubiquinona; ox/red +0.10
Citocromo c; Fe3+/Fe2+ +0.22
3+ 2+
Citocromo a; Fe /Fe +0.29
Oxigenos/agua +0.82
You might also like
- Circuito Primer Orden RCDocument9 pagesCircuito Primer Orden RCDayiito Morales100% (1)
- Estudio de Ondas Amortiguadas en Una Cuerda VibranteDocument17 pagesEstudio de Ondas Amortiguadas en Una Cuerda VibranteMauro GuerraNo ratings yet
- Conf. No.5 ESTEREOQUIMICADocument58 pagesConf. No.5 ESTEREOQUIMICAJeny Serrano0% (1)
- Taller 5Document4 pagesTaller 5DANNERI LEZAMA GALLEGOSNo ratings yet
- Tamaño de Las Partículas ColoidalesDocument5 pagesTamaño de Las Partículas ColoidalesGustavoToapantaNo ratings yet
- TEMA 5, Instrumentos de Presion y Temperatura.Document17 pagesTEMA 5, Instrumentos de Presion y Temperatura.Sadith SifuentesNo ratings yet
- Caracteristicas de TTL y CmosDocument7 pagesCaracteristicas de TTL y CmosSaul RiveroNo ratings yet
- Taller Colavorativo #2 - CIIIDocument4 pagesTaller Colavorativo #2 - CIIIJostin danilo gonzalezNo ratings yet
- Calibracion LDRDocument3 pagesCalibracion LDRHarold David Villacís100% (1)
- Sistemas Multicomponentes 2Ay2BDocument37 pagesSistemas Multicomponentes 2Ay2BTania FloresNo ratings yet
- Principio de Superposicion y OndasDocument16 pagesPrincipio de Superposicion y OndasjoseNo ratings yet
- DIFERENCIALESDocument5 pagesDIFERENCIALESJose Angel MitlNo ratings yet
- Practica3 - Metodos - Eq5 UPIBIDocument8 pagesPractica3 - Metodos - Eq5 UPIBIWendy DiazNo ratings yet
- Tarea No. 3 Espectro UV Visible Analisis Instrumental IBQ UAA 2021 (Completo 2)Document10 pagesTarea No. 3 Espectro UV Visible Analisis Instrumental IBQ UAA 2021 (Completo 2)Derek Ebenezer Mata NavarroNo ratings yet
- CronoamperometriaDocument17 pagesCronoamperometriaDaniel HenaoNo ratings yet
- Práctica 6 - Procesos Químicos Y Corriente Eléctrica - Aldo Esaú Xoxocotla SánchezDocument14 pagesPráctica 6 - Procesos Químicos Y Corriente Eléctrica - Aldo Esaú Xoxocotla Sánchezxozo land100% (1)
- 3 Parcial Análisis Instrumental 2da OpDocument29 pages3 Parcial Análisis Instrumental 2da OpBrian RodriguezNo ratings yet
- Reporte Digitales 6Document8 pagesReporte Digitales 6Ivann Zs'No ratings yet
- Ley de Ohm y Efecto JouleDocument2 pagesLey de Ohm y Efecto JouleCristian SabanaNo ratings yet
- Articulo de PolimerosDocument3 pagesArticulo de PolimerosLudwiig Damiian MaldonadoNo ratings yet
- Circuitos RL (Resistor, Inductor) - y RLC (Resistor, Inductor y CapacitorDocument31 pagesCircuitos RL (Resistor, Inductor) - y RLC (Resistor, Inductor y CapacitorJoe Berny100% (1)
- Guia de Fisic de La Energia UPIBIDocument3 pagesGuia de Fisic de La Energia UPIBIRebeca Pérez PNo ratings yet
- Problemario 2 Físisca de La Energía UPIBIDocument4 pagesProblemario 2 Físisca de La Energía UPIBITecuitlatl100% (1)
- LEY DE HESS, DIAGRAMA EQUILIBRIO para FQ2020 VERSION FINALDocument17 pagesLEY DE HESS, DIAGRAMA EQUILIBRIO para FQ2020 VERSION FINALJuanita rosasNo ratings yet
- Programa de Estudio para Bioquímica ClínicaDocument13 pagesPrograma de Estudio para Bioquímica ClínicaArthur GNo ratings yet
- Resumen Espectrometría de Absorción AtómicaDocument6 pagesResumen Espectrometría de Absorción AtómicaRoger Villar DurandNo ratings yet
- Cuasi Niveles de Fermi y Recombinacion RadiactivaDocument5 pagesCuasi Niveles de Fermi y Recombinacion RadiactivaGonzzalez SsebaNo ratings yet
- Espectroscopia de FluorescenciaDocument5 pagesEspectroscopia de FluorescenciaAmairany CorellaNo ratings yet
- TAREA 6 CinéticaDocument14 pagesTAREA 6 CinéticaManuel CortezNo ratings yet
- Ejercicios Campos Electricos EstaticosDocument13 pagesEjercicios Campos Electricos EstaticosAiza Mónica Aponte HernándezNo ratings yet
- Exposicion PerturbacionalDocument18 pagesExposicion PerturbacionalLaura RiiveraNo ratings yet
- InvestigaciónDocument13 pagesInvestigaciónMartinNo ratings yet
- Δt = T - T Δt = K *m Δt = 0.0 - (-2.95) ; ΔT = 2.95 m= ; m= 2.95/1.86= 1.53 molalDocument2 pages Δt = T - T Δt = K *m Δt = 0.0 - (-2.95) ; ΔT = 2.95 m= ; m= 2.95/1.86= 1.53 molalLuis RuizNo ratings yet
- Electro Práctica 11Document9 pagesElectro Práctica 11EdAlaman100% (1)
- Informe 5 Equilibrio QuimicoDocument9 pagesInforme 5 Equilibrio QuimicoDiana Supo OsorioNo ratings yet
- Tema 2 PDFDocument14 pagesTema 2 PDFCristianNo ratings yet
- Oscilaciones Armónicas de Un Péndulo-InformeDocument6 pagesOscilaciones Armónicas de Un Péndulo-InformeKarol ChavarroNo ratings yet
- s1 SadikuDocument6 pagess1 SadikuCristian VidalNo ratings yet
- Difusión UnidimensionalDocument18 pagesDifusión UnidimensionalIsai Martinez JimenezNo ratings yet
- Word Tierras Raras MonografiaDocument36 pagesWord Tierras Raras Monografiamexalurgia50% (2)
- Trbajo de TorrecillasDocument4 pagesTrbajo de TorrecillasMa Antonieta GalindoNo ratings yet
- Quimica 4Document848 pagesQuimica 4DAVID AriasNo ratings yet
- Electrodos Indicadores de Membrana o Electrodos Selectivos de IonesDocument1 pageElectrodos Indicadores de Membrana o Electrodos Selectivos de IonesRonalStivenEspañaNo ratings yet
- Practica 3. Ondas Mecánicas en Medios Elásticos.Document24 pagesPractica 3. Ondas Mecánicas en Medios Elásticos.Cassandra GonzálezNo ratings yet
- Lab8. Acondicionamiento de Sensores de Presión PDFDocument4 pagesLab8. Acondicionamiento de Sensores de Presión PDFjuan sebastian aldana camachoNo ratings yet
- Transferencia de Masa Por ElectrodeposiciónDocument15 pagesTransferencia de Masa Por ElectrodeposiciónBryan Martínez0% (1)
- Ley de LambertDocument5 pagesLey de LambertLeyner SalgadoNo ratings yet
- GfyyfyfyfDocument54 pagesGfyyfyfyfJulio GiraldoNo ratings yet
- Informe Inorganica 7Document6 pagesInforme Inorganica 7Karen TamayoNo ratings yet
- Analisis de Superficies Mediante AES - XPS y CEMSDocument53 pagesAnalisis de Superficies Mediante AES - XPS y CEMSLuis AngelNo ratings yet
- 1 BWDocument4 pages1 BWNelssi ColqueNo ratings yet
- SpectrosDocument24 pagesSpectrosDaniel Menéndez CrespoNo ratings yet
- Fisica Del Estado SolidoDocument5 pagesFisica Del Estado SolidoLuis Alejandro Terán MontoyaNo ratings yet
- PRACTICA #5.análisisDocument4 pagesPRACTICA #5.análisisJasmin ZoteloNo ratings yet
- Informe 3 de QuimicaDocument6 pagesInforme 3 de QuimicaEvelin HidalgoNo ratings yet
- Actividad 4Document7 pagesActividad 4Jose David Perez NavarroNo ratings yet
- Oxidacion Biolgica Medical Studs 1Document4 pagesOxidacion Biolgica Medical Studs 1roseNo ratings yet
- Bioquímica: Enzimas Oxido-Reductasas Involucradas en Reacciones RedoxDocument24 pagesBioquímica: Enzimas Oxido-Reductasas Involucradas en Reacciones RedoxAnonimo22No ratings yet
- 2 Oxidaciones BiologicasDocument9 pages2 Oxidaciones BiologicasLucasNo ratings yet
- Derecho A La Energia ElectricaDocument2 pagesDerecho A La Energia ElectricaRosa Mariia Quezada ArteagaNo ratings yet
- Procesal Penal PeritajesDocument16 pagesProcesal Penal PeritajesRosa Mariia Quezada ArteagaNo ratings yet
- Sociologia Nacional EnviarDocument3 pagesSociologia Nacional EnviarRosa Mariia Quezada ArteagaNo ratings yet
- Hurto Agravado - CADENA DE CUSTODIADocument4 pagesHurto Agravado - CADENA DE CUSTODIARosa Mariia Quezada ArteagaNo ratings yet
- Derecho EconómicoDocument8 pagesDerecho EconómicoRosa Mariia Quezada ArteagaNo ratings yet
- Clases de CooperativasDocument5 pagesClases de CooperativasRosa Mariia Quezada ArteagaNo ratings yet
- Derecho A La Energia ElectricaDocument2 pagesDerecho A La Energia ElectricaRosa Mariia Quezada ArteagaNo ratings yet
- Pre Informe c3Document35 pagesPre Informe c3Rosa Mariia Quezada ArteagaNo ratings yet
- Ensayo de FamiliaDocument2 pagesEnsayo de FamiliaRosa Mariia Quezada ArteagaNo ratings yet
- Identificación de Peligros Evaluación de Riesgos y Determinación de ControlesDocument19 pagesIdentificación de Peligros Evaluación de Riesgos y Determinación de ControlesCamilyn RamirezNo ratings yet
- CascaraDocument6 pagesCascaraRosa Mariia Quezada ArteagaNo ratings yet
- CascaraDocument6 pagesCascaraRosa Mariia Quezada ArteagaNo ratings yet
- Aguita Pa Ti JajaDocument1 pageAguita Pa Ti JajaRosa Mariia Quezada ArteagaNo ratings yet
- TLC Peru ChinaDocument7 pagesTLC Peru ChinaRosa Mariia Quezada ArteagaNo ratings yet
- Acta de Sustentación de Tesis Actualizada CatherineDocument6 pagesActa de Sustentación de Tesis Actualizada CatherineRosa Mariia Quezada ArteagaNo ratings yet
- Identificación de Peligros Evaluación de Riesgos y Determinación de ControlesDocument19 pagesIdentificación de Peligros Evaluación de Riesgos y Determinación de ControlesCamilyn RamirezNo ratings yet
- Cuadro Sinóptico. ForenseDocument5 pagesCuadro Sinóptico. ForenseRosa Mariia Quezada Arteaga0% (1)
- Acta de Sustentacion 2Document1 pageActa de Sustentacion 2Rosa Mariia Quezada ArteagaNo ratings yet
- Junta de AcreedoresDocument8 pagesJunta de AcreedoresRosa Mariia Quezada ArteagaNo ratings yet
- FiliaciónDocument21 pagesFiliaciónRosa Mariia Quezada ArteagaNo ratings yet
- NiasDocument1 pageNiasRosa Mariia Quezada ArteagaNo ratings yet
- ANEXOS ImagenesDocument6 pagesANEXOS ImagenesRosa Mariia Quezada ArteagaNo ratings yet
- Auto Estim ADocument1 pageAuto Estim ARosa Mariia Quezada ArteagaNo ratings yet
- Punto Mas Frio en Conserva de ZanahoriaDocument12 pagesPunto Mas Frio en Conserva de ZanahoriaRosa Mariia Quezada ArteagaNo ratings yet
- Himno Nacional Del PeruDocument3 pagesHimno Nacional Del PeruRosa Mariia Quezada ArteagaNo ratings yet
- Capitulo 2 BanDocument1 pageCapitulo 2 BanRosa Mariia Quezada ArteagaNo ratings yet
- Analísis Sociojurídico Del Porqué en La Localidad Del Santa Los Magistrados Son Criticados 2015Document2 pagesAnalísis Sociojurídico Del Porqué en La Localidad Del Santa Los Magistrados Son Criticados 2015Rosa Mariia Quezada ArteagaNo ratings yet
- Capitulo 2 BanDocument29 pagesCapitulo 2 Banstefanymor10No ratings yet
- Informe N°13 DestilacionDocument32 pagesInforme N°13 DestilacionRosa Mariia Quezada ArteagaNo ratings yet
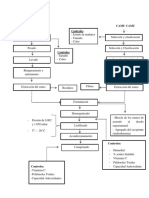
- Arandano Camu Camu Controles: Blanqueamiento y Enfriamiento Blanqueamiento y EnfriamientoDocument1 pageArandano Camu Camu Controles: Blanqueamiento y Enfriamiento Blanqueamiento y EnfriamientoRosa Mariia Quezada ArteagaNo ratings yet
- Aceite de Omega 3 Botella Nutra Bebé Lider - CLDocument1 pageAceite de Omega 3 Botella Nutra Bebé Lider - CLNidia CuevasNo ratings yet
- Diapositivas 8. Nomenclatura OrgánicaDocument22 pagesDiapositivas 8. Nomenclatura Orgánicaalex brunoNo ratings yet
- Exposición de Bioquímica de GlicosaminoglucanosDocument7 pagesExposición de Bioquímica de GlicosaminoglucanosKevin PerdomoNo ratings yet
- Transporte de Cargas en Sistemas BiologicosDocument2 pagesTransporte de Cargas en Sistemas Biologicosyoemis100% (1)
- Quíz Nomenclatura Inorgánica.Document3 pagesQuíz Nomenclatura Inorgánica.William MolanoNo ratings yet
- Glosario DieteticaDocument3 pagesGlosario DieteticaMary Itzel Hall TqmNo ratings yet
- Universidad Nacional Agraria de La Selva: Facultad de Recursos Naturales RenovablesDocument40 pagesUniversidad Nacional Agraria de La Selva: Facultad de Recursos Naturales RenovablesDemetrio Angelo Lama IsminioNo ratings yet
- Norma Astm E3Document15 pagesNorma Astm E3Angel AngelesNo ratings yet
- AlquinosDocument33 pagesAlquinosBrendaGüizaNo ratings yet
- Poliesteres y PoliamidasDocument27 pagesPoliesteres y PoliamidasAngel Trejo SegoviaNo ratings yet
- Laboratorio AlcoholesDocument13 pagesLaboratorio AlcoholesXavier VillonNo ratings yet
- Guia Rapida CDocument7 pagesGuia Rapida CChristian Bernal HerreraNo ratings yet
- P1Document8 pagesP1Gabriel AltamiranoNo ratings yet
- GTC 53-2Document24 pagesGTC 53-2IsabellaBonilla0% (1)
- Triptico - Sobre - El - Dominiod de La Taxonomia ModernaDocument2 pagesTriptico - Sobre - El - Dominiod de La Taxonomia ModernaGeomar Magdalena Arreaga TorresNo ratings yet
- Extracciã"n de La Trimiristina de La Nuez MoscadaDocument6 pagesExtracciã"n de La Trimiristina de La Nuez MoscadaJorge CastroNo ratings yet
- Informe 6 de FitoquimicaDocument5 pagesInforme 6 de FitoquimicaR. Daniel RodríguezNo ratings yet
- Quimica y La CocinaDocument4 pagesQuimica y La CocinaFrancisco100% (1)
- Celula ProcariotaDocument3 pagesCelula ProcariotaStephany Conde PoloNo ratings yet
- Upao Los Caminates Del NorteDocument50 pagesUpao Los Caminates Del NorteAlejandra PozoNo ratings yet
- Quimica OrganicaDocument53 pagesQuimica OrganicaEnrrique SalazarNo ratings yet
- Clase 1-2 CarbohidatosDocument5 pagesClase 1-2 CarbohidatosDaniel MuñozNo ratings yet
- Taller Nivelacion Profundizacion 11°Document7 pagesTaller Nivelacion Profundizacion 11°Delcy OCNo ratings yet
- Laboratorio Nº6 de Analisis Quimico CuantitativoDocument18 pagesLaboratorio Nº6 de Analisis Quimico CuantitativoJose FernandezNo ratings yet
- Balance Material MQ La Unión ZacapaDocument61 pagesBalance Material MQ La Unión ZacapaBrianNo ratings yet
- Clonación GeneticaDocument11 pagesClonación GeneticaAlex Guijarro PadillaNo ratings yet
- Extracción de ADNDocument5 pagesExtracción de ADNFrancisco Inzunza SaavedraNo ratings yet
- Botánica, CitologíaDocument10 pagesBotánica, CitologíaBárbara SmerkinNo ratings yet
- Quimica OrganicaDocument4 pagesQuimica OrganicaemanuelNo ratings yet
- Tesis SilviaDocument234 pagesTesis SilviaMishelle GuzmánNo ratings yet