Professional Documents
Culture Documents
Trabajo de Laboratorio de Fisico Quimica-Ley de Boyle
Uploaded by
anon_763006655Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Trabajo de Laboratorio de Fisico Quimica-Ley de Boyle
Uploaded by
anon_763006655Copyright:
Available Formats
INTEGRANTES: SEMESTRE: 3º
LASTENIA ARIPONA FECHA: 31/08/2016
YERLIN KARINA CALLE PAZ
REYNALDO CUELLAR VARGAS
JHONATAN CUELLAR ABREGO
KAROLYN ILLESCAS MARTINEZ
CRISTOFER GONZALES MAMANI
JOSE CARLOS LELARGE PLATA
PRACTICA Nº1
LEY DE BOYLE Y MARIOTTE
OBJETIVO GENERAL:
Observar el comportamiento de las variables
Establecer relación entre las variables: Presión, volumen a temperatura constante
OBJETIVO ESPECIFICO:
Demostrar hipótesis planteada sobre la ley de Boyle y Mariotte
FUNDAMENTO TEORICO
De los tres estados de agregación, solo el estado gaseoso permite la descripción
cuantitativa relativamente sencilla. Por el momento limitaremos esta descripción a las
relaciones entre las propiedades de tales como la masa, presión volumen y
temperatura.
El estado gaseoso es el más simple de los tres estados fundamentales de la materia
(gaseoso, líquido y solido). Un gas difiere de la materia en estado líquido o en solido
en que no posee un volumen intrínseco, es decir, ocupa todo el volumen de cualquier
espacio cerrado donde se encuentra. Estas y otras propiedades de los gases se
interpretan en términos de la teoría cinética de los gases. En principio se debe
puntualizar que cuando se habla de un ´´gas´´ generalmente estamos considerando un
´´gas perfecto o ideal´´, cuyo comportamiento esta dictado por las diversas leyes de
los gases. Todos los gases reales (He,Cl2, CO2,NH3), difieren en algún grado de los
imaginarios gases perfectos, pero es mas conveniente definirlas propiedades de un
gas perfecto y señalar luego las desviaciones particulares con respecto a este ideal.
En 1662, Robert Boyle realizo las primeras medidas cuantitativas del comportamiento
de los gases en relación a la presión y el volumen. Sus resultados indicaron que su
volumen es inversamente proporcional a la presión. Para el caso limite d un gas ideal
(presión suficiente baja, temperatura suficiente alta), las correspondencia entre las
variables de estado P, V, T y n es descrita por la ecuación térmica o general de estado:
PV=nRT, (R: constante universal de los gases)
Para el caso de cantidad de sustancia constante y proceso isotérmico, la ecuación se
reduce a:
INTEGRANTES: SEMESTRE: 3º
LASTENIA ARIPONA FECHA: 31/08/2016
YERLIN KARINA CALLE PAZ
REYNALDO CUELLAR VARGAS
JHONATAN CUELLAR ABREGO
KAROLYN ILLESCAS MARTINEZ
CRISTOFER GONZALES MAMANI
JOSE CARLOS LELARGE PLATA
PV= constante
P=(constante)(1/V)
Acorde a esta ecuación determinamos empíricamente por boyle-mariotte, el
incremento de presión que acompaña a un decremento de volumen y viceversa.
PRESION: La presión es una magnitud física que mide la proyección de la fuerza en
dirección perpendicular por unidad de superficie.
VOLUMEN: Es una magnitud métrica de tipo escalar definida como la extensión en
tres dimensiones de una región del espacio
TEMPERATURA: Es una magnitud escalar relacionada con la energía interna de un
sistema termodinámico, definida por el principio cero de la termodinámica.
2.- MATERIALES:
Aparato para ley de Boyle-Mariotte
INTEGRANTES: SEMESTRE: 3º
LASTENIA ARIPONA FECHA: 31/08/2016
YERLIN KARINA CALLE PAZ
REYNALDO CUELLAR VARGAS
JHONATAN CUELLAR ABREGO
KAROLYN ILLESCAS MARTINEZ
CRISTOFER GONZALES MAMANI
JOSE CARLOS LELARGE PLATA
Vernier
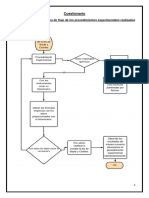
3.- PROCEDIMIENTO
1. Fije el aparato en la mesa de trabajo
2. Mida el diámetro interior de tubo y la temperatura ambiente. Anótela en su
cuaderno
3. Desplace el pistón del tubo mediante el tornillo y déjelo en una posición a 22cm
de cita graduada que tiene el tubo. Mida la presión el manómetro
4. Mueva el tornillo al fin de comprimir el aire en el tubo hasta alcanzar la posición
del embolo a 20cm. Mida la presión en el manómetro. Repita el paso anterior
hasta alcanzar la posición de 7cm
5. Anotar el valor de la presión atmosférica.
6. Realizar el calculo correspondiente, del volumen que ocupa en el aire en cada
desplace del pistón.
7. Realizar el grafico presión (N/m2) versus volumen (m3)
CALCULOS Y RESULTADOS
Diámetro exterior de vidrio=
Temperatura ambiente=
Presión atmosférica=
Longitud Volumen Presión Presión atm Presión abs
(cm) (m3) manométrica (N/m2) (N/m2)
20 2.1972 0 1.0027
18 1.9774 0 1.0027
16 1.7577 0.2721 1.0027 1.2748
14 1.5380 0.4082 1.4109
12 1.3183 0.5443 1.547
10 1.0986 0.6804 1.6831
8 0.8789 0.9525 1.9552
6 0.6592 1.3608 1.0027 2.3635
INTEGRANTES: SEMESTRE: 3º
LASTENIA ARIPONA FECHA: 31/08/2016
YERLIN KARINA CALLE PAZ
REYNALDO CUELLAR VARGAS
JHONATAN CUELLAR ABREGO
KAROLYN ILLESCAS MARTINEZ
CRISTOFER GONZALES MAMANI
JOSE CARLOS LELARGE PLATA
4 0.4394 1.905 2.9077
2 0.2197 2.9938 3.9965
Donde la presión absoluta, se calcula como P=Pm+Pa, donde Pm es la presión
media en el manómetro del equipo y Pa es la presión atmosférica.
a) Desarrolle todos los cálculos y las conversiones necesarias para completar
la tabla.
Para hallar el volumen de cada dato se utilizó la fórmula del
volumen de un cilindro.ej:
V= π r 2 h
1.87
V= ¿¿
π¿
Para obtener los datos en presión manométrica se realizó una
conversión de PSI a atm.ej:
1 atm
44psi × =2.9938 atm
14.6968 psi
Para obtener la presión absoluta se realiza la suma de la presión
manométrica más presión atmosférica.ej:
Pabs=Pman+Patm
b) Grafique los datos de la tabla anterior en un gráfico P-V es decir la presión
absoluta en (N/m2) y el volumen en m3. ¿Cómo se llama esta curva?
0,2197 2,9938 Es una curva isoterma
0,4394 1,905
0,6592 1,3608
0,8789 0,9525
1,0986 0,6804
1,3183 0,5443 c) Describa al menos cuatro propiedades físicas que
1,538 0,4082 definen por completo el estado físico de un gas.
1,7577 0,2721 Los gases ocupan completamente el volumen
1,9774 0 del recipiente que los contiene
2,1972 0 Los gases pueden comprimirse fácilmente
debido a que existen enormes espacios vacíos entre sus moléculas
Los gases son fluidos altamente comprensibles, que experimentan grandes
cambios de densidad con la presión y la temperatura.
La mayoría de los gases necesitan temperatura muy baja para lograr
condensarse.
INTEGRANTES: SEMESTRE: 3º
LASTENIA ARIPONA FECHA: 31/08/2016
YERLIN KARINA CALLE PAZ
REYNALDO CUELLAR VARGAS
JHONATAN CUELLAR ABREGO
KAROLYN ILLESCAS MARTINEZ
CRISTOFER GONZALES MAMANI
JOSE CARLOS LELARGE PLATA
d) Un gas ideal es sometido a una compresión isotérmica reduciendo su volumen a
4.50cm3. L a presión y volumen final del gas son 5.78x10 3mmhg y 6.55cm3
respectivamente. Calcula la presión inicial de gas en:
a. Pascal (Pa)
b. Atmosfera (atm)
DATOS
V1=4.50cm3
P1=?
P2=5.78x103mmhg
V2=6.55cm3
a) P1V1=P2V2
P2 V
P1= 2
V1
5.78 ×10 3 (6.55)
P1= =8413.1mmHg
4.50
133.322 Pa
P1=8413.1mmHgx =1121651.318 Pa
1 mmHg
5.78 ×10 3 (6.55) 1 atm
b) P1= =8413.1mmHg × =11.0698 atm
4.50 760 mmHg
P1=11.0698atm.
You might also like
- Problemas resueltos de Hidráulica de CanalesFrom EverandProblemas resueltos de Hidráulica de CanalesRating: 4.5 out of 5 stars4.5/5 (7)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesFrom EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesNo ratings yet
- Practica 3 FisicoquímicaDocument10 pagesPractica 3 FisicoquímicaRocha Valdovinos Aurelio NicolásNo ratings yet
- Ley de Charles y Gay Lussac-2015-IDocument7 pagesLey de Charles y Gay Lussac-2015-IWalter Chaupi PumacharaNo ratings yet
- Practica de Laboratorio N°1. Ley de Boyle - Fisicoquimica 1Document11 pagesPractica de Laboratorio N°1. Ley de Boyle - Fisicoquimica 1Miguel E. Villalobos GuerraNo ratings yet
- P. 5-Mezcla de GasesDocument9 pagesP. 5-Mezcla de GasesKuro Shiro50% (2)
- Primera Practica QuimicaDocument14 pagesPrimera Practica QuimicaSergio GonzalezNo ratings yet
- Experimento 4 QuimicaDocument26 pagesExperimento 4 QuimicaDiego MendozaNo ratings yet
- Reporte de Practica No.1 Quimica AplicadaDocument13 pagesReporte de Practica No.1 Quimica AplicadaMiau MiauNo ratings yet
- PRACTICA 2 Densidad y Peso Molecular de Un GasDocument7 pagesPRACTICA 2 Densidad y Peso Molecular de Un GasCAMILA CALDERON DORAMENo ratings yet
- Fisicoquimica Trabajo TerminadoDocument10 pagesFisicoquimica Trabajo Terminadoyosi.mahu.0033No ratings yet
- Practica 1 LabquimicaDocument14 pagesPractica 1 LabquimicaLuis perezNo ratings yet
- Reporte P2 - Lab - TermodinamicaDocument15 pagesReporte P2 - Lab - TermodinamicaAnnel AquinoNo ratings yet
- FQDocument14 pagesFQJoaco VilacaguaNo ratings yet
- Fisicoquimica Laboratorio 1Document22 pagesFisicoquimica Laboratorio 1Chrystian ParedesNo ratings yet
- FQ Lab 6 ARACELLY MONTORO ROJASDocument10 pagesFQ Lab 6 ARACELLY MONTORO ROJASAracelly rojasNo ratings yet
- Tarea Semana 7 Termo Dinamica Marcelo 2021Document14 pagesTarea Semana 7 Termo Dinamica Marcelo 2021Marcelo Martinez AlvarezNo ratings yet
- Informe de Fisicoquimica 1Document10 pagesInforme de Fisicoquimica 1Oscar Enrique Lopez MontañoNo ratings yet
- Ejercicio IndividualDocument7 pagesEjercicio IndividualMauricio SuarezNo ratings yet
- Fisico SolucionariosDocument390 pagesFisico Solucionariosargentina-2009No ratings yet
- Fisico SolucionariosDocument391 pagesFisico Solucionariosnenitalistania100% (1)
- LEY DE BOYLE Al 85%Document19 pagesLEY DE BOYLE Al 85%Lisacio Gago LopezNo ratings yet
- Ley de Charles y BoylesDocument5 pagesLey de Charles y BoylesAdrian Cabezas SolaresNo ratings yet
- Ley de Charles y BoylesDocument5 pagesLey de Charles y BoylesAdrian Cabezas SolaresNo ratings yet
- Lab 4 Fisica PDFDocument6 pagesLab 4 Fisica PDFEduardo BeltranNo ratings yet
- Quimica P1Document15 pagesQuimica P1olbatab74No ratings yet
- Reporte Practica 4 FinalDocument6 pagesReporte Practica 4 FinalMadeleine FloresNo ratings yet
- Ley de Boyle y MariotteDocument7 pagesLey de Boyle y MariotteMaykoll Alberto Zenteno ClarosNo ratings yet
- P 5 Mezcla de GasesDocument9 pagesP 5 Mezcla de GasesmarioNo ratings yet
- Taller Sem6-Qca10Document8 pagesTaller Sem6-Qca10johana cortezNo ratings yet
- Trabajo IrrigaciobesDocument15 pagesTrabajo IrrigaciobesarnaldocubaNo ratings yet
- Practica (1) ..Document12 pagesPractica (1) ..CRISTHIAN NUÑEZ LIMACHENo ratings yet
- FQ Lab 1Document10 pagesFQ Lab 1Aracelly rojasNo ratings yet
- Termometria de Gases-TermoDocument9 pagesTermometria de Gases-TermoJuan Francisco IslasNo ratings yet
- Lab 03 Termodinámica y Gases NoblesDocument12 pagesLab 03 Termodinámica y Gases Noblesdenis de la cuzNo ratings yet
- Ley BoyleDocument20 pagesLey BoyleCristian DiazNo ratings yet
- Informe 2Document14 pagesInforme 2adelina hernandezNo ratings yet
- Practicas de Termo de Gases - FIME UANLDocument25 pagesPracticas de Termo de Gases - FIME UANLErik Morales100% (2)
- Practica 1 GasesDocument11 pagesPractica 1 GasesCarlos A Villalobos100% (2)
- Lab Oratorio 4 QuimicaDocument9 pagesLab Oratorio 4 QuimicaJuan Miguel DiazNo ratings yet
- 4#RPDocument12 pages4#RPDiana OchoaNo ratings yet
- Informe 1,2,3Document9 pagesInforme 1,2,3Rodrigo Lope FloresNo ratings yet
- Informe Química 7Document6 pagesInforme Química 7Marzzia Santos UgazNo ratings yet
- Coeficiente Adiabático de GasesDocument12 pagesCoeficiente Adiabático de GasesRubi Nieto UgarteNo ratings yet
- Guias Mea 421gDocument21 pagesGuias Mea 421ggonzalo burgosNo ratings yet
- Laboratorio N 3 QuimicaDocument18 pagesLaboratorio N 3 QuimicaAndrews Alexander Erazo RondinelNo ratings yet
- Actividad - Fundamentos Gases IdealesDocument13 pagesActividad - Fundamentos Gases Idealesvelezricardo954No ratings yet
- Leyes de Los Gases Ideales - Informe 7 FinalDocument10 pagesLeyes de Los Gases Ideales - Informe 7 Finalcamila barrera barrientosNo ratings yet
- Práctica #5 - Determinación de La Constante IdealDocument6 pagesPráctica #5 - Determinación de La Constante IdealJose LeónNo ratings yet
- Laboratorio BOYLEDocument7 pagesLaboratorio BOYLESharon Gabriela Cornejo100% (1)
- PRACTICA 3 Gases IdealesDocument5 pagesPRACTICA 3 Gases Idealeskrystal rodriguez moralesNo ratings yet
- Práctica de Química. Determinación de La Masa Molar Del OxígenoDocument8 pagesPráctica de Química. Determinación de La Masa Molar Del Oxígenodpnrgqw58jNo ratings yet
- Reporte 8 Ley de Los GasesDocument8 pagesReporte 8 Ley de Los GasesMichael Legalize StoneNo ratings yet
- Energía Mediante Vapor, Aire o Gascapitulo12 PDFDocument25 pagesEnergía Mediante Vapor, Aire o Gascapitulo12 PDFNayarid OcañaNo ratings yet
- Norma ENOHSA. VIDocument164 pagesNorma ENOHSA. VIAntonella DemonteNo ratings yet
- Guía1 7mo Básico Ciencias Naturales Teoría Cinetico MolecularDocument6 pagesGuía1 7mo Básico Ciencias Naturales Teoría Cinetico MolecularNéstor MesaNo ratings yet
- Centrales Hidroeléctricas y Termoeléctricas en ColombiaDocument23 pagesCentrales Hidroeléctricas y Termoeléctricas en ColombiaDianne DuarteNo ratings yet
- SLPT 35366Document3 pagesSLPT 35366golfredinNo ratings yet
- Analisis Dimensional Ingenieria 2023Document4 pagesAnalisis Dimensional Ingenieria 2023Angel Fernandez MoralesNo ratings yet
- Sa Masa Reducida PRDocument7 pagesSa Masa Reducida PRJorge Enrique Santos AndahuaNo ratings yet
- Decs200 CD-6627 PDFDocument141 pagesDecs200 CD-6627 PDFWashington Lorenzo Lama MayorgaNo ratings yet
- Arranque Estrella TrianguloDocument6 pagesArranque Estrella TrianguloGuillermo duranNo ratings yet
- Trabajo de Corrección de Factor de Potencia y Conexión de Transformadores Trifásicos en ParaleloDocument10 pagesTrabajo de Corrección de Factor de Potencia y Conexión de Transformadores Trifásicos en ParaleloLuis fernando perezNo ratings yet
- Asociacion de ResistenciasDocument5 pagesAsociacion de ResistenciaszahirNo ratings yet
- 1el Hoy de La Fuerza Por Juan Jose Gonzalez Badillo - CompressDocument32 pages1el Hoy de La Fuerza Por Juan Jose Gonzalez Badillo - CompressAdriian NaviaNo ratings yet
- Practica de Laboratorio Propiedades MateriaDocument2 pagesPractica de Laboratorio Propiedades MateriaPalmer E. Yataco Valdez100% (3)
- Laboratorio N 2 Medida de Valores Medios y EficacesDocument9 pagesLaboratorio N 2 Medida de Valores Medios y Eficacesjuan carlos ChambiNo ratings yet
- Evaluacion Sumativa 1 Laboratorio de Corriente ContinuaDocument4 pagesEvaluacion Sumativa 1 Laboratorio de Corriente ContinuaHernan NavarroNo ratings yet
- Leyes Ponderales EstequiometriaDocument23 pagesLeyes Ponderales EstequiometriajuanNo ratings yet
- Marco Teorico-Linea de ConduccionDocument4 pagesMarco Teorico-Linea de ConduccionmanuelNo ratings yet
- Solucion TALLER 2Document16 pagesSolucion TALLER 2afgaleanoNo ratings yet
- Tarea Cap 27Document2 pagesTarea Cap 27Marco Antonio VillegasNo ratings yet
- Formulario Física IIDocument4 pagesFormulario Física IIKuranashiNo ratings yet
- Matriz de Evaluacion 1S-2020 AlexandraDocument21 pagesMatriz de Evaluacion 1S-2020 AlexandraVILLACIS ORQUERA RENE DAVIDNo ratings yet
- QUIMICA - Informe Ley OhmDocument11 pagesQUIMICA - Informe Ley OhmJose LarreaNo ratings yet
- 8 Taller Sonido Cuerdas y Tubos SonorosDocument2 pages8 Taller Sonido Cuerdas y Tubos SonorosCatalina Roberto100% (2)
- Motor, Driver y Regulador 2Document7 pagesMotor, Driver y Regulador 2yoshio takakiNo ratings yet
- El Lado Oscuro Del UniversoDocument9 pagesEl Lado Oscuro Del UniversoHéctor CovarrubiasNo ratings yet
- Punto de Trabajo de Un DiodoDocument6 pagesPunto de Trabajo de Un Diodoalex_pizarro_290% (1)
- Equilibrio Gas LiquidoDocument11 pagesEquilibrio Gas LiquidoYazmin Anahi FloresNo ratings yet
- Proyecto FisicaDocument2 pagesProyecto FisicaDaniel AsquiNo ratings yet
- LAS FUERZAS. La EXPLICACION DE LOS CAMBIOSDocument5 pagesLAS FUERZAS. La EXPLICACION DE LOS CAMBIOSmseli1060% (5)
- Reenvío Angular Serie 4000Document8 pagesReenvío Angular Serie 4000Victor BacilioNo ratings yet