Professional Documents
Culture Documents
Laboratorio 3 Ino Acidos y Bases
Uploaded by
Victor ManuelCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Laboratorio 3 Ino Acidos y Bases
Uploaded by
Victor ManuelCopyright:
Available Formats
FUNDAMENTO TEÓRICO
equilibrios de solubilidad
es importante también considerar aquí el estudio de otros equilibrios que tienen que ver con
otro tipo importante de reacción en solución :la disolución o precipitación de compuestos
iónicos ,que son reacciones heterogéneas .la disolución de un precipitado tiene lugar cuando el
producto de las concentraciones de los iones en la solución es menor que el producto de
solubilidad .la disolución y precipitación de compuestos son fenómenos que ocurren dentro de
nuestro organismo como en los alrededores .por ejemplo ,la disolución del esmalte dental en
soluciones acidas produce caries .la precipitación de ciertas sales en los riñones originan los
cálculos .al considerar los equilibrios de solubilidad se hacen predicciones cuantitativas acerca
de la cantidad de compuesto dado que se va a disolver .también se pueden utilizar dichos
equilibrios para analizar los factores que afectan la solubilidad.
Se denomina producto de solubilidad a la constante de equilibrio de la reacción de disolución
.se debe recordar que una solución saturada es aquella en la cual la solución está en contacto
con soluto sin disolver .cuando en la molécula del compuesto existen en laces iónicos ,estas se
van a disolver disociándose en iones ,lo que le da un carácter electrolítico a la solución .por
ejemplo: una solución acuosa saturada de baso4.puesto que el sólido es un compuesto iónico
,es un electrolito fuerte y produce iones ba+2 y so4-2 al disolverse .se establece rápidamente
el equilibrio siguiente entre el sólido no disuelto y los iones hidratados en la solución :
El lado izquierdo de la ecuación contiene una sustancia solida pura .al escribir las expresiones
de equilibrio para equilibrios heterogéneos ,no se consideran las concentraciones de los
sólidos y líquidos puros .por consiguiente ,la expresión de equilibrio para la disolución de un
sólido iónico ligeramente soluble depende solo de las concentraciones molares de las especies
en solución .debido a que el equilibrio expresa el grado en el que el sólido es soluble en agua
,la constante de equilibrio se conoce como
Reacción iónica
Las reacciones químicas entre soluciones de electrolitos no son reacciones entre moléculas
sino entre iones. por ejemplo, la reacción neta entre las soluciones del nitrato de plata y el
cloruro de sodio se puede expresar mediante la ecuación iónica.
Agcl =(ag+) + cl-
Ya que las otras sustancias iónicas como el ion na+ y no3- , se mantienen en la solución como
iones espectadores
Las reacciones químicas iónicas pueden clasificarse dentro de los cuatro tipos siguientes
Reacciones con formacion de precipitado
A partir de los compuestos solubles que contengan los iones necesarios es posible
obtener un compuesto insoluble o precipitado. por ejemplo, las ecuaciones iónicas
netas
Zn+2(ac) + s-2(ac) =znS
Mg+2(AC) + 2OH-(ac) =MgOH2(s)
Reacciones con liberación de un gas
Hay ocasiones en las que el producto de una reacción intercambio o metátesis es un
gas que tiene baja solubilidad en agua .por ejemplo el sulfuro de hidrogeno ,se forma
cuando un acido fuerte reacciona con un sulfuro metalico como el na2s
2Na(+) + S(-2)+2H(+)+SO4-2 =H2S(g) + 2Na+(ac)+SO4-2
2H+(AC)+S-2(ac)=H2S(S)
Los carbonatos y bicarbonatos también reaccionan con acidos fuertes para formar un
gas como el CO2(g).
Reacciones con formacion de un electrolito
Cualquier sustancia cuya solución acuosa contiene iones se denomina electrolito.
Cualquier sustancia que forma una solución que no contiene iones es un no electrolito
.los electrolitos que están presentes en solución totalmente como iones son los
electrolitos fuertes ,mientras que los que están parcialmente como iones y
parcialmente como moléculas son electrolitos débiles .al representar la ionización de
un electrolito débil en solución se utiliza se utiliza una doble flecha para indicar que las
reacciones inversa y directa puede lograr un balance llamado equilibrio químico .los
electrolitos débiles más importantes son: agua ,ácidos y bases débiles ,radicales ácidos
de los ácidos poli atómicos que contienen el ion h+ y radicales básicos poli atómicos
que contienen el ion OH-.
Las reacciones de formacion de un electrolito débil pueden ser de:
OBJETIVO
Conocer los diferentes tipos de reacciones iónicas.
Ilustrar conceptos químicos tales como formación de precipitados, desprendimiento
de gases, formación de iones complejos, interacciones acido-base a través de algunas
reacciones en pequeña escala.
Saber que el agua potable está constituida al menos por algunos iones en solución.
EXPERIMENTO 3
Observaciones
El sulfato de sodio, sulfato de aluminio y el sulfato de zinc son incoloros transparentes.
Las tres soluciones anteriores presentan olores fuertes y están estado líquido
(acuoso).
Se observa que al verter el cloruro de bario al sulfato de sodio se forma de manera
inmediata una espuma lechosa y en el fondo se da un precipitado el cual es el cloruro
de sodio.
Al verter el cloruro de bario en la solución de sulfato de aluminio se forma un
precipitado el cual es el cloruro de aluminio y se forma una espuma lechosa.
Al agregar al sulfato de zinc la solución de cloruro de bario se observa que se forma un
precipitado el cual es el cloruro de zinc y el color de esta solución es blanco.
Al agregar a la solución de sulfato de calcio el fosfato acido sódico se da la formacion
de espuma de color blanco no transparente.
La solución de sulfato de cobre es de color celeste y al agregar el hidróxido de sodio se
torna de color celeste lechoso.
Al verter el sulfato de cobre con el yoduro de potasio se da un precipitado de color
negro plomo y la solución pasa a un color marrón mostaza.
Ecuaciones químicas
Ca+2 + (SO4)2-(ac) + 2Na+(ac) + (HPO4)2(ac) Ca3(PO4)2(s) +(SO4)2-(ac) +
2Na+(ac)
Ca+2 + (SO4)2-(ac) + 2K+(ac) + 2I-(ac) CuI2(s) + (SO4)2-(ac) + 2K+(ac)
Ca+2 + (SO4)2-(ac) + 2Na+(ac) + 2OH-(ac) Cu(OH)2(s) +(SO4)2-(ac) +
2Na+(ac)
(SO4)2-(ac) + Zn2+(ac) + Ba2+(ac) + 2Cl-(ac) BaSO4(S) + Zn2+(ac) + 2Cl-(ac)
(SO4)2-(ac) + 2Na2+(ac) + Ba2+(ac) + 2Cl-(ac) BaSO4(S) + 2 Na+(ac) + 2Cl-(ac)
(SO4)2-(ac) + Al3+(ac) + Ba2+(ac) + Cl-(ac) BaSO4(S) + Al3+(ac) + Cl-(ac)
Diagrama de flujo
Explicación y discusión de resultados
En la mayoría de las reacciones se lleva a cabo la reacción con sales son estas sales los que se
descomponen(ionizan)y se da como resultado la presencia de iones en la solución esto hace
que la solución sea un electrolito (conduce la corriente) en tres de estas reacciones se forman
el sulfato de bario y en los demás fosfatos de calcio, yoduro cúprico e hidróxido de cobre son
estas sustancias los que le dan un color a la solución haciéndolo en casos celeste, marrón,
blanco.
observaciones finales
En las tres reacciones de cloruro de bario se forma el sulfato de bario.
El cloruro de bario y el sulfato de sodio se forma un precipitado el cual es el cloruro de
sodio.
El color marrón en la solución de sulfato de cobre y yoduro de potasio es el yoduro de
cobre.
El color celeste intenso en la solución de sulfato de cobre e hidróxido de sodio es por la
formacion de hidróxido de cobre.
comentarios y/o apreciaciones
En algunas reacciones se demoraba un cierto tiempo para que se formara el
precipitado.
Se aprecia que el cambio de color es por la formacion de un producto que es
característico de ese color.
En el experimento se tuvo que hallar dos reactivos los cuales me den el reactivo que
nos pedían.
conclusiones
Las reacciones que se han llevado a cabo en este experimento son reacciones entre
iones y no entre moléculas siendo estos últimos los que permanecen igual por lo cual
solo hay un reordenamiento de iones, los iones que permanecen igual son llamados
iones espectadores.
You might also like
- David FischmanDocument3 pagesDavid FischmanVictor ManuelNo ratings yet
- Titulacion de H3PO4 FinalDocument20 pagesTitulacion de H3PO4 FinalVictor ManuelNo ratings yet
- David FischmanDocument3 pagesDavid FischmanVictor ManuelNo ratings yet
- Diapos Mezcla de Acido Fosforico y Acido ClorihidricoDocument3 pagesDiapos Mezcla de Acido Fosforico y Acido ClorihidricoVictor ManuelNo ratings yet
- Solubilidad PDFDocument24 pagesSolubilidad PDFJuan GutierrezNo ratings yet
- Titulacion de H3PO4 FinalDocument20 pagesTitulacion de H3PO4 FinalVictor ManuelNo ratings yet
- Labo 7 CuantiDocument14 pagesLabo 7 CuantiVictor ManuelNo ratings yet
- ¿Cuál Es La Capital Histórica Del Peru?Document12 pages¿Cuál Es La Capital Histórica Del Peru?Victor ManuelNo ratings yet
- Guia Laboratorio 5Document5 pagesGuia Laboratorio 5Victor ManuelNo ratings yet
- La Pobreza Voluntaria de Nuestro SeñorDocument11 pagesLa Pobreza Voluntaria de Nuestro SeñorVictor ManuelNo ratings yet
- Boleta de Matricula Y Horario 2020-1 Duplicado: Universidad Nacional de IngenieriaDocument1 pageBoleta de Matricula Y Horario 2020-1 Duplicado: Universidad Nacional de IngenieriaVictor ManuelNo ratings yet
- RESUMENDocument19 pagesRESUMENVictor ManuelNo ratings yet
- Dios No Se Acordará Del PecadoDocument13 pagesDios No Se Acordará Del PecadoVictor ManuelNo ratings yet
- La gran paciencia de Dios con el culpableDocument10 pagesLa gran paciencia de Dios con el culpableVictor ManuelNo ratings yet
- CristoDocument13 pagesCristoVictor ManuelNo ratings yet
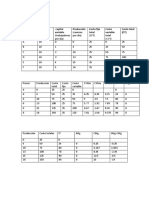
- Considere Los Costos Totales y Los Ingresos Totales de La Siguiente TablaDocument4 pagesConsidere Los Costos Totales y Los Ingresos Totales de La Siguiente TablaVictor Manuel78% (9)
- Cristo VencedorDocument11 pagesCristo VencedorVictor ManuelNo ratings yet
- Fichas de SeguridadDocument2 pagesFichas de SeguridadVictor ManuelNo ratings yet
- Trabajo 5Document5 pagesTrabajo 5Victor ManuelNo ratings yet
- Página 4/EP/BEGO1 C/20171419KDocument3 pagesPágina 4/EP/BEGO1 C/20171419KVictor ManuelNo ratings yet
- Adición Polar Al Grupo CDocument10 pagesAdición Polar Al Grupo CVictor ManuelNo ratings yet
- Considere Los Costos Totales y Los Ingresos Totales de La Siguiente TablaDocument4 pagesConsidere Los Costos Totales y Los Ingresos Totales de La Siguiente TablaVictor Manuel78% (9)
- Prueba de EntradaDocument2 pagesPrueba de EntradaVictor ManuelNo ratings yet
- San LuisDocument4 pagesSan LuisVictor ManuelNo ratings yet
- Metodo Fisico de SeparacionDocument52 pagesMetodo Fisico de SeparacionSilverioElieNo ratings yet
- Prueba de EntradaDocument2 pagesPrueba de EntradaVictor ManuelNo ratings yet
- Ejercicios TopicosDocument4 pagesEjercicios TopicosVictor Manuel100% (1)
- OctaveDocument1 pageOctaveVictor ManuelNo ratings yet
- CapitalDocument1 pageCapitalVictor ManuelNo ratings yet
- Laboratorio 3 Ino Acidos y BasesDocument4 pagesLaboratorio 3 Ino Acidos y BasesVictor ManuelNo ratings yet
- Isocop PDFDocument4 pagesIsocop PDFFlor RoldanNo ratings yet
- Marx - Trabajo Asalariado y Capital PDFDocument27 pagesMarx - Trabajo Asalariado y Capital PDFJoaquin RomeroNo ratings yet
- Matriz RamDocument59 pagesMatriz RamEdwin RamírezNo ratings yet
- Entrevista Con Un Médico Especialista en Herbolaria y Terapias Alternativas.Document7 pagesEntrevista Con Un Médico Especialista en Herbolaria y Terapias Alternativas.Leo DuMeNo ratings yet
- Informacion Ingredientes Cosméticos 1Document16 pagesInformacion Ingredientes Cosméticos 1Gabriela MorónNo ratings yet
- Memoria Descriptiva Arquitectura San IsidroDocument9 pagesMemoria Descriptiva Arquitectura San IsidroRicardo Liñan BlasNo ratings yet
- Clase 01 SimulacionDocument38 pagesClase 01 SimulacionBRENDA MITZI GARCIA JANCACHAGUANo ratings yet
- Evaluación de Filosofía de AristótelesDocument2 pagesEvaluación de Filosofía de AristótelesIrving Herney Pinzòn Tapias100% (1)
- Conexiones o Apoyos Estructuras ImportanteDocument25 pagesConexiones o Apoyos Estructuras ImportantegeosnovaNo ratings yet
- 9852 2920 56a Service Manual MT6020 (MK II)Document212 pages9852 2920 56a Service Manual MT6020 (MK II)Osvaldo Donoso Torres100% (1)
- Edificando El TemploDocument2 pagesEdificando El TemploAngeloAlexisNo ratings yet
- Conservacion de Ecosistemas y Respeto A Las Comunidades Locales Respecto A La Construcción Del Tren Maya Durante El Sexenio de Andrés Manuel López ObradorDocument23 pagesConservacion de Ecosistemas y Respeto A Las Comunidades Locales Respecto A La Construcción Del Tren Maya Durante El Sexenio de Andrés Manuel López ObradorHannia VainillaNo ratings yet
- Estimación de Edad FetalDocument10 pagesEstimación de Edad Fetalgiuseppeperoni PichardoNo ratings yet
- Especialidad EVADocument11 pagesEspecialidad EVAJosé DanielNo ratings yet
- Norma Inst. Eléctricas CablesDocument5 pagesNorma Inst. Eléctricas CablesLourdes Rocamora NadalNo ratings yet
- Dokumen - Tips - Guia Diagramas de Cortante y MomentoDocument21 pagesDokumen - Tips - Guia Diagramas de Cortante y MomentoCold SlugNo ratings yet
- Torta de Cumpleaños Blondies (Funfetti Blondies) - Cloudy KitchenDocument1 pageTorta de Cumpleaños Blondies (Funfetti Blondies) - Cloudy KitchenLUCIANo ratings yet
- Anexos, ConjuntivaDocument29 pagesAnexos, ConjuntivaMaryRuizNo ratings yet
- Vida Prodigiosa Del Ángel de Las EscuelasDocument473 pagesVida Prodigiosa Del Ángel de Las EscuelasCristiang_grcNo ratings yet
- Problemas Resueltos RadiactividadDocument4 pagesProblemas Resueltos Radiactividadsborgo92100% (1)
- Guía de PracticasDocument28 pagesGuía de PracticasPablo LuchoNo ratings yet
- Congreso Andasco 2018: Servicios públicos, TIC y tendenciasDocument4 pagesCongreso Andasco 2018: Servicios públicos, TIC y tendenciasJesusNo ratings yet
- TallerDocument2 pagesTallerVictor FlorezNo ratings yet
- NIC 36 Parrafos 12-23Document17 pagesNIC 36 Parrafos 12-23Angel TipismanaNo ratings yet
- Plagas y su control en granos almacenadosDocument16 pagesPlagas y su control en granos almacenadosCarlosEnriqueMurilloOcampoNo ratings yet
- REFRIGERACIÓNDocument13 pagesREFRIGERACIÓNAnnyEnmaVaRgasNo ratings yet
- 20 Abril 2021: 1.-Datos Generales de La Operación/Acción FormativaDocument1 page20 Abril 2021: 1.-Datos Generales de La Operación/Acción FormativaVíctor Martín PérezNo ratings yet
- Actividades de GeografíaDocument10 pagesActividades de GeografíaMaría José Martínez GálvezNo ratings yet
- A Propósito de Un Caso de Neurosis ObsesivaDocument9 pagesA Propósito de Un Caso de Neurosis ObsesivaAle PsicoNo ratings yet
- 1er Parcial CIV202Document3 pages1er Parcial CIV202Alexandra TiconaNo ratings yet