Professional Documents
Culture Documents
Resumo Bioquímica Urinário Oficial
Uploaded by
Igor LovegoodCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Resumo Bioquímica Urinário Oficial
Uploaded by
Igor LovegoodCopyright:
Available Formats
Resumo de Bioquímica do Sistema Urinário
Formação da Urina: Filtração, reabsorção, secreção e excreção.
Acoplamento do transporte ao metabolismo
Controle Renal do Equilíbrio Ácido-Base
Marcadores da Função Renal
Procedimentos Analíticos
Alterações Bioquímicas na Insuficiência. Renal
(Larissa)
O Sistema Urinário recebe cerca de 20 a 25 % do débito cardíaco (volume de ejeção do coração). Isso
porque são órgãos fundamentais para homeostase, e sua função depende justamente dessa grande chegada de
sangue. A principal função do rim é a excreção de resíduos, além da regulação do volume do líquido extracelular
e da pressão sanguínea, trabalhando e conjunto com o sistema circulatório. Ademais os rins fazem uma
sociedade de funcionamento com o comportamento, quando precisamos manter o equilíbrio iônico e a
osmolaridade, por exemplo acionando o comportamento da sede, que é quando temos um filtrado muito
concentrado, podendo assim diluir esse líquido, mantendo a osmalaridade em seus níveis normais. Os rins
controlam também o ph e produzem hormônios, como a eritropoietina, calcitriol. Fazem também a
gliconeogênese, principalmente em situação de jejum muito prolongado, podendo transformar o lactato em
glicose. Sintetizam peptídeos em aminoácidos. Regulam também a saturação de seus fosfolipídeos, regulando a
fluidez da membrana, para um bom funcionamento das proteínas transportadoras.
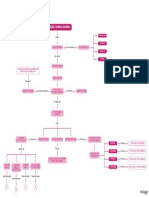
1. Formação da Urina: Filtração, reabsorção, secreção e excreção.
No esquema que mostra o trajeto tanto do filtrado quanto do sangue, as direções de reabsorção e
secreção. Tem-se o sangue chegando através da arteríola aferente e por pressão de filtração, parte do plasma
passa para dentro da cavidade da cápsula de Bowman. Quando ocorre a filtração, 100% de sangue que entra
pela arteríola aferente, apenas 20% será filtrado e será processado ao longo dos segmentos tubulares, sendo
que 19% serão reabsorvidos e 1% excretados.
O que determina, bioquimicamente, que a filtração aconteça de forma seletiva? Temos o epitélio da
cápsula de Bowman fundido com o endotélio dos capilares glomerulares, e esse epitélio é formado por células
especiais que são chamadas de podócitos; esses podócitos tem prolongamentos citoplasmáticos que são
chamados de pedicelos, entre cada pedicelo fica um espaço onde se tem poros da fenda, que são fendas que
ficam presentes entre cada pedicelo. Na região que está aparentemente vazia tem-se proteínas especiais que
formam uma estrutura que chamamos de diafragma da fenda. Além disso, temos uma membrana basal com
carga negativa, e os poros do endotélio que serão compostos por proteínas com carga negativa.
Na apresentação de glomérulo numa micrografia eletrônica e fizermos um corte transversal, conseguimos
observar estruturas como vasos capilares glomerulares em que no meio tem-se uma estrutura chamada de
mesângio, com células mesangiais. O mesângio é “tipo um cimento” caracterizado por dar sustentação e forma
para o glomérulo, além de ter algumas funções especiais dadas pelas suas células mesangiais: funções fagocíticas
e contráteis, essas funções fagociticas permitem que o mesângio seja limpo de material que seja extravasado
durante a filtração; possuem também receptores para hormônios vasoativos, permitindo sua capacidade de
contração; elas sintetizam matriz extra celular; sintetizam também citocinas inflamatórias e fibrogênicas, em
que essa capacidade está relacionada com alguns processos da patogênese renal.
Ampliando a região, temos os pedicelos, o espaço entre eles tem um “risquinho” que seria o diafragma
da fenda, que é onde ficam as proteínas importantes que estão envolvidas na seletividade da filtração. Temos
Medicina UFPA D 2015 – Urinário
primeiro a membrana basal glomerular, que tem a lâmina rara externa e interna, uma série de proteínas
carregadas negativamente e o papilar glomerular com suas fenestras, também com proteínas carregadas
negativamente, o que vai repelir outras moléculas que possuam a mesma carga. Os poros do endotélio,
lipoproteínas poli-hormônicas presentes nessa região, sendo que nesse endotélio nós vamos ter proteínas
entrelaçadas e o espaço entre essas proteínas é que vai ser caracterizado como um poro.
Têm-se as proteínas envolvidas na formação desse diafragma da fenda, com um complexo sistema
bioquímico que dá estrutura, por isso que o estudo dessas proteínas é de extrema importância, pois existem
doenças que são em decorrência justamente dessa perda de estrutura adequada, como a proteinúria finlandeza.
Essa doença se deu em uma família na Finlândia, a qual se dava pela alteração em um gene que codificava a
nefrina.
Na membrana basal glomerular temos lamininas, que são de extrema importância para que possamos
conectar outras proteínas à integrina e o distroglicano ao citoesqueleto. Temos o citoesqueleto da célula, do
podócito, um citoesqueleto que se prolonga nos pedicelos com proteínas que ancoram a célula no lugar certo
da membrana basal. Temos a laminina, as proteínas conectoras e proteínas ligantes que estão presas no
citoesqueleto de actina, isso é o que segura o podócito na sua posição envolvendo os capilares glomerulares.
Além disso, existe o diafragma da fenda com algumas proteínas também conectoras que unem lateralmente os
dois pedicelos, que em micrografia enxergamos aqueles “risquinhos”, sendo que essas proteínas conectoras
estarão ligadas as proteínas ligantes, que por sua vez ancoram as proteínas conectoras no citoesqueleto de
actina da célula. Assim, mantendo-se a arquitetura dos podócitos em torno dos capilares glomerulares.
Falando dos poros que temos no endotélio, existe o modelo que chamado de heteroporoso, que é um
modelo matemático que busca explicar o que encontramos no filtrado a partir de como é a composição de poros
desse endotélio. Tal modelo prevê que o endotélio é composto de uma série de poros pequenos, permitindo a
passagem de moléculas pequenas, livremente, impedindo a passagem de moléculas maiores, e uma pequena
quantidade de poros gigantes que é o que explica uma pequena quantidade de proteínas no filtrado, que atinge
realmente o túbulo proximal.
O que determina a filtração glomerular em termos bioquímicos? Falamos desse conjunto de proteínas
que são importantes para manter a estrutura, então, dada essa estrutura formada bioquimicamente teremos
como maneira de filtração das molécula a sua carga elétrica e o seu tamanho, já que tem que enfrentar a barrira
de filtração que foi mostrada anteriormente. As moléculas carregadas negativamente tem menor filtrabilidade
negativa, devido a grande carga negativa que temos nas barreiras. Em relação ao tamanho, a medida que
aumenta o peso molecular diminui a sua filtrabilidade relativa, ou seja, o valor de filtrabilidade de 1 significa que
a substância é filtrada tão livremente quanto a água. Por exemplo, a albumina possui um peso molecular muito
alto, por isso tem uma filtrabilidade relativa de 5%, ou seja, é pobremente filtrada, além de ter carga negativa.
Temos o sangue chegando, o plasma sendo filtrado, passando pela cápsula de bowman, seguindo para o
túbulo proximal, o restante do plasma segue pela arteríola eferente e vai seguir então seu trajeto pelos capilares
periglomerulares para participar de processos de reabsorção e secreção ao longo dos segmentos tubulares. O
que vai mandar nesses processos de reabsorção? Células tubulares, o capilar peritubular e a luz do túbulo por
onde chega o filtrado. Têm-se vias paracelulares e vias transcelulares.
A via paracelular é a que está entre as células, ou seja, lateralmente. Temos várias proteínas que são
importantes para que se possa ter um grau de vedação apropriado nessa via paracelular. Junções oclusivas são
complexos protéicos que regulam a permeabilidade a íons, então pode-se aumentar ou diminuir a quantidade
dessas proteínas mexendo na permeabilidade, conferindo diferentes graus de vedação. Casos de
hipomagnesemia grave que são dadas pela ausência ou pela alteração de paracelina - proteína do grupo das
claudinas - que ta envolvida justamente com a reabsorção de magnésio.
Medicina UFPA D 2015 – Urinário
A via transcelular vai funcionar por proteínas transportadoras, responsável pelo transporte de íons, de
solutos que não vão conseguir passar através da membrana por simples difusão, por isso é precisando ter canais
ou proteínas transportadoras. Sempre na membrana basolateral vamos ter a presença da bomba Sódio-
Potássio-ATPase, responsável por transferir o sódio para fora da célula e o potássio para o interior da célula,
gerando um gradiente negativo dentro da célula. Outra consequência importante da Sódio-Potássio-ATPase
nessas regiões do epitélio transportador é que sempre vamos ter pouca concentração de sódio no interior
celular, isso significa que a entrada de sódio a partir do lúmen tubular vai ser feita de forma passiva, sem gasto
de energia, assim conseguindo transportar outras moléculas em associação com o sódio por transporte ativo
secundário, exemplo seriam a glicose, os aminoácidos. As proteínas do transporte ativo secundário possuem um
alto grau de especificidade, atuando em cima de substratos específicos. Com a reabsorção de sódio, lembrando
que a força bioquímica responsável por isso é a Sódio-Potássio-ATPase, a aguá por osmose vai junto, com isso
como está sendo tirada carga positiva do lúmen está aumentando seu potencial negativo, forçando a
consequente saída de cloreto por transporte passivo. Em relação a uréia que não tem carga, a simples
reabsorção de água vai fazer com que ela seja reabsorvida no segmento tubular que seja permeável a ela.
Túbulo Contorcido Proximal
O túbulo proximal é o primeiro segmento do néfron, em que nele teremos a reabsorção de quase
tudo, e a secreção de hidrogênio livre, ácidos orgânicos e bases. Por ser o primeiro segmento as substancias que
foram filtradas e precisam estar no sangue, serão reabsorvidas completamente, como a glicose, sendo o
segmento tubular com “mais trabalho”. As células condizem com o alto grau de trabalho dessa região, com
bordas em escova bem amplas, tendo-se uma maior área na região apical, com um maior número de
transportadores, intensificando-se o processo de reabsorção; além disso, existe um grande número de
mitocôndrias justamente para a produção de ATP; nessa região também vai ter a excreção de produtos finais do
metabolismo como sais biliares, catecolaminas, fármacos.
Temos no túbulo proximal transportadores sódio-glicose de dois tipos: sódio-glicose transportador 1 e 2
(SGLT). A diferença entre eles seria o local onde se inserem no túbulo. O transportador 2 está presente nas
porções iniciais do túbulo contorcido proximal e o 1 nas porções finais. O 1 tem baixa afinidade e alta capacidade,
enquanto que o 2 tem alta afinidade e baixa capacidade. Eles estão distribuídos assim justamente porque o que
tem baixa afinidade (1) tem maior capacidade de transporte da glicose, funcionando melhor em altas
concentrações de glicose, se fosse a de alta afinidade nessas porções iniciais iria passar muita glicose e logo a
proteína iria se saturar. Umas vez dentro da célula, a glicose passa para o sangue através de transportadores
específicos, que são canais de glicose.
Em relação aos aminoácidos teremos diferentes transportadores dependendo do tipo de aminoácido. Na
estrutura do aminoácido tem-se um carbono central, com um grupo carboxila ionizado, um grupo amino
ionizado, um hidrogênio e o radical ou cadeia lateral. Aminoácidos neutros terão uma cadeia lateral neutra,
tendo carbono e hidrogênio, carbono-hidrogenio-oxigênio.
Qual a diferença entre essas cadeias?
Carbono e hidrogênio são átomos com eletronegatividade semelhante, compartilhando de maneira igual
os elétrons que estão presentes em suas ligações covalentes, assim se temos uma cadeia lateral com carbono e
hidrogênio apenas temos um aminoácido apolar, mas se tivermos oxigênio teremos eletronegatividades
diferentes, com uma carga parcial negativa para o oxigênio.
Por causa das diferentes conformações dos aminoácidos eles precisam de transportadores diferentes.
Vemos que há transportadores neutros, dibásicos e dicarboxílicos. Quem impulsiona o transporte dos
aminoácidos é o sódio com a atividade da bomba de sódio-potássio-ATPase. Os aminoácidos também não
Medicina UFPA D 2015 – Urinário
passam passivamente, eles têm receptores específicos do lado basolateral para que haja a reabsorção. Os
aminoácidos com menor afinidade pelos seus substratos estarão na região tubular primária e os de maior
afinidade estarão na porção final, para que de novo possamos reabsorver a maior quantidade de aminoácidos
possível.
Em relação ao fosfato, temos transportadores de dois tipos: TNP2a e TNP2c. O fosfato também é
reabsorvido pela bomba de sódio-potássio-ATPase, só que essa reabsorção é dependente do PTH. O
transportador sofre endocitose quando não há a presença do PTH, ele some da superfície da membrana,
diminuindo a absorção de fosfato. O PTH regula tanto a expressão e a retirada do transportador de fosfato da
membrana apical. Acredita-se que o funcionamento tanto de TNP2a e de TNP2c seja o mesmo. Além disso, 80%
do fosfato filtrado é reabsorvido no túbulo proximal (TNP2a e TNP2c). A hipofosfatemia é um distúrbio comum
em pacientes com altos índices de PTH.
Em relação às proteínas, elas serão reabsorvidas em caveólas, que são depressões celulares recobertas
de proteínas específicas como a clatrina (CRC) e tem a presença da megalina e da cubulina, que vão ligar
proteínas, vitaminas e minerais filtradas dentro das calveólas, que por sua vez vira um endossomo e a partir daí
podemos degradar as proteínas para absorver os produtos da degradação, no caso de aminoácidos (pedações
menores que compõe as proteínas). É nesse processo também que a vitamina D é ativada, que é ligada por
megalinas e cubulinas, sendo endocitadas e transferidas para dentro da mitocôndria, que com a presença da 1-
alfa-hidroxilase converte o calcidiol em calcitriol. Então, o calcitriol já ativado/formado vai ser reabsorvido. Esse
é o processo renal de reabsorção de vitamina D.
Além disso, sabemos que o túbulo proximal ocorre gliconeogênese, o metabolismo de aminoácidos e
peptídeos como a glutamina, a prolina, a hidroxiprolina, glicina, serina, citrulina e alanina. Bem como, ocorrem
reações de biotransformação (tornam o substrato mais solúvel em água, ganham polaridade): fase I (hidrólise,
redução, oxidação - polarização) e fase II (conjuga com molécula polar); detoxificação e nefrotoxicidade, pois o
metabólito pode ser convertido em algo tóxico ao ganhar polaridade.
João Felipe
Alça de Henle
Na alça de Henle também ocorre processos de reabsorção e secreção, então, temos 3 porções que são
funcionalmente distintas: ramo descendente fino, ramo ascendente fino e ramo descendente espesso. No ramo
descendente fino, tem-se poucas mitocôndrias, o que indica baixa atividade metabólica, ou seja, primariamente
está ocorrendo a reabsorção de água, visto que na alça de Henle, 25% da água é absorvida; há grande expressão
de aquoporinas nesse ramo, o que fortalece o fator de reabsorção de água dessa porção. A medida que o filtrado
passa pelo ramo descendente ele vai perdendo água e o líquido tende a ficar mais
concentrado. Na ascendente fina e espessa, a célula muda, sendo que a
ascendente fina acaba atuando como a faixa de transição entre a descendente
fina e a ascendente espessa. Na porção do ramo ascendente espesso nota-se
aumento na concentração de mitocôndrias, bem como aumento de bordas em
escova, indicando alta atividade metabólica e também da concentração de
transportadores de superfície pela borda em escova; nessa região ocorre
reabsorção de sódio, cloreto, potássio, cálcio, bicarbonato, íon magnésio e
secreção de íon hidrogênio. É uma região de controle ácido básico ao passo que
secreto hidrogênio e reabsorve bicarbonato. Como pode ser visto na imagem, a
consequência de um transportador é a secreção de hidrogênio e do outro é a
reabsorção de sódio, dois cloreto e potássio.
Medicina UFPA D 2015 – Urinário
Transporte ativo secundário é aquele impulsionado pelo primário,
então a bomba de sódio-potássio-ATPase determina a ação do
transportador. Canais de vazamento de potássio são importantes pois
dentro da célula tenho muito potássio por causa da atividade da bomba,
logo ele acaba extravasando e a presença desse potássio cria um potencial
postivio no líquido tubular, favorecendo o transporte de íons carregados
positivamento pela via paracelular, ou seja, a eletropositividade pelo
vazamento de potássio e reabsorção de cloreto estimula a difusão de cálcio
e magnésio por via paracelular/difusão paracelular.
O que acontece então na região da alça de Henle?
Tem-se a reabsorção de sódio, cloreto, potássio, cálcio e magnésio.
Sendo que sódio, potássio e cloreto serão reabsorvidos principalmente pela proteína simportador chamada de
sódio-potássio-2-cloreto. Ela retira cloreto e potássio além do sódio, que está impulsionando o processo. A
tendência do potássio é não ficar dentro devido aos canais de extravasamento. Ele se difunde por diferença de
concentração. Esse retorno ocorre para deixar o potencial positivo, dado pelo vazamento constante de potássio
e pela reabsorção da carga negativa do cloreto, isso impulsiona o transporte paracelular de cargas positivas.
Túbulo Distal
O que muda entre os segmentos são os transportadores. No túbulo
distal, temos o nefrón distal, que é o conjunto de todos os segmentos do
túbulo distal, que se divide em duas porções: túbulo contorcido distal
inicial e o final. O tracejado na imagem separa a medula do córtex. A região
inicial é a do aparelho justaglomerular e após a parte final tem-se o
segmento conector, o ducto coletor cortical, o ducto coletor medular
externo e o ducto coletor medular interno. Cada um deles com diferentes
expressões para a reabsorção de substâncias.
O que chega no néfron distal? Apenas 10% do filtrado, visto que todo o resto já foi trabalhado nas porções
anteriores. Essa porção do túbulo está relacionada com alterações
quantitativas finais dos íons, é um ajuste fino do que já foi feito
maciçamente, ou seja, o que de íons ainda precisa ser reabsorvido
para manter a homeostase. Nessa região, temos as junções de
oclusão bem desenvolvidas, visto que oferecem um grau de
vedação bem maior para que possamos evitar uma retrodifusão
passiva, visto que o filtrado está bem mais diluído. Esse conjunto
de de segmentos trabalha para chegar a uma composição
hidroeletrolítica final da urina ideal para a situação metabólica do
organismo.
O que acontece na porção inicial do túbulo distal?
Medicina UFPA D 2015 – Urinário
- Ocorre a reabsorção (em menor escala) de sódio, cloreto, cálcio e íons magnésio. Bordas em escova mais
discretas, visto que a carga de reabsorção nessa região é menor. Mitocôndrias presentes também. O
cotransporte de sódio e cloreto é impulsionado pela sódio-potássio-ATPase. Esse segmento é impermeável à
água e à ureia, sendo chamado de segmento de diluição. Ocorre absorção de magnésio por canais específicos e
o que acontece com ele nessa região ainda não é certo (não há consenso). Mas, acredita-se que ele se liga à uma
proteína ligante ao magnésio, que transporta o íon para um contratransportador de sódio e magnésio para fazer
a reabsorção ou pra um magnésio-ATPase. Suspeita-se disso porque já sabe que nessa região o cálcio faz esse
processo, sendo divalente assim como o magnésio. O cálcio se liga à calbindina para ser reabsorvido. Essas 3
etapas: entrada do cálcio, ligação ao ligante e a chegada às proteínas que irão promover a reabsorção são
reguladas por PTH.
No ducto coletor, ainda no túbulo distal, tem-se diferentes populações celulares. Dois grupos celulares:
células principais e células intercaladas. As células intercaladas estão mais envolvidas no ajuste do pH (equilíbrio
ácido-base). As células principais estão relacionas com a reabsorção de cloreto de sódio e com secreção de
potássio.
Quais os mecanismos feitos nessa região?
Na membrana basal há a presença de canais de sódio e canais de potássio e a bomba de sódio-potássio
ATPase. Todos os segmentos o ducto coletor expressam aquaporinas e são sensíveis à ação do hormônio
antidiurético. O receptor de aldosterona está dentro da célula devido a seu caráter lipídico, diferente do
receptor de PTH que estava na superfície. Quando a aldosterona está ligada ao receptor, ela estimula uma
cascata de reações que culmina na ligação de proteínas que formam o canal de cálcio na membrana apical.
Como resultado disso, temos a reabsorção de sódio e a secreção de potássio. Na ausência da aldosterona, temos
a internalização desses canais, ou seja, eles são retirados da membrana para que a reabsorção de sódio e a
excreção de potássio diminua (papel da aldosterona).
Na célula intercalada, temos a secreção de hidrogênio e a reabsorção de potássio.
Todos os segmentos do ducto coletor vão expressar aquaporinas e são sensíveis a ação do ADH (diz se
vou poupar ou excretar aquela água, já que está no final do néfron).
No ducto coletor medular interno tem-se alguns processos finais de reabsorção de sódio, cloreto, água e
ureia (região permeável à ureia). Reabsorção de bicarbonato e secreção de hidrogênio. Essa parte é relacionada
com o controle ácido-básico. Bomba plutônica é a de maior capacidade de expressão de hidrogênio (ativada
energeticamente por transporte ativo primário). Transporte maciço de íons hidrogênios pelas células
intercaladas. Como já foi dito, é o local final de processamento da urina, em que é capaz de secretar íons H+
contra gradiente de concentração, tendo também papel fundamental na regulação ácido-base. Diferente da sua
porção cortical, a porção medular é permeável a ureia, ajudando a elevar a osmolaridade e contribuindo para
formar a urina. A permeabilidade à água é controlada pelo nível de ADH.
Medicina UFPA D 2015 – Urinário
Resuminho do que foi falado anteriormente quanto às porções e aos hormônios envolvidos:
Logo, a excreção é o resultado dessa equação. O
que é filtrado menos o que é absorvido mais o que é
secretado. Ou seja, eu posso filtrar, mas não
necessariamente o que é filtrado é excretado, pois
pode ser reabsorvido. Não necessariamente o que não
foi filtrado não vai ser excretado, pois pode ser
secretado. O que é realmente excretado na urina é o
cálculo da equação.
A tabela mostra os componentes que são filtrados, excretados e a taxa de sua porcentagem, dando
enfoque à creatinina que não é reabsorvida, pois tem que ser excretada, sendo utilizada como marcador de
função renal. Ocorre nesse processo como um todo uma eliminação rápida de produtos indesejáveis e também
o controle do volume e composição dos líquidos corporais.
2. Acoplamento do transporte ao metabolismo.
Todos os transportes citados precisam de energia. Então, o metabolismo das células é decisivo na
manutenção desse processo como um todo. Nos rins, temos uma alta taxa de consumo de oxigênio. Isso permite
a manutenção de funções de transporte e as funções metabólicas das células epiteliais tubulares. Pela anatomia
renal, nem todas as regiões recebem aporte suficiente de oxigênio, então algumas regiões do rim estão mais
direcionadas pra glicólise anaeróbica po causa do baixo suprimento do oxigênio. A capacidade de cada segmento
tubular em lidar com insultos anóxicos depende da sua capacidade de produzir ATP anaerobicamente. Sabe-se
que a regiçao medular possui menos aporte de oxigênio, justamente por causa da irrigação, então se há
diminuição da pressão sanguínea quem mais sofre é a região medular.
Lembrando a glicólise anaeróbica, temos que da glicose produz-se 2 moléculas de piruvato, que por sua
vez é reduzido ao lactato em condições de pouco oxigênio. Isso ocorre porque o NADH indica que houveram no
mínimo duas reações com perda de elétron (oxidação). Para formar NAD reduzido, precisa-se de NAD oxidado.
Em falta de oxigênio. O NADH é um cofator que atua carregando elétrons. Esse NAD na forma reduzida indica
Medicina UFPA D 2015 – Urinário
que houve reação com perda de elétrons. Esse processo ocorre na fase 2 da glicólise. A fase 1 é a de gasto de
ATP e a fase 2 é a fase de falhamento, com 4 ATP e para pagar o ATP gasto é que ocorre a reação de oxidação.
Na falta de oxigênio, ou seja, em condições anaeróbicas a glicólise para justamente na fase de falhamento.
Então,a redução do piruvato ao lactato e também há a reciclagem do NAD oxidado para evitar o gasto
desnecessário de energia pela glicólise.
1 molécula de glicose me dá 32 ATPs no mecanismo oxidativo e apenas 2 no metabolismo anaeróbico.
Temos regiões corticais investindo em metabolismo oxidativo (região do túbulo proximal com bastante aporte
sanguíneo). A região do túbulo contorcido distal é uma região cortical que recebe bastante oxigênio, mas não
tanto como o túbulo proximal, logo, vai se basear tanto em metabolismo oxidativo como em glicólise
anaeróbica.
A região medular vai depender muito da atividade de enzimas glicolíticas. Isso foi descoberto a partir de
um experimento em diferentes regiões tubulares. Foi monitorada a capacidade de produção de lactato de cada
um dos segmentos tubulares em duas situações: uma normal e outra com a exposição de antimicina A.
A antimicina A é um bloqueador da função oxidativa, ou seja, deixa a célula “pensar” que está sem
oxigênio para verificar como a célula iria responder em termos de produção de lactato (ativação de via
aneróbica). Então, o que foi encontrado? (observar gráfico acima).
No túbulo proximal, verifica-se ZERO (não faz glicólise anaeróbica nem em condições normais nem em
condições de ausência de oxigênio), ou seja, se houve parada de fluxo para essa região do túbulo proximal, a
região vai sofrer muito, visto que ela não tem condições de produzir ATP sem a presença de oxigênio.
Já as outras regiões apresentam respostas diferentes, todas elas com aumento da produção de lactato se
a reação oxidativa é inibida, sendo outras mais e outras menos, com destaque para a região medular interna,
que já possui uma alta produção de lactato mesmo em condições normais, visto que nessa região a chegada de
oxigênio é mais limitada.
Medicina UFPA D 2015 – Urinário
Quando temos o transporte transepitelial de sódio, temos
uma relação com a taxa de consumo de oxigênio. Uma relação linear
bem marcante, pois quando maior for a quantidade de sódio
absorvida, maior o consumo de oxigênio. Quanto maio o uso de
bomba de sódio-potássio-ATPase é maior o gasto de ATP, poranto
mais oxigênio será utilizado para essa síntese. Logo, a maior parte
do “trabalho renal” é dedicado ao transporte de sódio, observando-
se uma relação linear entre reabsorção de sódio e consumo de
oxigênio. 80% desse oxigênio vai ser usado para o transporte de
sódio e 20% vai ser usado para o metabolismo basal. Isso relaciona
o papel da célula renal em ativar a produção de ATP ou não.
Existem gatilhos, moléculas que funcionam como
sinalizadoras. Como descobriram quais moléculas são importantes
nesse processo de sinalização? A partir da inibição dessas moléculas
para ver o que acontece. Foi inibida a bomba de sódio-potássio-ATPase com a oubaína (inibidora específica
dessa bomba). Obtiveram os seguintes resultados: quantidade de ATP não foi alterada, os níveis de ADP
diminuíram 20%, Qoxigênio foi inibido em 50% e a razão de NADH/NAD+ aumentou.
Conclusão: relação ATP/ATP e relação de NAD oxidado e NAD reduzido é o que vai impulsionar as
mitocôndrias das células renais em ativar a produção de ATP ou não. Isso não é uma exclusividade das células
renais, visto que o ATP é importante para verificar o nível energético das células do organismo. A célula vai
trabalhar pra manter o nível de ATP alto em relação ao nível de ADP, e quando ADP começa a aumentar e ATP
diminuir, todas as vias metabólicas relacionadas com a produção de ATP são ativadas e o processo se inverte e
isso é possível devido às enzimas regulatórias nessas vias que são moduladas por ATP (modulador alostérico).
Isso favorece a resposta imediatada nessas vias quando tem diminuição da carga energética nas células. Na
mitocôndria das células renais, quando percebe que há aumento de ADP ela vai intensificar a produção de ATP
pela via da fosforilação oxidativa mitocondrial.
Aula 2
CONTROLE RENAL DO EQUILÍBRIO ÁCIDO-BASE E MARCADORES DA FUNÇÃO RENAL
(João Victor)
CONTROLE RENAL DO EQUILÍBRIO ÁCIDO-BASE
Relembrando alguns conceitos da química:
Ácidos: moléculas ou íons que podem liberar H+.
Bases: moléculas ou íons que podem receber H+.
Proteínas carregadas negativamente podem receber H+, ou seja, agem como bases e agentes tamponantes.
Alcalose: remoção de íons H+ dos líquidos corporais.
Acidose: adição de H+ aos líquidos corporais.
Concentração de H+ é expressa na forma de logaritmo pH.
A diferença de uma substância ácida para uma solução ácida é que substância ácida são moléculas ou íons que
podem liberar H+ em solução e solução ácida é uma solução com muito H+ livre.
Substancias ácidas ou básicas fracas podem agir como agentes tamponantes, exemplificando quando se tem um
ácido fraco em solução, ele libera sua base conjugada e H+, então se jogarem um ácido forte nessa solução, esse
H+ extra se ligará a base conjugada, impedindo uma variação do pH.
O pH do líquido extracelular varia entre 7,38 e 7,42.
Medicina UFPA D 2015 – Urinário
Variações do pH não são boas para o organismo, uma vez que proteínas desnaturam graças à mudança de carga
dos aminoácidos que compõem as proteínas e todas as interações que formam a estrutura tridimensional da
proteína serão rompidas, perdendo sua função.
Balanço do íon H+ no organismo
Para que se tenha um balanço do H+ no corpo, se dever ter um equilíbrio entre ingestão e produção desse íon
associado a sua remoção líquida, e essa remoção líquida dos íons H+ é função renal. Ademais, existem outros
sistemas que ajudam na manutenção do pH como sistemas tampão e a compensação pulmonar, que se livram
de H+ com mais rapidez que os rins.
O nosso organismo tende a produzir excesso de H+ , por isso, existem todas essas formas de estabilização do
pH.
Produção diária de ácidos
Existe uma produção de ácidos enorme diariamente, e eles são divididos em ácidos voláteis e ácidos não voláteis.
Ácidos voláteis: CO² gasoso (eliminação pulmonar)
São gerados pela oxidação de moléculas nutrientes, o resultado da respiração celular, se ele não fosse exalado
pelos pulmões, a reação: CO² + H²O = H²CO³ = H+ + HCO³- , tenderia para extrema direita, culminando na
produção de H+ e na diminuição do pH. E graças à eliminação pelos pulmões a reação desloca para extrema
esquerda, não tem acumulo de H+ livre. Em condições normais, esses ácidos não causam impactos sobre o
balanço ácido-básico.
Ácidos não voláteis: eliminação renal
Gerados a partir de aminoácidos:
Cisteína e Metionina (S) Ácido sulfúrico
Lisina e Arginina Ácido hidroclorídrico
Gerados a partir de ácidos nucléicos e fosfoproteínas Ácido fosfórico
Ácidos orgânicos Ácido láctico e cetoácidos
É importante dizer que esses ácidos são formados pelo metabolismo, porém eles não chegaram ao rim nessa
forma, uma vez que eles são tamponados, instantaneamente, consumindo bicarbonato (HCO³-), base conjugada,
e indiretamente deixa prótons livres, além de excretar, esses ácidos, os rins irão repor o bicarbonato perdido.
(Beatriz Moraes)
Assim que eu gero um ácido no organismo ele precisa ser tamponado. Só que quando ele é tamponado ele tá
consumindo bicarbonato, que é o principal tampão do sangue. Se ele consome bicarbonato é a mesma coisa
dele estar adicionando prótons livres, entende? Então, gerou ácido sulfúrico, ácido clorídrico, fosfórico, lático e
cetoácidos. Acha que eles vão aparecer assim, dessa forma lá no FG? Não, porque no momento em que eles são
produzidos eles são neutralizados, tamponados pelo bicarbonato. Se é o bicarbonato que tampona, há consumo
de bicarbonato à medida que é produzido ácidos metabólicos. Se eu tiro bicarbonato de circulação eu deixo
prótons livres, porque eu não tenho o bicarbonato para formar ácido carbônico e estabilizar o pH, certo? Então
os rins vão ter o papel de repor o bicarbonato que foi consumido pelo tamponamento desses ácidos
metabólicos. Vejam que disso aqui a gente tem 80 mEq sendo gerados diariamente pelo metabolismo dessas
moléculas.
Quais são nossas defesas para mudanças no pH? Para lidar com toda essa série de ácidos? Então nós temos
primeiro o sistema de tampão, que vai neutralizar os ácidos imediatamente. Tem o centro respiratório que age
com um pouquinho mais de tempo, por causa da taxa de ventilação pulmonar e toda a regulação que tem que
ser feita em nível de bulbo pra que haja um controle dessa respiração. E os rins, que leva um pouquinho mais
de tempo porque envolve ativação de enzimas. Então a gente tem as duas primeiras linhas de defesa evitando
que a concentração se altere muito, até a resposta mais lenta da terceira linha que vão conseguir realizar a
compensação ácida-base necessária.
Temos aqui a resposta temporal de tamponamento, para diferentes tipos de defesa: tampões químicos,
pulmões e rins. E aqui o tempo após a carga ácida. Vejam que primeiro vai acontecer os tampões químicos,
Medicina UFPA D 2015 – Urinário
seguidos dos pulmões, e posteriormente dos rins, que é mais lenta porém mais contínua, relacionada com a
ativação de enzimas. A gente tem enzimas que são induzidas para gerar mais tampões e com isso favorecer o
retorno de mais bicarbonato pro sangue. Esse retorno de mais bicarbonato faz com que os prótons que estão
sendo gerados em excesso possam ser neutralizados.
O que são os sistemas tampão? São formados por substâncias capazes de se ligar de forma reversível com os
íons hidrogênio, evitando alterações excessivas de pH. Então eu vou ter um sal ou uma base correspondente e
um ácido fraco. Eu tenho as mesmas concentrações da forma livre de tampão, e da forma complexada. Então
se eu adiciono numa solução que tem concentrações equimolares de ácido e base conjugados, o que que vai
acontecer? Se eu adicionar aqui uma base, essa base vai ser neutralizada por esse próton, que é liberado de
uma substância ácida do tampão. Se eu coloco um íons hidrogênio, esse íon se liga a forma livre do tampão
convertendo essa forma aqui nessa (isso devia ser uma imagem). Então a efetividade de um tampão também tá
relacionada com a sua concentração, quanto mais tampão eu tiver presente, maior a sua capacidade de
tamponamento. Porque imagina que se eu ficar adicionando continuamente prótons em uma solução que tem
tampão eu vou acabar transformando toda essa forma de tampão nessa outra, e vai chegar o momento que ele
não vai ter mais capacidade de tirar hidrogênios livres de solução. Porque a forma que ligava hidrogênio já foi
toda consumida, complexada.
Aqui a gente um experimento com cão, e um com água não tamponada. E aqui a gente tem adição de volumes
de ácido clorídrico. Vejam que quando não temos o sistema de tamponamento o pH cai abruptamente e
indefinidamente a medida que vai sendo adicionado mais Hcl. Já com o cão a gente tem uma estabilidade do
pH, porque no organismo a gente tem um sistema tampão que vai lidar com esse hidrogênio que ta sendo
adicionado no sistema. (gente eu só conseguir entender cão, então acho que é)
Então a gente tem o sistema tampão bicarbonato como quantitativamente mais importante do líquido
extracelular, apesar de ele ter o pKa de 6,1. O que é o pka? K é constante de equilíbrio. É o pH em que a gente
tem concentrações equimolares das duas formas dos tampões. Isso significa que o pka de 6,1 eu tenho a
capacidade de tamponamento máxima do sistema tampão bicarbonato. Mas vocês podem perguntar “mas a
gente não tem o pH do liquido extracelular em torno de 7,4? Por que que ele é mais importante? Não seria
melhor ter um tampão mais aproximado de 7,4?”. Ele é tão importante assim porque quantitativamente a gente
tem muito bicarbonato no sangue, pela presença constante de CO2. Então eu tenho muita concentração desse
tampão apesar de ele ter um pka mais baixo. Assim, essa quantidade faz dele mais efetivo. Então se eu tenho
um aumento de Co2, que é o que tá continuamente acontecendo no nosso organismo, eu vou ter a formação
de ácido carbônico, e a dissociação fraca desse ácido em H+ e bicarbonato, porque o acido carbônico é um ácido
fraco, então ele se dissocia fracamente em próton livre e bicarbonato. Claro que terá o controle pulmonar da
eliminação e excreção do CO2.
Então o que acontece no líquido extracelular se a gente adicionar cargas de ácido, de próntons livres e eu tenho
esse sistema tampão bicarbonato? Aumento de prótons livre formação de ácido carbônico aumento de
CO2 eliminação desse excesso de CO2 pelos pulmões. Se a gente tem uma base sendo adicionada, a base vai
roubar um hidrogênio do acido carbônico e vai formar bicarbonato de sódio e água, e esse excesso de
bicarbonato vai ser eliminado pelos rins. Nas duas situações eu não vou ter alteração de pH, por causa dos
tampões realizados tanto pela presença do ácido carbônico quanto pelo bicarbonato.
Bom, também há o sistema tampão fosfato, que é extremamente importante no organismo. Mas ele vai ser
importante não pra tamponar o líquido extracelular, mas sim pro líquido tubular e também do líquido
intracelular. Então o liquido tubular renal vai poder se apropriar da presença de fosfato no líquido tubular, e
esse fosfato na forma de ácido fosfórico vai poder capturar hidrogênios livres no liquido tubular fazendo com
que seja possível ele excretar uma quantidade maior de prótons, porque não podemos excretar os prótons livres
na urina, porque acidificaria demais a urina. Nesse saco eu teria que eliminar uma quantidade muito grande de
água pra eu conseguisse excretar a urina na faixa de pH ideal, em torno de 4,5 a 5. Então eu uso os tampões,
ligo o hidrogênio que tem que ser excretado e pode ser eliminado sem mexer no pH da urina. O fosfato é
importante nesse processo mas a gente vai falar da amônia também.
Então é importante porque eu posso ter uma alta concentração de fosfato no líquido tubular, eu posso regular
e diminuir a reabsorção de fosfato, deixar mais fosfato no liquido tubular pra que ele possa servir de tampão
em condições de acidose. O líquido tubular tem um pH mais próximo do tampão, veja que o pka desse tampão
é um pouquinho mais alto que o tampão bicarbonato. Aí o que que vai acontecer nesse processo? Mesmo
Medicina UFPA D 2015 – Urinário
raciocínio anterior. Se eu adiciono acido clorídrico eu vou ter a formação de dihidrogênio-fosfato, a partir do
monohigrogênio-fosfato. O dihidrogênio-fosfato pode ser um doador de prótons. O monohidrogenio-fosfato
pode ser um receptor de prótons livres. Dessa forma esse hidrogênio pode ser excretado, não na forma livre. Se
eu adiciono uma base, eu vou roubar um próton desse dihidrogenio-fosfato, vou formar água e formo o
monohidrogenio-fosfato. Sendo assim, eu não mexo nos prótons da solução, não alterando pH, ele vai ser
neutralizado pelo próton do dihidrogenio-fosfato.
Pergunta: o que é a base conjugada e o ácido conjugado?
Resposta: o ácido eu tenho potencial de liberar hidrogênio, a base eu tenho potencial de receber hidrogênio.
Então nessa situação aqui eu tenho uma molécula com potencial de hidrogênio, então ela vai receber o
hidrogênio e formar o dihidrogenio-fosfato. Esse hidrogênio que foi adicionado em solução não vai permanecer
livre. No liquido tubular eu vou ter concentrações equimolares da forma mono e dihidrogenio-fosfato. Uma
forma pode ser convertida na outra, dependendo da necessidade. Se há adição de prótons, eles se ligaram à
forma mono, se há necessidade de prótons (quando há adição de uma base) a forma dihidrogenio-fosfato doa
prótons ao líquido. A explicação tá sendo focada nos prótons. Se há adição de uma base, o dihidrogenio-fosfato
vai doar um próton, virando monohidrogenio-fosfato, e a ligação desse hidrogênio liberado com a hidroxila
forma água. O pH não se altera porque o tampão neutralizou essa base.
Alem disso, temos proteínas agindo como tamponantes, e uma proteína muito importante nesse processo é a
hemoglobina. Então, a hemoglobina se liga a prótons livres formando uma hemoglobina protonada. Então, se
eu tenho no plasma um aumento da concentração de CO2, e a célula sanguínea ta presente nesse plasma, esse
CO2 consegue se difundir pela membrana do eritrócito, vai formar ácido carbônico pela ação de uma enzima
chamada anidrase carbônica (essa formação de acido carbônico pode acontecer espontaneamente, mas ela é
lenta). A anidrase pega esse CO2 que se difundiu do liquido extracelular pra dentro do eritrócito, faz com que
reaja com a água formando o acido carbônico, e esse acido se dissocia em hidrogênio livre e bicarbonato. Esse
hidrogênio livre se liga à Hb, que é uma proteína negativa, então ela se estabiliza. O que acontece com o
bicarbonato? Eu tenho aqui um trocador, e ai entra cloreto pra hemácia e o bicarbonato vai pro sangue. Além
de eu tirar prótons livres do plasma eu ainda dou bicarbonato, o que equivale a uma retirada dupla de hidrogênio
de líquido extracelular, então é um tamponamento extremamente importante. 60 a 70% do tamponamento vai
ser feito dessa maneira.
(Comentário do mangaba) O nosso sangue é alcalino graças ao sistema de tampão que a gente tem, porque se
não seria muito ácido, porque produzimos muito ácido. Então eu vou ter sistemas tampão circulante, de células
circulantes, para evitar que esse hidrogênio fique livre, porque as nossas proteínas extracelulares funcionam
bem no pH de 7,4. E lembrem, esse cara é uma logarítmica, se eu passo de 7,4 pra 7,3, é muito hidrogênio que
eu to retirando de solução.
Temos o centro respiratório, que só pra lembrar. O CO2 produzido nas células vai ter eliminação pulmonar, se
eu aumento a ventilação pulmonar eu aumento a eliminação de CO2, e se eu diminuo, eu diminuo a eliminação
de CO2. E quando a gente vai ver o equilíbrio dessa reação, a medida que eu começo a aumentar a concentração
de CO2, que eu não elimino pelos pulmões, eu vou deslocar a reação pra cá e eu vou ter acidificação do liquido
extracelular. Por isso que é tão importante manter essa taxa de ventilação coerente com o nível de CO2 que ta
sendo produzido no organismo. A própria pressão de CO2 vai fazer com que haja um aumento da ventilação, a
gente tem um controle disso na região do bulbo. Por exemplo, eu tenho uma taxa de ventilação normal, e assim
eu não tenho uma alteração de pH nos líquidos corporais. Se eu começo a aumentar a intensidade da ventilação,
eu tenho alteração do pH dos líquidos corporais, ou seja, aumenta o pH, porque há maior eliminação de CO2.
Se eu começo a hipoventilar eu diminuo o pH, pois terá mais Co2 em circulação e a reação vai estar favorecida
para esse lado.
Chegamos nos rins. Os rins podem fazer regulação do equilíbrio acido-base ao excretar a urina ácida ou básica
dependendo das alterações do líquido extracelular. Além disso, eles tem a capacidade de repor bicarbonato pro
sangue, repor o que foi consumido no tamponamento dos ácidos produzidos pelo organismo. Então, quando eu
produzo o filtrado glomerular o bicarbonato passa livremente. Então se eu não reabsorvo esse bicarbonato, eu
vou estar diminuindo o pH, vai haver uma perda de base do sangue.se eu tiver um aumento da excreção de
prótons, terá uma perda de ácidos. Então, assim se consegue controlar o equilíbrio. Então, há recuperação de
todo bicarbonato filtrado, voltando aos capilares peritubulares e corrente sanguínea, associada a essa
recuperação eu tenho a secreção de prótons. Pra cada bicarbonato recuperado um próton é secretado, e ainda
Medicina UFPA D 2015 – Urinário
eu consigo excretar a carga diário de acido volátil (acho que foi isso que ela falou). Isso vai acontecer por
reabsorção de bicarbonato, secreção de prótons e produção de novo bicarbonato. Lembrando que quando eu
produzo ou simplesmente coloco de volta o bicarbonado filtrado é a mesma coisa que tirar prótons de solução,
porque o bicarbonato é sítio de ligação pra esses prótons livres.
Onde vai ocorrer a reabsorção de bicarbonato e secreção de hidrogênio? Basicamente em todas as partes do
nefron. Mas em maior quantidade no túbulo contorcido proximal. Isso porque é extremamente importante que
esse bicarbonato volte rapidamente pro sangue. A concentração plasmática de bicarbonato é aproximadamente
24 mEq/L. Se eu tenho uma faixa de filtração glomerular em torno de 180 L/dia, sendo 4320 mEq/dia sendo
filtrados, passando do sangue para o liquido tubular. Eu preciso delinear tudo isso, como? Pra cada bicarbonato
absorvido, um próton é secretado. Lembra que eu disse que a gente tem 80mEq de ácidos não voláteis sendo
produzidos por dia, então se pra cada bicarbonato que é absorvido eu secreto um hidrogênio, eu vou ter que
secretar tudo isso de hidrogênio pra conseguir reabsorver todo o bicarbonato que foi secretado e ai eu vou ter
que secretar mais os hidrogênios relacionados aos prótons produzidos pela produção dos ácidos não voláteis.
Então por dia eu secreto cerca de 4400 mEq de prótons nos rins. Resumindo: pra eliminar todo o bicarbonato
eu preciso eliminar a mesma quantidade de hidrogênio, e também eliminar os prótons produzidos pela liberação
de ácidos não voláteis, que são 80 mEq. Somando tudo isso, dá 4400 mEq de prótons sendo secretados
diariamente.
Então temos transportadores relacionados com diferentes porções tubulares. O que acontece? Tá vindo lá no
rim tubular bicarbonato que foi filtrado e ele tem que entrar aqui de novo, só que a gente não tem
transportadores de bicarbonato pra dentro da célula, então ele entra de uma maneira indireta. Aqui nessa
membrana, de borda em escova, tem a anidrase carbônica 4, a qual favorece a conversão do acido carbônico,
que é formado pela associação do bicarbonato presente no filtrado como próton que ta sendo bombeado aqui.
Por ação da anidrase 4 que ta presente na borda em escova nesse epitélio tubular eu vou ter a formação de CO2
e água a partir do acido carbônico. O CO2 vai se difundir pra dentro da célula epitelial tubular, e dentro dela vai
fazer o processo inverso, agora por ação da anidrase carbônica 2. O bicarbonato vai ser absorvido por um
cotransportador de sódio-bicarbonato e eu tenho a formação de um outro hidrogênio pra pescar outro
bicarbonato que ta passando. Ai se vê a importância de secretar a mesma quantidade de hidrogênio que a de
bicarbonato que tem que ser absorvido. Então transportadores envolvidos nesse processo: um trocador sódio-
hidrogenio (antiporte, transporte ativo secundário – sódio a favor do gradiente de concentração e hidrogênio
contra o gradiente de concentração). Outro importante é o sódio-bicarbonato. Nesse caso quem vai de carona
é o sódio, porque essa é um transportador eletrogênico, transporta 3 bicarbonatos pra um sódio, e eu tenho
essa região aqui mais positiva que essa. Ela vai favorecer a diminuição da concentração de sódio aqui dentro,
junto com a sódio/potássio ATPase. Então assim vai pescando o bicarbonato que vai passando pelo liquido
tubular.
(Ela explica tudo de novo porque poucos entenderam). Primeiro: a função dessa parte do tubo é reabsorver
bicarbonato. O CO2 que ta dentro da célula renal ou que é difundido do interstício renal, vai reagir com água
formando acido carbônico, reação catalisada pela anidrase carbônica 2, isoforma que esta presente dentro das
células epiteliais tubulares. (Fora é 4 e dentro é 2). Começando de dentro da célula, o CO2 se difunde do
interstício renal, vai reagir com a água por ação da anidrase carbônica 2, formando o acido carbônico. Este se
dissocia em próton livre e bicarbonato. Esse próton livre vai ser secretado através de um trocador sódio-
hidrogenio, ou um antiporte, ou um contratransportador, tudo a mesma coisa. Esse próton secretado no liquido
tubular vai ser ligar ao bicarbonato que foi filtrado, formando ácido carbônico fora da célula, no liquido tubular.
Esse ácido carbônico vai sofrer ação da anidrase carbônica 5 e se dissociar em CO2 e água. O CO2 se difunde pra
dentro da célula e vai formar de novo bicarbonato. E eu consigo então dessa forma reabsorver o bicarbonato,
de forma indireta. Pra isso eu preciso de excreção de hidrogênio, justamente pra formar acido carbônico.
Outra maneira de fazer reabsorção de bicarbonato e secreção de hidrogênio é mais adiante nos túbulos distais
finais e túbulos coletores por transporte ativo primário. Vejam que aqui em vez de eu ter aquele trocador sódio-
hidrogenio eu tenho uma bomba protônica, que tem uma capacidade muito maior de secretar hidrogênios. Se
nessas porção tubular eu ainda tiver bicarbonato passando, ou seja, eu ainda não consegui absorver tudo nas
porções iniciais do néfron, essa é uma outra forma de eu conseguir capturar esse bicarbonato. Se eu não tiver
mais bicarbonato passando esse hidrogênio vai ser tamponado com algum tampão do liquido tubular e vejam
que da mesma forma eu produzo bicarbonato.
Medicina UFPA D 2015 – Urinário
(Derek Newbery)
(PRIMEIRO SLIDE PG 13)
Observa-se novamente a presença de diversos transportadores
nas diferentes porções tubulares. No túbulo proximal, alça de
henle ascendente espessa e na porção inicial do túbulo distal,
há no líquido tubular certa quantidade de bicarbonato que foi
filtrado, este precisa ser reabsorvido, no entanto, não existem
transportadores de bicarbonato pra dentro da célula, então ele
entra de uma maneira indireta.
Então, como essa reabsorção ocorrerá? Primeiramente, o
lúmen tubular dessas porções apresenta uma anidrase
carbônica do tipo IV, a qual favorece a conversão do ácido
carbônico (H2CO3), formado pela associação do bicarbonato (
HCO3-1) presente no filtrado com o próton (H+) que está sendo secretado na borda em escova por meio
de um contra transportador Na+/H+ (H+ + HCO3-1 ↔ H2CO3), em CO2 e H2O. Em seguida, esse CO2 formado se
difunde para a célula epitelial tubular, onde fará o processo inverso por meio da ação da anidrase carbônica II,
que atuará formando novamente H2CO3 a partir de H2O e CO2. Então, o ácido carbônico formado se dissocia em
H+ e HCO3-1, este bicarbonato passará da célula epitelial para o interstício por meio de um cotransportador Na+/
HCO3-1. Desse modo, o H+ poderá ser secretado para o líquido tubular, o que reinicia o ciclo. Sendo importante
ressaltar, assim, que a reabsorção de bicarbonato está sempre acoplada a secreção de um H+.
Têm-se envolvido nesse processo os seguintes transportadores:
Um trocador Na+/H+ na membrana apical, o qual atua por mecanismo de transporte ativo secundário, pois
transporta H+ contra seu gradiente a partir do transporte de sódio a favor de seu gradiente de concentração;
Um cotransportador Na+/ HCO3-1, um transportador eletrogênico, em que na verdade o gradiente elétrico
bicarbonato proporciona a sua saída da célula e o sódio é, então, levado junto com ele;
Uma Na+/K+ ATPase na membrana basolateral, importante para manter o gradiente de sódio necessário
para o contra transporte pelo trocador Na+/H+.
(SEGUNDO SLIDE PG 13)
Nos túbulos distais finais e túbulos e ductos coletores, a secreção de H+ e reabsorção de bicarbonato é feita de
outra maneira. Nestes, ao invés de um trocador Na+/H+ a membrana apical apresenta um bomba iônica que atua
somente secretando H+ por transporte ativo primário. Da mesma forma, há também a produção de um íon
bicarbonato acoplada a secreção de H+.
Estas porções atuam reabsorvendo bicarbonato se ele ainda
estiver presente no líquido tubular, ou seja, se as porções
iniciais não conseguiram reabsorver todo o bicarbonato que
foi filtrado. Por outro lado, no caso de não haver mais
bicarbonato passando no líquido tubular nestas porções, o H+
secretado será tamponado com algum tampão do líquido
tubular, mas mesmo assim haverá a produção de um
bicarbonato, o qual será absorvido para o sangue. Ou seja,
mesmo que não haja sequestro de bicarbonato, há produção
deste no interior da célula, tem-se, portanto, o ganho líquido
de um bicarbonato, o qual será usado para tamponar ácidos
provenientes das vias metabólicas. É importante lembrar que os ácidos metabólicos produzidos por todo o corpo
não chegam até o rim, pelo fato de que são tamponados imediatamente, para tal consumem bicarbonato
Medicina UFPA D 2015 – Urinário
circulante no plasma. Então, o rim atua repondo esse bicarbonato e secretando hidrogênio, não exatamente
aquele H+ que foi formado pela produção do metabólito ácido.
-Alguem não entendeu então ela explicou novamente essa última parte:
Por exemplo, uma determinada via metabólica forma um ácido sulfúrico. Esse ácido sulfúrico vai ficar no sangue
circulando até chegar no rim para ser eliminado? Não. Por que não? Porque ele se dissocia antes, liberando H+,
o que baixa o Ph. Esse H+ livre liberado, vais ser, portanto, imediatamente tamponado pelo bicarbonato. A
liberação desse ácido consumiu um bicarbonato. Dessa forma, o rim atua compensando ao repor bicarbonato
para o plasma.
(TERCEIRO SLIDE PG 13)
Os túbulos distais finais e túbulos e ductos coletores apresentam células principais e células intercaladas, tais
mecanismos citados acima ocorrem nas células intercaladas. Estas possuem dois tipos: A e B. A do tipo A
apresenta em sua membrana apical uma bomba protônica que secreta H+ ativamente e uma H+/K+ ATPase. Há
também na membrana basolateral dessas células intercaladas do tipo A, trocadores HCO3-/ Cl-, um tipo de
trocador aniônico (Aniôn exchanger, por isso na imagem o nome é AE-1).
O mesmo processo que ocorre nos túbulos iniciais acontece nas células intercaladas do tipo A, ou seja, no líquido
tubular o HCO3- se liga ao H+ e forma H2CO3,
originando, em seguida, H2O e CO2, este
então se difunde para o interior da célula,
onde novamente ocorre interação com H2O
formando H2CO3, que logo se dissocia em
HCO3- e H+. O bicarbonato formado e levado
para o interstício pelo trocador HCO3-/ Cl- e
o H+ é secretado para o lúmen tubular por
meio da H+/K+ ATPase ou da bomba
secretora de H+.
Nestas regiões, é possível que seja formada
uma urina altamente ácida por conta da
presença dessas bombas. No entanto, o limite para essa acidificação é a presença de tampões urinários, pois o
H+ não pode circular livre nessa urina, precisa, portanto, ser tamponado.
As células intercaladas do tipo B são ativadas em casos de alcalose metabólica, pelo fato de serem uma imagem
especular das intercaladas tipo A, fazendo com que tenham funções opostas. Isso se explica pela presença da
bomba secretora de H+ na membrana basolateral e dos trocadores HCO3-/ Cl- na membrana apical das
intercaladas tipo B. Dessa forma, tem-se uma secreção de bicarbonato e absorção de H+. Ademais, as
intercaladas do tipo B são convertidas em tipo A quando há situações de acidose metabólica. Tal mudança se dá
pela inversão da localização dos transportadores.
(PRIMEIRO E SEGUNDO SLIDES PG 14)
Apenas cerca de 0,03 mEq/L de H+ pode ser excretado livre
na urina, essa quantidade máxima se justifica pelo fato de
que o pH da urina mínimo é de 4,5, então maiores
quantidades de H+ livre poderia tornar a urina mais ácida
que esse valor. Por dia, há uma produção de 80 mEq/L de
ácidos não voláteis, se essa quantidade fosse excretada na
forma livre seria necessário que o indivíduo produzisse
mais de 2 mil litros de urina para que o pH dessa fosse
mantido acima de 4,5. Então, o que como se faz o
tamponamento destes ácidos? Há um mecanismo de
formação de ácidos tituláveis. O que é um ácido titulável?
Tal nome se deve pelo fato de que o método para avaliação da quantidade de ácido excretado na urina se dá
por meio da titulação desta, em que se adiciona hidroxilas até que esta alcance o valor do pH sanguíneo, a
Medicina UFPA D 2015 – Urinário
quantidade de hidroxila que foi adicionada para tal corresponde a quantidade de ácido livre que essa urina
possui. O principal ácido titulável é o fosfato, mas sulfato e urato também são produzidos. Estes são responsáveis
pelo tamponamento de cerca de 30% do conteúdo de H+ no líquido tubular. O restante é tamponado por meio
do mecanismo de amoniogênese que pode ser aumentado nos casos de acidose, deferentemente do mecanismo
de ácidos tituláveis que tem uma produção fixa.
(TERCEIRO SLIDE PG 14)
Em relação ao mecanismo do tampão fosfato, percebemos ainda a secreção de H+ pelo contra transportador
H+/Na+ na membrana apical. Este então se ligará ao HPO4- presente no lúmen, formando H2PO4, que será
excretado na urina. Este H+ não estará mais livre para se ligar a bicarbonato e contribuir para sua reabsorção, o
que não permitirá o prosseguimento do ciclo de reabsorção de bicarbonato e secreção de H+. Além disso, como
não há ciclo, é importante lembrar que com a formação de H+ um HCO3- também é produzido, o que acarreta
na produção líquida de um HCO3-.
Essa produção de bicarbonato, novamente, é importante para a reposição daquelas que foram usados no
tamponamento de ácidos metabólicos. Conclui-se que sempre que o H+ se ligar a um tampão diferente do
bicarbonato, o efeito líquido é a adição de um novo bicarbonato no sangue.Mas por que se fala que é um
bicarbonato novo? Porque até aqui, estava ocorrendo uma ciclagem, em que o próton é bombeado com o intuito
de sequestrar o bicarbonato que estava passando no líquido tubular, era absorvido na forma de CO2 e o ciclo se
repetiria para o bicarbonato ser reabsorvido. Por outro lado, no mecanismo da produção de novo HCO3-, há o
bombeamento de hidrogênio e o bicarbonato formado pelo processo intracelular está sendo reabsorvido como
um ganho líquido, ele não tá saindo pelo lúmen tubular. Se a formação de novo bicarbonato não acontecesse,
todo o tampão HCO3- seria consumido para tamponar os ácidos metabólicos, então o rim atua compensando ao
repor tampão para o sangue.
(PRIMEIRO SLIDE PG 15)
Fosfato, urato e sulfato são capazes de tamponar de 30 a 40 mEq/dia de ácidos não voláteis, percebam, ó caros
leitores, que a conta não bate, já que por dia são produzidos 80 mEq destes. O restante, portanto, será
tamponado por meio do mecanismo de amoniogênese, por meio do qual é possível a produção de novo tampão.
Quando ocorre o aumento da concentração de H+ no líquido extracelular, há um aumento do metabolismo renal
da glutamina, um aminoácido produzido no fígado e metabolizado no túbulo proximal do néfron, formando,
assim, dois HCO3- e dois íons amônio (NH4+). Novamente, percebe-se uma produção líquida de íons bicarbonato.
A partir de então existem duas correntes de raciocínio.
(TERCEIRO SLIDE PG 15)
Primeiramente, de acordo com o guyton, o NH3, proveniente do metabolismo da glutamina, é secretado para o
lúmen tubular. Esta amônia se liga a H+ e forma amônio, o qual poderá ser excretado na forma de sal.
Medicina UFPA D 2015 – Urinário
(SEGUNDO SLIDE PG 15)
Por outro lado, outra corrente demonstra que, durante o
metabolismo da glutamina na mitocôndria da célula
proximal, tem-se a formação de amônio e de dois íons
bicarbonato.
Obs: tanto a glutamato desidrogenase quanto a
glutaminase, enzimas que atuam no metabolismo da
glutamina, terão sua expressão e atividade estimuladas pela
acidose.
(PRIMEIRO SLIDE PG 16)
Para compreender melhor como as duas correntes se relacionam, é importante o entendimento acerca do
trajeto que essa amônia segue. Primeiramente, o amônio é produzido no túbulo proximal e secretado por contra
transporte com íon sódio. Esse amônio segue até a região da alça de
henle ascendente espessa, onde será reabsorvido. O interstício se
encontra menos ácido, o que induz a dissociação de NH4+ em H+ e NH3.
Essa NH3 se difunde através da membrana e volta para o lúmen
tubular, onde será novamente reabsorvida na porção fina da alça de
henle, gerando, assim, uma alta concentração de amônia no
interstício da região medular. Essa NH3 concentrada, logo se difunde
para a região próxima aos ductos coletores para ser secretada. Em
seguida, ela se liga a H+ no líquido tubular, formando NH4+ . Conclui-se
que o guyton apenas demonstra a última parte desse ciclo, em que há
a secreção de amônia nos ductos coletores.
De acordo com esse ciclo, se vocês forem observadores, perceberão
que não há de fato uma excreção real de prótons, pelo fato de que a
amônia no ducto coletor apenas está se ligando a um H+, porém é
importante lembrar que anteriormente ela já havia liberado um H+ no interstício. Portanto, não há excreção
líquida de prótons.
(SLIDE 1 PG 17)
Então, qual a importância do amônio no equilíbrio ácido base? Esta se deve pelo fato de que se ele for
reabsorvido, será levado até o fígado, entrará no ciclo da uréia, a partir do qual há formação de dois H+ livres, o
que anularia a formação de dois bicarbonatos correspondente ao metabolismo renal da glutamina. Como íon
amônio é excretado, há um ganho líquido de dois bicarbonatos que contribuem para o tamponamento
sanguíneo. Dessa forma, percebe-se que uma corrente defende a importância da amoniogênese se deve pelo
tamponamento de ácidos não voláteis e pela produção de bicarbonato, enquanto que outra restringe seu papel
apenas à formação de íons bicarbonato.
(SLIDE 2 PG 17)
Em relação às desordens do equilíbrio ácido base, tem-se que a acidose é a que mais comumente acontece, pelo
fato de que, normalmente, há uma maior produção de ácidos do que bases em decorrências dos processos
metabólicos. Como que o rim reage a essas desordens? Primeiramente, há um estímulo à reabsorção de
bicarbonato e à secreção de prótons. Esse efeito ocorre por meio de um aumento da atividade de
transportadores Na+/H+ e da inserção exocitótica de estoques intracelulares de transportadores na membrana
plasmática, como bomba secretora de íons H+ e contra transportador Na+/H+. Sendo que tais efeitos são
evocados a partir de uma acidose intracelular. Em resposta a acidose pode haver aumento na aminiogênese
também, por uma maior atividade e expressão de enzimas responsáveis pelo metabolismo da glutamina.
Também pode haver uma maior disponibilidade de tampões urinários, em que, por exemplo, a reabsorção de
Medicina UFPA D 2015 – Urinário
fosfato diminui para que se tenha uma maior
disponibilidade dele no líquido tubular para tamponar
uma carga extra de prótons livres.
Além disso, questiona-se se pH gera todos esses efeitos
sozinho ou se há a participação de vias metabólicas
intracelulares a partir da percepção de uma maior
concentração de H+. Até o presente momento, acredita-
se que existe sim uma participação direta do pH, mas
existem também algumas moléculas que fazem
sinalização celular, tais como: endotelina, atua na
ativação de transportador Na+/H+ e de cotransportador
Na+/HCO3- na membrana basolateral, fazorecendo, assim,
uma maior reabsorção de bicarbonato e secreção de íons hidrogênio; cortisol, age também nos mesmos
transportadores aumentando suas concentrações. A amioniogenese é ativada tanto pelo cortisol quanto pela
diminuição do pH intracelular. Além disso, a reabsorção de fosfato é diminuída pelo hormônio PTH.
(Rafael Castro)
MARCADORES DA FUNÇÃO RENAL EM PROCEDIMENTOS ANALÍTICOS
Quais os tipos de moléculas, a partir do que conhecemos de reabsorção e excreção podem funcionar como
potentes marcadores de função renal? Moléculas que são 100% reabsorvidas são bons marcadores, pois se
aparecerem na urina indicam que algo está errado e moléculas que não são reabsorvidas, que são totalmente
excretadas, pois se aparecerem no sangue em maiores concentrações também indica que algo está errado.
Por exemplo, a creatinina ela não é reabsorvida, isso significa que a concentração dela na urina é alta e no sangue
é baixa, esta relação é o normal, se houver uma inversão dessa relação, é um indicativo que há algo de errado.
Ao contrário com as proteínas, é mais comum estar presente no sangue e pouca quantidade na urina, se houver
muita proteína na urina é um indicativo de alteração.
A avaliação de uma possível disfunção renal vai estar relacionada com o aumento da concentração plasmática
do que deveria ser excretado e a presença de elementos que não deveriam ser excretados na urina. O que deve
ser excretado na urina? Ureia e creatinina, essas moléculas devem estar em pouca concentração no sangue. Ao
contrário, proteína deve ter pouca concentração na urina.
Os principais marcadores de função renal são os compostos nitrogenados (alguns livros chamam esses
compostos de NNP - Nitrogênios Não Proteicos) e seus principais representantes são: ureia e creatinina. Estes
elementos têm uma baixa concentração plasmática e uma alta concentração urinária, quando esta relação se
inverte é indicativo de lesão renal.
Outro marcador de função renal é a proteinúria, presença de proteínas na urina, é um achado precoce, ou seja,
quando há presença de proteína na urina é um indício inicial de alteração na filtração glomerular, possui
tratamento e o prognóstico é bastante positivo.
Outros compostos nitrogenados, em algumas ocasiões, podem ser utilizados, como ácido úrico e amônia,
mas nunca sozinhos porque eles podem aumentar suas concentrações plasmáticas por outras vias que não estão
relacionadas com problemas renais. Por exemplo, alterações metabólicas e alimentares podem fazê-los
aumentar, mexendo na concentração plasmática de ácido úrico sem ter problema renal. Por isso estes
compostos devem ser avaliados com cautela e sempre associado com a creatinina.
1. UREIA
A ureia corresponde a 80% do nitrogênio urinário humano, ou seja, somos animais ureotélicos, nós excretamos
os compostos nitrogenados em forma de ureia, pois a amônia é tóxica para nós. Isto acontece devido não haver
uma reserva de aminoácidos. Por exemplo, existe uma reserva para carboidrato em forma de glicogênio e existe
Medicina UFPA D 2015 – Urinário
reserva de lipídeos em forma de triglicerídeos, entretanto, não há reserva para aminoácidos e se houver um
excesso de aminoácidos que o organismo não precisa para formar novas proteínas é necessário eliminá-los.
Então, se o aminoácido não tem uso para síntese de novas proteínas, se eu tenho muito aminoácido circulante
porque tenho uma dieta rica em proteínas e se tenho um jejum severo ou diabetes mal tratada, o excesso de
aminoácido precisa ser eliminado (exceto em caso de jejum severo e diabetes mal tratada, que as reservas de
glicose e ácidos graxos já foram utilizadas e o organismo usa as proteínas musculares constitutivas para produzir
energia).
Quando a gente degrada um aminoácido, é criado um problema, devido à saída do grupo amina da estrutura do
aminoácido, que é a amônia (NH3), uma base forte. Se esta amônia ficar livre ela irá roubar hidrogênio (H+), o
que levará uma mudança do pH e alteração de todo o sistema. A amônia é tóxica, o que gera a necessidade de
dar um fim a amônia rapidamente.
Ao degradar um aminoácido à primeira coisa que acontece é a liberação da amônia (NH3) que rapidamente é
transformada em amônio (NH4) e o esqueleto carbônico que sobra, o alfa-cetoácido. Então, temos diferentes
aminoácidos e diferentes alfa-cetoácidos. Por exemplo, quando a Alanina perde o grupo amino, vira piruvato. O
que é o piruvato? É um metabólito da glicólise, transformando-se em Acetil-CoA e depois podendo ser
encaminhado para o Clico de Krebs, para depois gerar energia. Ou seja, muitos alfa-cetoácidos podem entrar
em rota de energia.
Sobra o amônio (NH4), o que deve ser feito com este amônio? Ele pode ser usado para a síntese de compostos
nitrogenados, como bases nitrogenadas ou outras moléculas que utilizam o grupo amino, ou ele tem que ser
rapidamente excretado e a forma de excreção desse grupo é a ureia.
As reações que antecedem a formação da ureia são importantes, pois algumas enzimas destas reações são
marcadores de função hepática, por exemplo, quando o médico avalia função renal, ele pede transaminase,
TGO e TGP. Estas enzimas estão relacionadas com o processo de formação da ureia, pois o processo acontece
no fígado, se temos essas enzimas aparecendo no sangue, isto significa que as células hepáticas estão sendo
lesadas.
O primeiro processo de metabolização do aminoácido se chama reação de Transaminação, que são catalisadas
por aminotransferases ou transaminases (são sinônimos), então o que a célula faz? Ela pega um aminoácido que
tem que ser metabolizado e transfere o grupo amino desse aminoácido para o alfa-cetoglutarato e forma L-
glutamato e sobra o alfa-cetoácido correspondente desse aminoácido que perdeu o seu grupo amino. Qual a
lógica desse processo? Eu coleto grupo amino daqueles 20 grupos de aminoácidos diferentes que compõe as
proteínas e formo um único tipo de aminoácido, que é o glutamato. Este glutamato terá acesso livre para entrar
na mitocôndria da célula hepática para sofrer desaminação oxidativa para liberar o grupo amino que entrará
no ciclo da ureia.
Então, no ciclo da ureia, o grupo amino que foi liberado do glutamato (pela catalisação da glutamato
desidrogenase) forma carbamilfostato que formará outras moléculas. Como pode ver, a ureia elimina dois
grupos aminos de uma vez só, ela é muito eficiente por isso. Um vem do glutamato que sofreu desaminação
Medicina UFPA D 2015 – Urinário
oxidativa e o outro grupo amino vem do aspartato do citosol, esta ureia será encaminhada para o rim para
excreção.
No ciclo da ureia há gasto de ATP, o que aparentemente é estranho, já que a produção da molécula de ureia
gasta energia para ser eliminada, pois a célula tende a economizar energia (trabalha com parcimônia – termo
da biologia). A necessidade de sintetizar ureia está relacionada com a toxicidade do grupo amino em forma de
amônia, em estágios finais de intoxicação por amônia leva a edema cerebral, aumento da pressão intracraniana
e estado comatoso (em coma). O porquê deste sintomas ainda não é conhecido, porém há explicação para isto:
se a gente observa todo o metabolismo da formação da ureia, faz para entender sintoma. Possíveis causas: 1a
se eu acumulo amônia, tenho alteração do pH, pois a amônia é uma base forte e se transformará em amônio,
elevando o pH, provocando alteração estrutural em proteína e todas as rotas metabólicas serão alteradas; 2a
Depleção de ATP, para formar glutamina que é o meio de transporte do glutamato de órgãos extra-hepáticos
para o fígado, para poder levar os grupos amina para o fígado, é gasto ATP para isso, além de gastar ATP, diminui
a concentração de alfa-cetoglutarato (que é retirado do ciclo de Krebs), se está sendo retirando alfa-
cetoglutarato do ciclo que produz energia, acaba por contribuir com a redução da produção de energia. Então,
se eu tiver mais amônia que precisa ser transportada, vou ter mais glutamina para transportá-la e com isso há
aumento de pressão osmótica, o que pode estar relacionado ao edema cerebral e aumento de pressão
intracraniana. Além disso, se está se formando muita glutamina, consequente mente haverá uma redução de
glutamato; 3ª Redução de glutamato (um neurotransmissor que também é precursor de outros
neurotransmissores, como o GABA). Devido a redução de glutamato, haverá redução de outros
neurotransmissores. Todos esses sintomas estão relacionados ao sistema nervoso central, o que pode está
relacionado ao papel do glutamato no SNC (não é uma conclusão definitiva, mas uma via de possível causa).
Por que não se pode carregar um grupo amino produzido em um órgão extra-hepático pela corrente sanguínea
até o fígado ligado a uma molécula de glutamato? Porque o glutamato é um aminoácido carregado, tem carga
negativa e é difícil ele atravessar a membrana da mitocôndria da célula hepática. Então o que as células fazem?
Sintetizam glutamina. Então, a glutamina é importante para o transporte de íons amônia para o fígado, pois é
apenas neste órgão que acontece a síntese de ureia. (A professora deu ênfase ao gasto de energia para
realização do processo de formação da ureia e concluiu falando que é importante devido à alta toxicidade da
amônia).
1.1. A função da ureia como marcador de função renal
Nós produzimos cerca de 50~100g de ureia por dia, como uma forma atóxica de excretar amônia. Parte da ureia
filtrada é reabsorvida, pois tem um papel importante no processo de concentração urinária e regulação da água
que será reabsorvida, o que nos leva a ter uma uremia, presença de ureia no sangue, que fica em torno de 10 a
40 mg/dL, um aumento muito grande disso pode ser sintoma de uma doença renal. Qualquer diminuição da
função excretora renal haverá uma alteração na relação concentração de ureia na urina x concentração de
ureia no sangue (alta concentração de ureia na urina e baixa no sangue, quando ocorre diminuição da função
excretora renal esta relação se inverte, ocorrendo uma hiperuremia – alta concentração de ureia na corrente
sanguínea). Isto é comum de ser observado em algumas alterações renais, como glomerulonefrite (300 mg/dL
de ureia no sangue), esclerose renal, tuberculose renal, rim policístico, nefropatias, etc.
Entretanto, a ureia como marcador de função renal, tem que ser olhada com cautela, devido à produção da
ureia ser a partir da degradação de aminoácidos, então, se eu tiver uma alimentação super-proteica, pode-se
ter um aumento de ureia no sangue (devido a degradação de muito aminoácido), já na urina os níveis estarão
normais, neste caso, o aumento de concentração sanguínea não irá interferir na excreção da ureia pela urina.
Outras patologias não renais podem levar ao aumento da concentração de ureia no sangue. Por isso a avaliação
renal não é feita apenas observando os níveis de ureia, ela sempre estará associada a dosagem de creatinina,
para o diagnóstico ficar mais completo, porque se sabe que a creatinina não é influenciada pela alimentação,
por exemplo. A creatinina é influenciada por outros aspectos, mas existem fórmulas matemáticas que já
conseguem normalizar essas influencias, já se conhece o grau de erro que a creatinina pode induzir em uma
pessoa que faz muita atividade física, por exemplo.
Medicina UFPA D 2015 – Urinário
2. CREATININA
Tudo começa porque o ATP não é uma boa molécula de escolha para armazenar em quantidade como reserva
de energia. Por quê? Quais são as formas de regulação enzimática? Regulação Alostérica e Regulação Covalente.
As enzimas alostéricas precisam ser pelo menos diméricas, pois uma subunidade será regulatória e a outra
catalítica. Nesta subunidade regulatória haverá ligação de moduladores alostéricos, algumas moléculas, como o
ATP, são moduladores alostéricos. O que acontece se eu começar a guardar muito ATP? O ATP é modulador
alostérico negativo de rotas que produzem ATP, porque não haveria necessidade de produzir mais ATP se ele
está em excesso. O sinal para a célula produzir ATP é uma inversão da relação ADP x ATP, ou seja, ATP diminui
e ADP aumenta, isto para a célula significa diminuição de energia, fazendo ser necessário ativar rotas que façam
que a razão inverta. Por isso o ADP é um modulador alostérico positivo de rotas para produzir energia e o ATP é
um modulador alostérico negativo para produzir energia. O ATP, então, não é uma boa molécula para ser
armazenada.
Então como se faz para armazenar energia nos músculos, que necessitam ter reservas de energia, pois podem
ser exigidos de repente? O músculo usa ligações fosfato de alta energia em forma de creatina-fosfato (ou fosfato
de creatina), esta creatina não é produzida nos músculos, apenas fosforilada e armazenada. Isto serve quando
o músculo necessita de energia que não dá para esperar a via de fosforilação oxidativa (mais demorada), então
a creatina-fosfato dá o seu fosfato para o ADP e forma ATP, este ATP, então, pode ser usado para a contração
muscular.
Todo o processo de síntese de creatina-fosfato começa no rim, através da enzima AGAT (Glicina Amidino
Transferase) que leva a transformação de Arginina e Glicina em GAA (Ácido Guanidino Acético) e Ornitina. O
GAA será lançado na corrente sanguínea para chegar até o fígado; no fígado ocorrerá o processo de metilação
deste GAA para haver a conversão em CREATINA. A creatina sai do fígado até chegar nos órgãos que precisam
guardar energia (coração, cérebro e músculo). Nestes órgãos a creatina vai sofrer fosforilação pela creatina-
fosfoquinase (todas as quinases fosforilam e as fosfatases desfosforilam) para se tornar creatina-fosfato.
O que sobra desta creatina-fosfato após ser usada para a produção de energia? Sobra uma molécula chamada
Creatinina, um metabólito do uso da creatina-fosfato. Ela precisa ser eliminada, a creatinina não tem utilidade
para a célula, por isso ela é filtrada e eliminada.
Pergunta: A elevação dos níveis de creatinina na urina não é indício de falência renal, mas sim no sague? Não
exatamente, deve haver uma comparação entre o sangue a urina, para ver como está a taxa, se estiver elevado
no sangue e na urina, a razão permanece a mesma, então mostra que não tem lesão renal. Agora, quando a
pessoa usa muito suplemento alimentar e dieta hiper-proteíca, ela acaba sobrecarregando o rim, então as
chances de ter lesão renal é alta.
Então, a creatinina é totalmente excretada pelos rins, então, qualquer elevação plasmática de creatinina é
indicativo que os rins não estão conseguindo filtrar facilmente essa creatinina. Há, também, uma pequena fração
de creatinina que consegue ser secretada, o que isso significa? Que nem toda creatinina passou pelo glomérulo,
uma pequeníssima parte é secretada e isso deve ser contabilizado quando for fazer o cálculo final, se não
podemos superestimar a taxa de filtração glomerular (se for feito uma relação direta da taxa de creatinina que
aparece na urina e a taxa de creatinina na filtração glomerular – considerando que ela é totalmente filtrada – e
esquece que uma parte da creatinina é secretada direta nos túbulos, acaba superestimando a filtração. Então,
pode-se imaginar que a taxa de filtração está maior do que o normal, porém, há uma parte de creatinina vindo
de uma via que não é pela filtração glomerular. Por isso, deve-se compensar quando for fazer os cálculos da taxa
de filtração glomerular).
Existem limitações em relação ao uso de creatinina como marcador: por exemplo, massa muscular mais
elevada, a pessoa vai ter mais creatina-fosfato, então ela vai ter mais creatinina. Os níveis de creatinina vão
mudar conforme a idade e sexo. Porém, o legal da creatinina é que já se sabe muito sobre ela.
3 – PROTEINÚRIA
Medicina UFPA D 2015 – Urinário
Presença de proteína na urina mais do que o normal, por problema na reabsorção tubular ou filtração
glomerular. Normalmente, a função de barreira dos glomérulos e reabsorção, torna o filtrado quase livre de
proteínas. Por que isto é importante? Tem-se a formação de 170 litros de filtrado por dia e se considerarmos
que temos 7 g/dL de proteínas plasmáticas e se estas proteínas passassem pelo glomérulo renal, seria filtrado
11,9 kg de proteína por dia, o que tornar-se-ia inviável a reabsorção pelos túbulos (devido ao processo de
reabsorção de proteínas ser saturável), além disso, o fígado seria incapaz de ressintetizar, pois depois que
perdemos proteína no filtrado ela vai ser reabsorvida em seu aminoácidos constituintes. O fígado teria que
ressintetizar 11,9 kg de proteína por dia.
Existe uma limitação de tamanho e carga elétrica que vai barrar as macromoléculas constituintes da proteína. A
perda parcial desta barreira leva a sérias consequências, como aumento de pressão oncótica (pressão osmótica),
formação de edema e outras coisas relacionadas com perda de proteína.
Apesar da existência dessa barreira, um pouco dessa proteína passa pela cápsula de Bowman, pelos poros de
shunt. Então, atravessa de 1 a 5 gramas de proteína a cápsula de Bowman e 95% é reabsorvida no túbulo
proximal por um processo de endocitose saturável (devido à presença de cavéolas, que são depressões que têm
proteínas que favorecem o processo de reabsorção das proteínas que passam no glomérulo).
Resumindo, as proteínas que passam pela cápsula de Bowman, vão ser reabsorvidas nos túbulos proximais na
forma de aminoácidos constituintes, pois as proteínas são endocitadas e são hidrolisadas por lisossomos, que
vão chegar até o sangue, ou seja, o que é reabsorvido é o aminoácido constituinte, a proteína é perdida. Os
outros 5%, que são proteínas pequenas, são excretados na urina. A albumina é comum aparecer em grande
quantidade na urina de pessoas que tem problemas renais (pois é uma proteína grande). É comum encontrar na
urina proteínas dos próprios túbulos renais (Tamm-Horsfall), um pouco de albumina (menos da metade) e
proteínas de baixo peso molecular.
Quando os níveis de proteína na urina passam dos 150mg/dia, tem-se o que é chamado de Proteinúria. Alguns
termos utilizados (os níveis podem variar de laboratório para laboratório): Microalbuminúria: excreção urinária
de albumina entre 30 e 300 mg/dia. Albuminúria: excreção urinária de albumina de mais de 300 mg/dia. Alguns
laboratórios não diferenciam em albuminúria e microalbuminúria, chamam a perda de albumina de albuminúria.
Pode-se ter microalbuminúria sem proteinúria associada (por exemplo, pode-se ter 120 mg/dia de proteína e
60mg/dia de albumina).
Quando se passa de 300 mg/dia de proteínas na urina há uma glomerulopatia associada, ou seja, o glomérulo
está lesado e deixando passar tanta proteína que nem o túbulo proximal não está conseguindo reabsorver.
Existem, então, diferentes níveis de proteinúria e cada nível terá uma importância clínica diferenciada.
Pode-se ter uma proteinúria de baixa intensidade, aquelas com que tem menos de 300 mg/dia, o que
levará ao clínico pensar que o paciente está com princípio de processo patológico. Se esta glomerulopatia
inicial não for tradada, a contínua passagem de proteína pelo glomérulo vai levar ao agravamento da
glomerulopatia (podendo tornar-se crônica). Em casos de nefropatia diabética, pelo excesso de glicose e
diurese, o que sobrecarrega o rim, levam a albuminúria (recomenda-se que os diabéticos façam
constantemente exame para verificar presença de albumina na urina). A nefropatia diabética pode
apresentar: paciente sem hipertensão, TGF normal ou elevada, acidificação e concentração urinária
preservadas, mas com presença de albuminúria.
Proteinúria de média intensidade, são os casos no qual há excreção de mais de 300 mg/dia de proteína,
no qual há quadro de lesão glomerular clinicamente relevante, necessitando de investigação mais
detalhada, fazendo-se exames de clearance de creatinina, creatinina no plasma, ultrassonográficos
(devido ao aumento do rim em casos agudos) e biópsia renal. Mesmo após o diagnóstico e início do
tratamento, faz-se necessário realizar exames de urina constantemente para verificar se está diminuindo
a proteinúria (ela serve como indicativo se o tratamento está dando certo ou não).
Proteinúria maciça, na qual há uma perda de 3,5 g por dia de proteína na urina, estando associada a
outros sintomas, como hipoalbuminemia (albumina reduzida no sangue), que reduz a pressão oncótica
Medicina UFPA D 2015 – Urinário
do plasma e promove edema generalizado, além de provocar hipercolesterolemia associada, porque o
fígado fica sobrecarregado em sintetizar a albumina perdida, aumentando a atividade hepática e,
consequentemente, aumento de lipoproteínas. Estes três sintomas juntos (proteinúria maciça, edema
generalizado e hipercolesterolemia) caracterizam a síndrome nefrótica.
A síndrome nefrótica pode ocorrer em glomerulonefrite severa, em intoxicação medicamentosa e até por picada
de alguns insetos. Pode ocorrer sem alterações histológicas visíveis (chamada de síndrome nefrótica de lesões
mínimas) e quanto maior for a proteinúria, maior a chance da síndrome nefrótica evoluir para uma insuficiência
renal crônica terminal (devido ao fato de que excreção de proteína leva a inflamação que pode levar a esclerose
precocemente e a quadros de insuficiência renal crônica).
Existem três mecanismos básicos de proteinúria:
a) Decorrente do aumento de permeabilidade glomerular, ou seja, a proteína aparece no filtrado porque o
glomérulo tem mais permeabilidade a ela devido a lesão glomerular;
b) Decorrentes de defeito na reabsorção tubular, ou seja, o glomérulo está íntegro, mas o que chega ao
túbulo não pode ser reabsorvido por algum problema tubular, então terá eliminação de proteína;
c) Decorrente da filtração de proteínas anômalas, neste caso, existe outras patologias não renais, por
exemplo, um mieloma múltiplo pode gerar imunoglobulinas parcialmente formadas que tem um tamanho
menor e carga elétrica alterada, que acabam conseguindo ultrapassar a barreira glomerular.
- Proteinúria decorrente do aumento da permeabilidade glomerular
São classificados em seletivas e não seletivas.
O aumento da permeabilidade não seletiva é caracterizado pelo aumento de poros de shunt, o que acarretará
no aumento de passagem de macromoléculas com raios maiores de 50 angstrons. A proteinúria nesta situação
é caracterizada por proteínas de alto peso molecular (imunoglobulinas) e concentração de albumina também
alta (20 vezes superior as imunoglobulinas). Glomerulopatias com esta característica são agressivas e de caráter
progressivo.
O aumento da permeabilidade seletiva é caracterizado não pelo aumento de poros (que continua o mesmo),
perdem-se as cargas dos proteoglicanos e outras proteínas presentes nos poros de shunt, levando a perda da
repulsão eletrostática negativa. Neste caso, a urina terá uma alta concentração de albumina, não haverá
imunoglobulinas, porque os poros estão normais (então, proteínas de alto peso molecular são quase
indetectáveis). Assim, consegue-se diferenciar a seletiva da não seletiva. A seletiva tem um caráter menos
progressivo que a não seletiva e tem uma melhor resposta ao tratamento. Vale ressaltar que ambas podem
acontecer juntas, o que agravará ainda mais os sintomas associados.
- Proteinúria decorrente de defeitos na reabsorção tubular
Neste caso, a barreira glomerular está perfeita, a passagem de proteína acontece nos níveis normais.
Entretanto, a falta de reabsorção tubular levará ao aumento da proteína na urina. Neste caso, a urina terá uma
concentração maior de albumina e proteínas de baixo peso molecular. Esta concentração é proporcional ao que
é presente no filtrado. Normalmente, é caracterizada por uma proteinúria de baixa intensidade (menor que 1
grama de proteína por dia).
- Proteinúria decorrente da filtração de proteínas anômalas
Elas são decorrentes de lesões não renais. Formam-se imunoglobulinas anômalas, que é comum em
idosos. Em mieloma múltiplo, pode-se ter proliferação de linfócitos B mal formados. Em caso de amiloidose
primária, que é o acúmulo de proteínas em tecidos específicos, também há produção de proteínas mal formadas.
As proteínas mal formadas não vão ser repelidas de maneira eficiente nos poros pela repulsão eletrostática
negativa, vão ter tamanhos menores que dos poros e vão conseguir ser filtradas. Então, a proteinúria não é
decorrente de lesão renal, mas porque as proteínas estão sendo mal formadas. Esta proteinúria é conhecida
como Proteinúria de Bence Jones. Esta proteinúria pode atingir níveis maciços, níveis de mais de 1,5 g/dia (a
Medicina UFPA D 2015 – Urinário
professora falou agora que é 1,5 g/dia para caracterizar proteinúria maciça, antes era 3,5 g/dia) por dia, porém
não será observado hipoalbuminemia e nem o quadro de síndrome nefrótica, porque esta proteinúria não é
formada por albumina, mas por imunoglobulinas anômalas.
Para concluir. A proteinúria é causa e consequência de insuficiência renal. O acúmulo de proteínas no lúmen
tubular vai causar reações inflamatórias, que leva a lesões estruturais do interstício e progressão da insuficiência
renal. Estudos in vitro já mostram que a presença de proteínas no mesângio, leva as células mesagiais liberarem
citocinas que causam glomeruloesclerose. Além disso, já foram observados efeitos adversos nas regiões
tubulares proximais, então a própria proteinúria sendo um mecanismo de progressão de lesão renal. A
proteinúria acaba sendo um alvo terapêutico importante para barrar a progressão de patologias renais.
4. CISTATINA C (TRAÇO GAMA OU PÓS-GAMA-GLOBULINA)
A Cistatina C está em estudo e não está em uso, porque ainda é caro. Ela tem um pequeno peso molecular, tem
função na célula de inibir proteases e é produzida de forma contínua e estável por todas as células nucleadas,
então, a taxa plasmática da Cistatina C é contínua. Além disso, possui pequeno tamanho e alto ponto isoelétrico
(pH em que a proteína está neutra), o pH da Cistatina C é de 9,3, isso significa que no pH celular ela está positiva,
o que leva ela ser totalmente filtrada. Devido à taxa constante de Cistatina C no sangue, qualquer aumento dela
no sangue vai indicar uma diminuição na taxa de filtração glomerular. Ela é interessante porque não sofre
influência dos fatores que alteram a creatinina, que são: massa muscular, sexo ou alimentação hiper-proteíca e
parece não ser afetada por estados febris.
Aula 3
(Andréa)
PROCEDIMENTOS ANALÍTICOS
Não é possível medir a função renal diretamente a partir da taxa de filtração glomerular, não dá para
isolar um glomérulo e medir o quanto de plasma passa através dele. Portanto, usam-se técnicas indiretas para
fazer essa análise, chamadas de medidas de depuração, determinam o ritmo de filtração glomerular através da
taxa de depuração plasmática de compostos pelos rins. A taxa de depuração plasmática é o quanto de plasma
tem que passar através dos rins para que ele se livre se uma determinada substância, sendo filtrada do plasma.
Quando uma substância é acrescentada no plasma, invariavelmente, ela vai sofrer um decaimento da sua
concentração com o tempo, isso pode ser devido a diversos processos dependendo da substância. Entre esses
processos têm-se: entrada em todas as células do organismo (ex. glicose. Ela é absorvida pelo intestino, chega
no plasma e é absorvida pelas células); metabolização hepática; eliminação renal. Dependendo da substância
há diferentes vias de saída do plasma.
Ao escolher uma substância para avaliar a taxa de filtração glomerular, é preciso escolher uma substância
que seja retirada do plasma devido à eliminação renal, sem ter outra eliminação paralela, caso contrário
ocorrerá uma subestimação ou uma superestimação da taxa de filtração glomerular. A taxa de depuração de
qualquer substância que tem eliminação renal depende da facilidade com que ela é filtrada pelos glomérulos,
bem como pelo seu processamento ao longo dos túbulos. Além disso, essa substância deve ser somente filtrada
pelo glomérulo, não pode ser reabsorvida (isso irá subestimar a taxa de filtração glomerular), não pode ser
secretada (isso pode superestimar a taxa de filtração glomerular).
Se eu tiver uma substância que é filtrada livremente no glomérulo e não é processada no restante dos
túbulos, sua quantidade na urina por unidade de tempo é uma indicação do quanto de plasma passa pelo
glomérulo.
Vantagens de se utilizar essas técnicas de depuração: quantificar a função excretora dos rins; quantificar
a taxa de sangue que flui através dos rins; avaliar processos de filtração glomerular, reabsorção tubular e
secreção tubular.
Medicina UFPA D 2015 – Urinário
Se eu sei que no plasma que passa através dos rins eu tenho 1mg de uma subtância X por ml de plasma e
eu sei que esse 1mg é excretado na urina por minuto, a taxa de depuração dessa substância X é 1 ml de plasma
por minuto. Ou seja para eu ter 1mg dessa substância na urina eu preciso que 1 ml de plasma passe através do
glomérulo, porque essa é a sua concentração no plasma.
A depuração se refere ao volume de plasma que seria necessário para fornecer a quantidade da substância
excretada na urina por unidade de tempo. Têm-se uma equação que ajuda a determinar esse ritmo:
TFP (Taxa de Filtração Plasmática) = Taxa de Excreção Urinária
TFP= Taxa de depuração da substância x Concentração plasmática da substância
TEU = Concentração urinária da substância x Fluxo urinário
A taxa de depuração da substância é a mesma coisa que a taxa de filtração glomerular, afinal a substância
em questão tem filtragem livre, portanto:
TFG = Taxa de Excreção Urinária
Concentração plasmática da substância
Como já mencionado, não é possível avaliar diretamente a taxa de filtração glomerular, portanto utilizam-
se marcadores. Um bom marcador é produzido endogenamente, por isso a creatinina é tão importante, por sua
produção endógena. Além de ser totalmente filtrada, não é reabsorvida, apresenta apenas uma pequena
secreção, que é conhecida e pode ser corrigida.
Além da creatinina, têm-se substâncias que são exógenas e também são totalmente filtradas, porém seu
uso na prática clínica é limitado, pois seria preciso fazer infusão intravenosa constante dessa substância para
atingir seu estado estacionário e usá-la como marcador de função renal.
Porém esses marcadores exógenos são usados experimentalmente, como a inulina. A inulina é um
sacarídeo, é injetada por bombas de infusão intravenosa no paciente e se atinge um ponto de equilíbrio, quando
a concentração de inulina é de 1mg/ml. Se a concentração de inulina plasmática é 1mg/ml, e a concentração
urinária dessa substância é de 125 mg/ ml, sendo que o volume urinário é 1 ml por minuto, é possível calcular a
taxa de filtração glomerular.
Ao substituir esses valores, é possível inferir que se eu tenho 125 mg da substância por ml na urina, teve
que passar 125 ml de plasma. A inulina é um bom marcador de taxa de filtração glomerular. O problema é que
ela não é produzida endogenamente, sendo necessária infusão intravenosa constante, até se atingir um ponto
de equilíbrio (geralmente 1mg/ml) e a partir daí quantificar a quantidade na urina para estimar a taxa de filtração
glomerular.
Pergunta: Como é possível determinar a taxa de urina por minuto?
Coleta ao longo do tempo. Se for coletado por 1 hora e teve um volume X, faz-se uma regra de três e se
sabe estimar a produção de urina por minuto. Como se fosse uma relação linear, não tem como ser diferente.
(Águida)
Vamos supor que uma infusão contínua de inulina é administrada para calcular a TFG. No estado de
equilíbrio tem-se 8mg/l de inulina. Coleta-se a urina por 2 horas (coleta de urina cronometrada), o volume de
urina excretado durante esse tempo foi de 200ml, então em 1h é de 0,1l/h. A concentração final de inulina na
urina foi de 720mg/l, qual seria então a TFG?
(O cálculo e o textinho na íntegra estão no slide)
R: 9 litros por hora.
Essa técnica de depuração começou a ser usada com a ureia (ela fala que começou a ser usada em 1929
etc). O grande problema é que, apesar da ureia ser livremente filtrada, ela é 40% reabsorvida, então isso dificulta
um pouco a interpretação do resultado. Sendo assim, não é possível avaliar completamente a depuração de
Medicina UFPA D 2015 – Urinário
ureia, porque ela é totalmente filtrada, só que ela não aparece totalmente na urina no final, pois 40% não vai
para a urina porque é reabsorvida.
A ureia pode ser usada em termos de uremia, mas sempre associada à dosagem de creatinina, nunca
como uma dosagem isolada, para que se possa ter um panorama mais completo da realidade do que está
acontecendo nesse órgão.
A ureia tem um outro viés que dificulta a interpretação do resultado: a alimentação hiper protreica, que
leva à muita produção de ureia, sem que haja nenhum problema renal, mas é claro que se a alimentação
hiperproteica for prolongada (suplementos de aminoácido, suplemento disso, suplemento daquilo), sem fazer
atividade física, os rins vão acabar sendo sobrecarregados, e aí sim pode se desenvolver uma patologia renal.
O método mais utilizado é a depuração da creatinina endógena. A creatinina é liberada em ritmo
constante no sangue, a partir do metabolismo muscular, e é livremente filtrada e eliminada através da urina
(estágio estacionário da creatinina – concentração constante). Existe uma pequena secreção tubular de
creatinina, cerca de 10% da creatinina que é excretada não passou pelo glomérulo, ela foi secretada através dos
túbulos, e isso seria um inconveniente no uso da creatinina como um marcador de função renal, e esse efeito
de secreção de creatinina é mais acentuado em pacientes com TFG baixa, porque acumula creatinina no plasma,
então terá mais volume para ser secretado. É difícil usar a creatinina como uma taxa de depuração em pacientes
com doenças terminais, porque a secreção vai ser muito elevada e a tendência vai ser superestimar a TFG se for
utilizada a creatinina como um marcador.
A técnica utilizada para avaliar a concentração de creatinina plasmática também marca outras moléculas,
e essa marcação é mais ou menos proporcional à quantidade de creatinina que é secretada (um erro anulando
outro). Então é assim que se chega à uma taxa bem próxima do que é realmente a filtração da creatinina. Quando
se marca outras moléculas, eleva também a creatinina plasmática, elevando assim a creatinina urinária,
elevando dos dois lados consegue chegar mais próximo da realidade.
Apesar de tudo, a creatinina é o marcador renal mais utilizado na prática clínica. O cálculo da creatinina é
feito da seguinte forma:
(É a explicação da fórmula do slide)
A TFG (sendo a mesma coisa que depuração) é igual à Taxa de Excreção (Concentração na Urina [Us] x
Volume Urinário [V]), sobre a Concentração Plasmática [Ps]. Aqui na equação ainda foi adicionado o tempo (24h)
e ai faz-se uma relativização (porque superfície corporal, massa muscular etc vão interferir na quantidade de
creatinina) por 1,73, que é uma superfície corporal média de um adulto. Se são indivíduos pediátricos ou obesos,
tem um outro fator de correção que é o A, que considera o peso e altura para que se possa fazer uma
relativização mais aproximada da realidade.
Os resultados são ml/min de creatinina, por superfície corporal. Os valores para mulheres são menores
que os valores para homens, pois os homens têm maior produção de creatinina, portanto, uma maior
eliminação.
A própria Doença Renal Crônica vai ser avaliada em seus estágios de acordo com a TFG, e essa TFG vai ser
determinada dessa forma (que foi descrita acima). Coleta de urina cronometrada, não se pode perder volume
urinário, pois é importante para colocar no cálculo, então para se fazer o cálculo precisa da concentração urinária
e volume urinário, significando que a coleta da urina tem que ser controlada ao longo do dia. O material precisa
ser muito bem coletado e além disso, precisa-se coletar sangue para que se tenha a concentração plasmática da
creatinina.
Fatores que dificultam avaliação da TFG:
A coleta de urina de 24h pelo próprio paciente pode gerar um erro, tanto de volume urinário
como erro de armazenamento, isso vai gerar problemas na TFG final, podendo ser abaixo do valor real.
Medicina UFPA D 2015 – Urinário
Algumas drogas inibem a secreção e aumentam a creatinina sérica, então não se pode utiliza-las
quando se quer fazer a dosagem de creatinina.
Na Insuficiência Renal Grave tem uma grande porcentagem de creatinina sendo secretada, então
é totalmente inviável o portador dessa patologia usar depuração de creatinina para análise.
Na Insuficiência Renal Grave tem a secreção de 60%, então a maior parte de creatinina que chega ao
túbulo não é filtrada, e sim secretada.
Na depuração consegue-se ter uma medida da TFG, com todos os vieses. Para desviar desse processo na
prática clínica, utiliza-se a medida da creatinina plasmática que consegue estimar a TFG, usando cálculos
matemáticos que corrigem alguns erros de Massa Corporal, Sexo, Idade.
Pergunta: Consegue corrigir na Insuficiência Renal?
Não. Para Insuficiência Renal Crônica não se tem ainda um marcador muito apropriado. Todos os
processos renais são alterados, então não se tem o controle do quanto está alterado para poder usar correções
matemáticas (valores). O desenvolvimento da Insuficiência Renal tem vários estágios, então não tem como
“adivinhar” qual o estágio que a pessoa está. Utiliza-se as medidas de depuração plasmática total.
A análise é feita através dos cálculos matemáticos (a filtração é igual a excreção da creatinina), como a
produção é constante, as três partes são igualadas, (produção, filtração e excreção).
Filtração: TFG (ou depuração) X creatinina plasmática.
Excreção: Concentração na urina X volume urinário.
Produção: Taxa de Creatinina Plasmática x TFG
Se eu isolar a taxa de creatinina plasmática, eu percebo que ela é inversamente proporcional à TFG, o que
é uma coisa óbvia. A medida que eu vou diminuindo a TFG, eu começo a aumentar a concentração de creatinina
no plasma. A concentração de creatinina plasmática é função inversa da TFG.
TFG Retenção de Creatinina Concentração Plasmática de Creatinina
(Ela mostra um gráfico no slide)
O gráfico mostra uma relação entre a TFG e a Concentração Plasmática de Creatinina. A linha cinza
representa a normalidade, ela muda quando a TFG muda de um estágio normal para bastante reduzida. De 120
até 60 de TFG, tem-se uma concentração considerada normal de creatinina sérica, quando começa a ter valores
mais reduzidos de TFG, ela aumenta.
Por isso, a relação entre TFG e Concentração Plasmática de Creatinina é claramente não linear, ou seja,
grandes mudanças na TFG (ex: de 120 para 80/60) são associadas com pequenas mudanças de creatinina sérica.
Quando se interpreta um dado de creatinina plasmática e nota-se um pequeno aumento naquele paciente que
está sendo monitorado, isso pode significar uma grande perda de capacidade de Filtração Glomerular.
Outro fator que deve ser levado em conta é que a creatinina tem esse efeito sobre a massa muscular,
então para interpretar dados apenas de creatinina plasmática, tem que lembrar que quanto maior a massa
muscular, maior a produção de creatinina. Então pode-se ter um significado clínico diferenciado para dois
indivíduos com massas musculares diferentes (aquela imagem que tinha uma mulher bem magrinha e um
homem super musculoso), ou seja, eu posso ter um indivíduo musculoso com uma taxa de creatinina plasmática
alta e ainda assim ele ter uma TFG normal, pois ele apresenta mais creatinina no plasma. Se você está medindo
só a creatinina plasmática e pegar um indivíduo musculoso, ela estará, mas não significa que ele apresenta uma
lesão renal, porque na urina ela também estará alta.
Para a pessoa magra, ela pode apresentar uma taxa de creatinina plasmática normal e ainda assim,
apresentar uma TFG, pois ela tende a produzir menos creatinina por ser magra. Ela está dentro da normalidade,
Medicina UFPA D 2015 – Urinário
só que para ela a normalidade está alterada, pois ela tem pouca massa muscular, podendo mascarar a
interpretação do resultado.
(Mais um gráfico)
O A é o indivíduo musculoso, o B é o indivíduo normal e o C é o indivíduo franzino. Todos estão dentro da
normalidade de Taxa de Creatinina Plasmática, mas a filtração glomerular em cada um deles está diferente. O
normal muda de acordo com a massa muscular do indivíduo.
Outra coisa que se leva em conta quando a creatinina plasmática é avaliada para estimar a TFG é o efeito
da idade.
Com a idade, há uma perda progressiva de néfrons, então, aos 80 anos há uma perda de 50% da TFG.
Seria esperado ocorrer uma elevação recíproca da creatinina plasmática, no entanto, o que ocorre é, com a
diminuição dos hormônios que estão relacionados com a manutenção da massa muscular, há uma perda de
massa muscular, levando a uma diminuição na produçã de creatinina.
Para indivíduos idosos, valores de creatinina plasmática considerados normais podem estar indicando
uma TFG reduzida. A perda de massa muscular leva a uma menor produção de creatinina.
(Mais uma parte para acompanhar no slide)
Para resolver todos esses vieses e ainda utilizar apenas a Concentração Plasmática de Creatinina para
estimar a TFG, faz-se correção matemática. A estimação da TFG com alguns fatores de correção leva em conta
a massa muscular, a idade e o peso e, se for uma mulher multiplica por 0,85 para corrigir o efeito da massa
muscular feminina ser menor.
Tem-se dificuldade em utilizar apenas a creatinina plasmática por conta de todos os vieses (idade, massa
muscular, sexo) e além disso, para fazer o método natural de depuração, há uma dificuldade na coleta de urina
se não é feita em ambiente hospitalar. Através do uso das equações matemáticas, consegue-se chegar mais
próximo da estimativa real da TFG.
Um homem de 20 anos, de 80 kg, com uma Concentração Plasmática de Creatinina igual à dessa mulher
que tem 65 anos e 60 kg. Se eu aplico esses dados na equação eu chego a uma estimativa de TFG bem diferente,
porque a equação leva em conta as características do homem e da mulher.
A equação MDRD leva em conta mais parâmetros, além da creatinina plasmática (idade, sexo, etnia). Mais
uma vez os resultados da TFG serão diferentes (vendo o slide, vocês podem pensar que o resultado está muito
diferente mas é porque uma está dando ele relativizado pela superfície corporal, na anterior, era por ml/min,
então na verdade o resultados das duas é muito próximo).
Métodos de depuração são utilizados para determinar a TFG, porque é dificil estimar a quantidade
de plasma que passa pelo glomérulo de uma maneira direta, por isso que se faz a utilização de moléculas que
conseguem marcar a passagem de plasma, sendo elas mesmas filtradas com a mesma intensidade que o plasma
é filtrado. Então o que aparence dessa molécula na urina é o que passou de plasma no glomérulo. A técnica
tradicional de depuração avalia a contração na urina, concentração np plasma, avalia ao longo do tempo, para
chegar na TFG. Esse método só é bom em ambiente hospitalar, onde se consegue fazer uma coleta adequada
de urina.
(Ádria)
INSUFICIÊNCIA RENAL
Na insuficiência renal há regressão progressiva de metabólitos nitrogenados, afinal, é o rim que excreta
esses metabólitos, temos também edema, pois haverá filtração anômala de proteínas que causará edema e a
perda de capacidade de urinar, incapacidade de regulação do equilíbrio ácido-base, incapacidade dos balanços
dos níveis plasmáticos de uma série de íons.
Quando esse quadro se instala de maneira lenta, sem muitos sintomas, ocorre devido os néfrons terem
plasticidade, por exemplo, quando um néfron começa a perder função, outro néfron faz a função dobrada,
Medicina UFPA D 2015 – Urinário
compensando. Por causa disso, os sintomas da insuficiência renal demoram muito a aparecer. Quando os
sintomas surgem, o quadro já está bem avançado, dar-se o nome de insuficiência renal crônica (IRC). Já de
forma abrupta, por algumas causas que citarei adiante, com todas as ações recorrentes de todos esses
problemas que a falta da ação renal vai acarretar, é chamado de insuficiência renal aguda (IRA), caracterizada
por perda significativa e abrupta da função renal, geralmente o primeiro sintoma é a diminuição do volume
urinário, ela é potencialmente reversível, mas possui uma alta morbidade associada.
Vai acometer pacientes de todas as áreas de atuação médica, ou seja, pelo menos uma vez na vida
médicos de outras áreas vai acabar lidando com casos de insuficiência renal. Possui diagnóstico complexo devido
possuir diversas comorbidades associadas.
A IRA divide-se em IRA pré-renal, IRA renal ou intra-renal e IRA pós-renal. Então pode ser causada por
alterações que antecedem o rim, alterações hemodinâmicas; pode ser causada por problemas que acontecem
dentro do rim e, ainda, pode ser causada por problemas pós renais, pelos ureteres, por exemplo.
A IRA pré-renal: origem hemodinâmica, os rins estão funcionando, o problema é que não há um aporte
adequado de sangue, nesse caso há um baixo débito cardíaco (DC), contribuindo para uma baixa perfusão renal
ou uma hipovolemia, vasodilatação periférica, aumento da resistência vascular renal, diminuição da filtração
glomerular por isquemia também são causas de IRA pré-renal, todas alterações hemodinâmicas. Uma
quantidade cada vez menor de sangue chega até os rins, que estão íntegros, logo o processo é reversível, desde
que corrija o problema original: a hemodinâmica. Fisiologicamente, 25% do DC é direcionado aos rins, que vão
filtrar 60 vezes/dia o volume plasmático para reabsorver o que precisa ser reabsorvido e eliminar o que precisa
ser eliminado. E desse processo há um ajuste fino da excreção de sódio, uma fração de excreção menor que 1%,
isso faz com que consigamos manter o volume do liquido extracelular constante.
A diminuição de aporte de sangue aos rins acarreta em queda da filtração glomerular, o aumento da
creatinina plasmática, em proporção inversa a queda de filtração glomerular, aumento desproporcional da ureia
plasmática, porque o rim vai estar envolvido em fazer uma concentração da urina, para poder reabsorver água
e com isso tentar restabelecer a volemia, e a diminuição do fluxo urinário. Começa a haver uma inversão da
razão sódio/potássio na urina que normalmente é maior que 1, isso significa que o rim está reabsorvendo todo
o sódio possível (a taxa de excreção de sódio se aproxima a zero) para tentar restabelecer os níveis de água para
restabelecer a volemia. Resumindo: a variação típica dos parâmetros bioquímicos plasmáticos urinários numa
IRA pré- renal observada é o aumento da concentração plasmática de creatinina, aumento da concentração
plasmática de ureia desproporcional, razão ureia creatinina invertida, ou seja, maior que 40, vou ter mais ureia
que creatinina, justamente devido a essa reabsorção desproporcional de ureia em relação a creatinina, tenho a
diminuição do fluxo urinário, diminuição muito grande da excreção de sódio, diminuição da excreção de potássio
e vejo ainda o aumento da osmolalidade urinária.
O agravamento da hipoperfusão e hipovolemia, isso até, não é estabelecida a volemia e isso permanece
por mais tempo, pode haver transição de uma IRA pré renal para uma IRA renal ou intra-renal, nesse caso as
células do coração estarão como prioridades, pois se eu continuo tendo uma hipolovemia, continuo diminuindo
ainda mais o sangue para o rins para poder direcionar o sangue para órgãos especiais, como cérebro e coração,
o que vai agravar ainda mais a isquemia e hipóxia renal, com isso vai haver vasoconstrição rena, diminuição do
fluxo renal e diminuição ainda maior da taxa filtração de filtração glomerular, nesse quadro há a transição da
IRA pré renal para IRA renal, podendo ter associado a isso a necrose tubular aguda.
Qual a lógica de fornecimento de oxigênio para diferentes porções dos rins? Uma vez que é um órgão que
recebe um valor considerável do DC mas utiliza muito pouco desse oxigênio, pois o sangue que chega até os
rins, chega para garantir a filtração glomerular, o total utilizado de oxigênio presente nesse sangue pelo rim é
pequeno, a medula externa, por exemplo, beira a hipóxia, porque ela possui transporte ativo elevado, há uma
diminuição da tensão do oxigênio nessa região devido a disposição contracorrente dos vasos, migração precoce
Medicina UFPA D 2015 – Urinário
de oxigênio dessa região para essa região (ela aponta para o slide) em processo de isquemia esse quadro fica
mais grave ainda.
Nesse processo de transição a capacidade de retenção de urina e redução da taxa de excreção de sódio
são mantidas, nesse caso, quando ainda não tem estabelecido uma IRA renal, a gente tem condições de rever a
IRA pré-renal pela correção da hipovolemia. Só que se esse processo persiste a gente vai ter então o
estabelecimento de uma IRA renal, muitas vezes isso pode acontecer sem antes existir uma IRA clássica pré-
renal ocorrendo.
A IRA intra-renal pode ser de dois tipos oligúrica e não-oligúrica. A IRA intra-renal oligurica é aquela em
que há redução da produção de urina, a não oligúrica não apresenta redução de produção de urina, e as vezes
tem maior produção de filtrado que não chega a nem ser urina. Na IRA intra-renal há necrose tubular, por causa
de agressão ou isquemia; edema por retenção de líquidos, principalmente, na forma oligúrica, ou seja, se tem
diminuição da eliminação da urina significa que o filtrado está sendo retirado do túbulo em porções anteriores,
logo não está chegando no seu destino final; hipertensão arterial, por hipervolemia; diminuição da filtração
glomerular, isso no caso da oligúrica; aumento da ureia e da creatinina plasmática, obviamente a taxa de
filtração glomerular está bem diminuída; diminuição da depuração renal, proteinúria podendo evoluir para
forma crônica, que aí sim é irreversível. A IRA renal pode ser revertida dependendo do tempo que ela está
estabelecida, pois ela pode evoluir para forma crônica se não for tratada a tempo.
Há aumento da ureia e da creatinina plasmática, mas não mais de maneira desproporcional, mostrando
que os rins não estão conseguindo mais fazer a reabsorção de ureia para fazer a reabsorção de água. A razão
ureia/creatinina passa a ser menor que 40, geralmente é maior, pois temos mais ureia que creatinina na corrente
sanguínea. Temos fluxo urinário extremamente reduzido na oligúrica, e na não-oligúrica pode-se ter mais de
400 ml por dia; o sódio na urina aumenta, pois o rim não consegue mais reabsorver sódio; o potássio na urina
diminui; a osmolalidade urinária é semelhante ao plasma, então o filtrado não mais está sendo processado. Isso
indica que os rins não estão funcionando adequadamente.
Nesse momento, você observa células tubulares necrosadas ou ausentes, eu vou ter restando nos túbulos
em alguns seguimentos apenas a membrana basal. Porque a hipóxia é tão prejudicial para as células renais e a
células aeróbias? Quando submetido a uma hipóxia prolongada há diversas alterações vasculares, que vão gerar
vasoconstrição arterioso glomerulares e com isso uma hiperperfusão, isso tudo vai levar uma diminuição de
filtração do glomérulo. Com isso, essa vasoconstrição pode ser ocasionada por um desbalanço entre
vasoconstritores e vasodilatadores, podendo ter excesso de vasoconstritores, deficiência de vasodilatadores,
como prostaglandinas, NO, fator natriurético atrial e ainda a presença maciça de células inflamatórias que tem
efeito vasoconstritor. Mas isso não explica diretamente a necrose das células tubulares, nem a disparidade que
existe entre IRA renal oligúrica e IRA renal não-oligúrica.
O que explica são efeitos deletérios da própria hipóxia em todos os tipos celulares, como diminuição do
fornecimento de nutrientes, diminuição da remoção de metabólitos, altas taxas de glicogenólise, altas taxas de
glicólise levando a acidose láctica, queda na produção de ATP porque não há oxigênio , então vai ter que se
sustentar na fermentação láctica, então haverá acúmulo de AMP e seus metabólito, que são adenosinas e
hipoxantina. E ainda vou ter perda de gradientes iônicos, porque se eu não tenho ATP liberado para as bombas
funcionarem os gradientes iônicos também vão ser perdidos e vou ter a libração de cálcio intracelular pra ativar
proteases aí vou direcionar a célula para apoptose. O que essa lista de coisas vai ocasionar na célula renal? A
queda na produção do ATP vai levar ao comprometimento do transporte ativo, portanto, todos os processos
renais que envolvem transporte ativo; vamos ter a síntese de integrinas comprometidas (proteínas de
ancoragem que fazem as células renais se organizarem direitinho), pois também é necessário ATP para isso.
Além disso, eu vou ter a manutenção do citoesqueleto da célula comprometida, a integrina precisa do
citoesqueleto para se ancorar e se manter na posição correta, se o citoesqueleto está desorganizado a integrina
Medicina UFPA D 2015 – Urinário
vai ficar desorganizada, essa desorganização do citoesqueleto causa perda da polaridade celular, pois é
importante eu ter na região apical da célula transportadores, na região basolateral a Na+/K+ ATPase, os
transportadores de glicose, de aminoácido, que foram reabsorvidos à custa do funcionamento da Na+/K+
ATPase. O que acontece se há perda dessa polaridade? Eu passo a ter Na+/K+ ATPase nas duas faces da
membrana, não vou ter mais transporte de sódio resultante para nenhum lado, a célula renal perde a sua função
de reabsorção de sódio por essa perda de polaridade.
Na não-oligúrica vamos observar uma grande formação de urina, mas essa formação de urina vai estar
como uma característica igual ao plasma, pois não tem como remodelar esse filtrado porque os transportadores
estão perdidos na membrana, não tem mais transporte resultante nenhum. Por outro lado, se as integrinas não
ancoram direito as células na posição adequada, começa haver o descolamento dessas células, ocasionando em
micro obstruções dos néfrons, passando a ocupar a luz do néfron, e o liquido (o filtrado) extravasa para o
interstício. Isso é algo que pode ocorrer na IRA oligúrica, uma vez que não chega um volume adequando no final
porque antes disso há obstrução do néfron e extravasamento do líquido para o interstício renal que também vai
favorecer a formação do edema. Logo, a explicação para a necrose das células tubulares e as diferenças entre a
IRA oligúrica e não-oligúrica está relacionada com os efeitos da própria hipóxia, pela falta de ATP, fazendo com
que a célula se desorganize por inteiro seja em relação a mecanismos de transportes, seja pela própria regulação
do epitélio.
(Felipe)
Se a hipóxia é deletéria a reperfusão também é.
O que é reperfusão? É quando a gente reestabelece o aporte sanguíneo em um órgão ou num organismo
que ficou por algum tempo sem receber esse sangue. Por quê? Porque quando ele tá em isquemia ele tá sem
O2, aí a gente faz a reperfusão (que é fazer o sangue perfundir de novo no órgão). Nesse momento vai haver a
chegada ao órgão de muito oxigênio.
Na situação de isquemia temos o ATP sendo totalmente consumido, já que não conseguimos produzir
grande quantidade de ATP na ausência de oxigênio. Então, esse ATP tá sendo consumido e a gerar seus
metabólitos, como adenosina e hipoxantina. Essa hipoxantina vai acumulando, enquanto não tem oxigênio, pois
ela só consegue ser metabolizada na presença de oxigênio. Quando fazemos o processo de reperfusão, retorno
do oxigênio pra o órgão, essa hipoxantina vai ser metabolizada e aí ela vai gerar diversas substancias toxicas
denominadas de espécies reativas de oxigênio ou radicais livres. Então a metabolização da hipoxantina vai gerar:
radical ânion superóxido, peróxido de hidrogênio, radical hidroxila, todos eles altamente deletérios, porque são
moléculas altamente oxidantes que podem lesar ainda mais esse rim que já está debilitado.
Temos enzimas antioxidantes que podem lidar com essas espécies reativas de oxigênio pra cada um delas
temos enzimas, que está representado, essa sódio, significa superóxido deslutase, é uma enzima que usa como
substrato o radical ânion superóxido e converte ele a peróxido de hidrogênio. Em seguida, temos outra enzima
atuando, que é a catalase. A catalase converte o peróxido de hidrogênio em água e oxigênio e aí a gente
consegue neutralizar. Esse peróxido de hidrogênio, se ele não for rapidamente metabolizado, ele pode ser
convertido numa espécie mais tóxica ainda que é o radical hidroxila, uma espécie extremamente oxidativa que
pode oxidar o epitélio renal, bagunçar ainda mais aquela estrutura que já estava bem lesada. Então a própria
reperfusão também pode representar um processo de agravamento do estado patológico. Então a gente tem aí
um campo de estudo bem amplo, por exemplo, pra transplante, porque quando você tira um órgão pra ele ser
transplantado, faz ele entrar em isquemia e depois quando ele é recolocado ele vai ser reperfundido, então a
gente vai ter um processo de formação de espécies reativas de oxigênio. Tem várias linhas da ciência que estão
relacionados com isso, por exemplo manter uma hipotermia para fazer uma reperfusão em temperatura mais
baixa pra diminuir a atividade enzimática e fazer isso aqui acontecer de uma maneira mais lenta. Então, quando
Medicina UFPA D 2015 – Urinário
a gente tem um desbalanço entre espécies reativas de oxigênio e sistema de defesa antioxidante, temos um
estresse oxidativo. Alguma coisa fazendo com que haja um aumento muito grande na geração de espécies pró-
oxidantes, como: radical ânion superóxido, peróxido de hidrogênio, radical hidroxila, sem o aporte adequado de
enzimas antioxidantes ou de moléculas antioxidantes, como a glutationa. Então, como esse desbalanço pra o
lado dos pró-oxidantes, passa a ocorrer danos em macromoléculas. Todo esse quadro reflete uma situação de
estresse oxidativo.
IRA Pós-Renal
Ela vai ser causada pela obstrução de vias acessórias aos rins. Pós-rim. Então, obstrução de ureteres.
Ela pode ser causada:
- Por cálculos renais;
- Por coágulos sanguíneos;
- Por tumores compressivos.
Ou seja, tudo o que pode se acumular aqui nessa região do sistema urinário, causando uma pressão
reflexa na estrutura do rim. Então vai gerar: cólicas renais, alterações urinárias. Pode não ter no início nenhuma
alteração laboratorial e a presença do cálculo desencadear uma reação inflamatória que pode levar a destruição
glomerular. Então, no início é pós-renal, mas a presença do cálculo pode levar a uma reação inflamatória que
pode fazer com que o próprio rim passe a ser lesionado e aí ela pode passar a ser intra-renal também.
O mecanismo dessa IRA: na verdade, como a gente tem obstrução do fluxo sanguíneo aqui, a gente
aumenta a pressão hidráulica dessa via, só que essa pressão hidráulica ela vai refletir lá nos túbulos e na cápsula
de Bowman. Então, vou ter pressão de um lado, pela da filtração. Pressão do outro, por causa da obstrução. A
pressão se anula. Então, vamos ter uma diminuição da taxa de filtração glomerular. Ocorre anulação da pressão
efetiva de ultrafiltração. Com isso, a gente vai ter o processo de filtração parado, porque uma pressão vai anular
a outra. Então, se a gente tem dias de obstrução, 1 ou 2 dois dias, a gente vai ter uma produção local de
vasoconstritores que vai manter essa taxa de filtração glomerular reduzida. Caso persista, ela pode sair dessa
região pós-renal e passar a ser uma IRA renal, porque a gente pode evoluir pra uma necrose tubular aguda,
infecção urinária, que pode levar inclusive à perda do órgão. Então tem que ser tratado esse cálculo, retirado
esse tumor ou o que estiver obstruindo essa via pós-renal. Desfazendo-se essa obstrução a gente tem como
reverter a queda da filtração glomerular.
Diagnóstico da IRA renal: primeiro, o fluxo urinário costuma ser um sintoma que é observado pelo próprio
paciente. Apesar de que um fluxo normal não exclui um diagnóstico de IRA, vocês viram que tem a não oligúrica,
né?! Que também é um tipo de IRA renal. Então, o fluxo urinário fica em torno de 400 mL/dia para menos, se
for uma oligúrica. A concentração de creatinina plasmática também pode ajudar a definir a IRA. Um valor normal
também não exclui a IRA, porque a gente tem valores que podem mudar de acordo com o indivíduo, de acordo
com as características do paciente.
A diferenciação de IRC pode ser feita pela ultrassonografia renal. a gente consegue fazer um diagnóstico
diferencial da pré-renal e renal por aqueles parâmetros que eu mostrei pra vocês de osmolaridade, de relação
de sódio, potássio, de relação de uréia. Então, a gente tem na renal a osmolaridade da urina muito semelhante
a do plasma, na pré-renal, a gente vai ter uma osmolaridade elevada da urina. A razão uréia e creatinina vai ser
diferenciada nos dois tipos de insuficiência renal. A fração de excreção de sódio também vai ser diferente. Vocês
lembram que na IRA renal, a gente não tem mais capacidade do rim de reabsorver o sódio, então a gente começa
a excretar sódio. Outro parâmetro que pode ajudar a fazer esse diagnóstico diferencial. Pode-se fazer um teste
terapêutico corrigindo a volemia. Se a correção da volemia resolver o problema, trata-se de uma IRA pré-renal.
Caso negativo, IRA renal. Então, de novo, um diagnóstico precoce é o que vai levar a um prognóstico mais
favorável.
Medicina UFPA D 2015 – Urinário
Todo esse contexto a creatinina pode ser utilizada como biomarcador, mas vai ser um biomarcador tardio.
Ou seja, quando a gente vê o aumento de creatinina plasmática é porque a lesão já está estabelecida. Então, na
verdade, a gente ainda não tem um marcador ideal pra esse tipo de lesão e existem vários estudos buscando
esse marcador ideal. Então qual seria esse marcador ideal? Que reunisse todas essas características. Rápida
detecção, discernimento entre as diferentes formas de insuficiência renal, que conseguisse identificar a etiologia
(ou seja, a lesão vem de uma isquemia, de uma toxina, vem de sepse), mesurar a gravidade da lesão e ainda a
resposta ao tratamento, esse é o cenário ideal. Ainda não existe uma molécula assim, mas é dentro desse
contexto que ela tá sendo procurada. Moléculas em estudos, além da cistatina C: por exemplo, as lipocalinas
(elas aumentam no plasma e na urina com lesão renal isquêmica ou tóxica, ou seja, elas conseguem classificar a
etiologia). A gente tem moléculas de lesão renal que são proteínas expressas na própria membrana das células
dos túbulos proximais. Se presente na urina, pode indicar lesão tóxica isquêmica. Outra molécula que tá em
estudo é a interleucina 18 (IL-18), que é uma citocina pró-inflamatória sintetizada no túbulo proximal. A
presença na urina vai indicar lesão isquêmica. Isso em modelos animais, não tem dados para seres humanos. A
gente tem a cistatina C, uma pequena proteína que é livremente filtrada, totalmente reabsorvida, sem ser
secretada. Ela vai nos ajudar a ter um diagnóstico mais precoce que a creatinina na queda da taxa de filtração
glomerular.
Então, continua-se nessa busca do marcador ideal.
Insuficiência Renal Crônica (IRC) ou Doença Renal Crônica (DRC)
Em aspectos gerais relacionados a essa doença a gente tem alguns dados. Ela já é tão frequente que já é
consenso que existe um tipo de epidemia mundial dessa insuficiência renal crônica terminal.
O mecanismo inicial do insulto renal pode variar de acordo com a etiologia. Mas os mecanismo de
progressão dessa nefropatia vão ser semelhantes. Vai resultar numa perda progressiva e irreversível de um
grande número de néfrons funcionais. Então, uma característica comum dessa nefropatia crônica é que a lesão
começa devagar. Então, como ela começa devagar um néfron consegue compensar a atividade do néfron que
foi degradado. Um néfron vai compensando a atividade do outro até que chega um momento que o tecido fica
mais necrosado do que funcional e aí que a gente começa a notar os efeitos. O processo de perda acontece ao
longo de anos e esses sintomas só vão aparecer nas fases finais, por causa desses mecanismos adaptativos que
os néfrons exibem. Ela tem diferentes níveis de I a V, determinados pela taxa de filtração glomerular. Então,
quando a gente tem menos de 60 mL/min, de superfície corporal, de taxa de filtração glomerular a gente já
classifica como uma doença renal crônica, quando está abaixo de 30, já tem que entrar com terapia renal
substitutiva e menor que 15 já entra em falência renal.
A partir da terceira década de vida, já é fisiológico diminuir 1mL/min/superfície corporal/ano na taxa de
filtração glomerular. Então, é normal que indivíduos idosos tenham uma redução muito grande na taxa de
filtração glomerular.
- Professora, essa avaliação é feita pela depuração?
- É sim, pela depuração.
- Então, essa medição plasmática é mais uma forma de triagem.
- Exatamente. É uma forma de fazer uma estimativa da taxa de filtração glomerular, quando o indivíduo
ainda não está em ambiente hospitalar pra classifica-lo, se vale a pena evoluir para um processo de análise da
depuração plasmática.
Então, como vai acontecer o mecanismo de progressão dessa nefropatia crônica? A gente vai ter uma
lesão inicial que vai ser oriunda de uma doença de base. Podem ser diferentes tipos de doença. Por exemplo,
hipertensão arterial, diabetes, dislipidemias, tudo isso pode ser o início de um processo de lesão renal de uma
forma lenta e gradual. Aí nesse caso a gente vai ter um processo de perda irreversível de néfrons, mas de forma
bastante gradual. Primeiro um néfron, depois outro, mais outro, e aí os vizinhos vão “segurando as pontas” pra
Medicina UFPA D 2015 – Urinário
que a lesão não seja agravada. Então, essa perda de néfrons vai causar aumento das pressões e fluxos glomerular
e tubular, associado a isso, um aumento de permeabilidade a macromoléculas que vai levar à proteinúria.
A proteinúria é causa e consequência da destruição da estrutura glomerular. Então, a continuidade dessa
proteinúria vai gerar uma inflamação túbulo-intersticial, que vai levar a uma fibrose renal e isso, então, vai levar
à perda de mais néfrons e esse processo se repete.
A gente pode também ter uma lesão tão grave da doença de base que já leva diretamente à fibrose renal
e aí processo cicla nesse sentido.
Então, como vocês viram, podemos ter diferentes patologias que levam ao desenvolvimento desse
processo todo.
A proteinúria, no caso da nefropatia crônica, pode ser um marcador bioquímico de gravidade dessa
nefropatia. Lembrem que quando a gente fala em proteinúria, a gente tem que fazer um monitoramento no
indivíduo. Uma única dosagem de proteinúria não constitui diagnóstico de lesão renal. Ela tem que ser
monitorada, de forma constante, pra gente ver que essa proteinúria é recorrente no indivíduo e ver se ela está
evoluindo ou não.
Nesse caso, na doença renal crônica, como é que a gente vê a uréia e a creatinina? O que acontece com
elas no caso de doença renal crônica? As concentrações vão aumentar em proporção ao grau de néfrons
funcionais. Então a gente pode fazer medidas da sua depuração plasmática e da concentração da creatinina pra
usar, pra gente poder avaliar o grau de insuficiência renal, só que a gente tem que ter em mente que quando o
indivíduo chega no grau de doença renal crônica a gente vai ter aquela secreção exacerbada da creatinina, chega
a ter 60% de secreção nesses casos. Então, isso tem que se ter em mente pra se fazer a análise do resultado
dessa depuração plasmática nesse nível de lesão renal.
Então, pra a própria insuficiência renal crônica, por todas essas características que ficam difíceis de se
interpretar em relação a creatinina na doença renal crônica, a gente tem a falta de um marcador ideal, sendo
um biomarcador simples, de baixo custo e de detecção precoce, porque a gente tem esse problema na taxa de
depuração de creatinina na função renal. Uma pequena secreção tubular de creatinina aumenta
percentualmente conforme a perda de função renal e a gente não tem como confiar nessa coleta, se não estiver
em ambiente hospitalar. Em todos esses casos nós temos as cistatinas C, que é um marcador promissor pra essa
características.
Recapitulação:
A gente viu que a gente pode usar métodos de depuração pra avaliar a taxa de filtração glomerular. Eles
vão elencar que tipo de moléculas pra serem utilizadas pra que possa se avaliar essa depuração quando a gente
não consegue ver diretamente:
- Não reabsorvida;
- Que não seja secretada (que é o que acontece com a creatinina e essa secreção aumenta com o nível de
lesão renal);
- Totalmente filtrada e livremente filtrada (tão livremente quanto o plasma);
Em condições mais aproximadas da normalidade a secreção é pequena e a gente tem aquela
compensação. Lembra que eu falei pra vocês? A técnica que a gente usa pra marcar creatinina plasmática do
criptricato alcalino (não entendi o nome). Ela detecta outras substâncias também. Então, a gente superestima a
creatinina plasmática e a gente também superestima creatinina urinária, porque a gente tem a secreção, então
fica elas por elas e a gente chega a uma taxa aproximada de depuração.
Como a gente tem esses vieses, por exemplo, de coleta adequada não ser apropriada, porque se agente
tem um paciente coletando urina ele pode perder volume urinário. Então a gente tem estratégias pra poder na
prática química fazer algumas estimativas você que teve uma triagem de um indivíduo que vai ali realmente por
método de depuração pra gente ter uma abordagem mais específica dessa taxa de filtração glomerular. Então
Medicina UFPA D 2015 – Urinário
aí a gente faz o quê? Usa a creatinina plasmática. E aí a gente tem uma série de equações que vão fazer a gente
interpretar o dado de creatinina plasmática de uma forma mais apropriada, levando em conta suas
inconveniências, como: massa muscular, idade, sexo, etnia. Então, essas equações.
Quando eu mostrei o gráfico pra vocês, foi demonstrado que um pequeno aumento de creatinina
plasmática representa uma grande diminuição/perda da taxa de filtração glomerular.
Massa muscular: o indivíduo musculoso pode realmente ter uma maior taxa de creatinina plasmática não
por um problema renal, mas sim porque ele produz mais.
Na idade: podemos ser levados a pensar que pelo mais velho ter menos néfrons, vai aumentar a taxa de
creatinina. Mas não é por aí, porque a gente pede massa muscular com a idade. Então, de novo, eu posso ter
uma taxa de creatinina plasmática normal, só que ela pode estar realmente aumentada, não é mesmo? Porque
o indivíduo perdeu massa muscular.
Depois disso falamos da insuficiência renal aguda e crônica e seu diagnóstico diferencial. Na pré-renal eu
tenho o rim funcionando, então tudo o que tu espera de uma atividade renal vai acontecer, os marcadores
bioquímicos vão estar relacionados a uma função renal preservada, ao contrário da intra-renal, aí a gente já vai
ter a osmolaridade da urina semelhante a do plasma, sódio já vai começar a ser perdido, não vai ser mais
reabsorvido, uma série de alterações que já indicam lesão renal e a gente já viu que essa lesão renal está muito
relacionada aos efeitos deletério da hipóxia, que vai fazer todo aquele desarranjo de citoesqueleto, de
integrinas, que vai fazer com que a célula se descole dos seus pontos de fixação na matriz extracelular, podendo
inclusive obstruir os néfrons, o líquido ser extravasado, por isso que a gente acaba tendo uma diminuição do
filtrado na oligúrica e não-oligúrica, então a gente consegue explicar pelos próprios efeitos deletérios da própria
hipóxia.
Vimos também que diferentes tipos de patologia podem desencadear a doença renal crônica e o grande
problema dela é que ela é silenciosa, ela não mostra sintomas nas fases iniciais, os sintomas só vão aparecer nas
fases finais, quando essa compensação que os néfrons conseguem fazer começar a ficar fora de controle, então
aí que começam os sintomas. Por isso ela é tão grave, passa muito tempo silenciosa e só vai aparecer quando
os rins estiverem realmente debilitados.
Medicina UFPA D 2015 – Urinário
Exercícios de fixação
1. Quais as principais características bioquímicas presentes no glomérulo que garantem a formação do
filtrado glomerular livre de células e macromoléculas? Por que isso é clinicamente relevante?
R= As moléculas que formam essa membrana de filtração são carregadas negativamente, impedindo que
proteínas negativas passem, ou seja, repulsão eletrostática de macromoléculas; Poros pequenos e poros de
shunt, que na verdade não são poros simétricos, mas espaços nas grandes fibras de colágeno e proteoglicanos,
essa é a razão de no filtrado ter um concentração pequena, mas presente de proteínas e que podem ser
reabsorvidas pelo epitélio tubular.
2. O processamento do filtrado glomerular ao longo dos segmentos tubulares depende de mecanismos de
transporte através de vias transcelulares e paracelulares. Quais são esses mecanismos? Para cada um dos
mecanismos cite uma proteína envolvida, sua localização tubular e sua função.
R= Via paracelular ocorre quando a reabsorção é através das células e entre as células, e existem diferentes
proteínas transmembrana como claudinas e ocludinas, que fazem diferentes níveis de vedação nessas junções
oclusivas, e é interessante saber que diferentes partes do néfron, conseguem absorver algumas moléculas mais
que outras e isso é controlado pela organização dessas proteínas. Via transcelular ocorre pela ação de
transportadores na parte apical da célula que são dependentes da bomba de sódio e potássio que fica na parte
basolateral das células
3. Frente a isquemia renal qual a porção do néfron seria mais comprometida? Por quê?
R= O túbulo contorcido proximal, porque ele é extremamente dependente da fosforilação oxidativa, que necessita
de O2 para acontecer, uma vez que suas células são ricas em mitocôndrias, pela alta necessidade de ATP, já que
a maior parte da reabsorção de substâncias acontece nele, logo, a fermentação láctica é pouco desenvolvida
nessa área.
4. Estudos demonstram que existe uma correlação positiva entre consumo de oxigênio e taxa de
reabsorção de Na+ pelas células renais. Por que isso ocorre?
R= Quanto mais sódio se transporta, mais oxigênio se necessita, uma vez que pra bomba de sódio e potássio
funcionar necessita de ATP, e a partir disso os transportadores que dependem da entrada de sódio na célula
podem funcionar. Porque se tem mais oxigênio servindo como aceptor de elétrons final na cadeia
transportadora de elétrons, e sem o oxigênio, não se tem o gradiente eletroquímico que ATPsintase precisa para
liberar o ATP que ela sintetizou
5. Explique como as células tubulares proximais regulam a demanda por transporte ativo com a produção
de ATP pela cadeia respiratória.
R= Existe um sinal citosólico que informa para célula que é necessário a produção de ATP como os níveis altos de
ADP e a razão NAD reduzido e NAD oxidado diminuída.
6. De que forma os rins regulam as concentrações de prótons e bicarbonatos no líquido extracelular?
R: Reabsorvendo bicarbonato e excretando hidrogênio. Através da recuperação da carga filtrada de bicarbonato,
secreção de H+ (esses dois processos são pareados) e excreção de água (não deu pra ouvir direito se era
realmente isso) através de ácidos não voláteis ou através da devolução de bicarbonato para o sangue, que havia
sido consumido no tamponamento dos ácidos não voláteis quando eles foram produzidos no sangue. Então são
três processos: reabsorção de bicarbonato, secreção de H+ e produção de novo bicarbonato.
Medicina UFPA D 2015 – Urinário
7. Qual a diferença entre ácidos voláteis e não voláteis?
R: Os voláteis são excretados por via pulmonar e os não voláteis apenas pela via renal. Os voláteis são derivados
da respiração celular, oxidação de combustíveis energéticos: glicose, ácidos graxos, corpos cetônicos, passam
pelo ciclo de Krebs, produz CO2, cadeia transportadora de elétrons e o CO2 é eliminado por via pulmonar. Caso
ele não seja eliminado, ocorre um acréscimo de H+ na corrente sanguínea. Os não voláteis são derivados do
metabolismo de aminoácidos, são rapidamente tamponados, porém é preciso devolver para o sangue o
bicarbonato que foi consumido nesse tamponamento.
8. Qual a importância do tampão fosfato, da amoniogênese e da excreção renal de amônio?
R: Excretar latas concentrações de íons hidrogênio, sem afetar o pH da urina que não pode baixar muito de 4,5.
Quando é preciso excretar uma grande quantidade de ácido não volátil conjuga-se esse ácido com tampões
urinários para evitar que o pH da urina se altere. A amoniogênese, que apresenta duas vias de pensamento. A
mais antiga diz que o íon amônio seria um tampão que pode capturar prótons do líquido tubular para facilitar
sua inclinação. A outra via diz que esse íon amônio é produzido como íon amônio no metabolismo da glutamina,
então não tem como ele conseguir sequestrar íons hidrogênio do líquido tubular e a amoniogênese seria no
interesse da produção de bicarbonato e excreção renal de NH4 para que ele não volte para a corrente sanguínea,
não caia no fígado, pra síntese de uréia (iria produzir dois prótons, anulando os dois bicarbonatos).
9. Quais as respostas renais a nível bioquímico frente a uma acidose metabólica?
R:Na acidose metabólica ocorrerá um aumento da concentração de íons H+. O rim precisará excretar mais H+ e
produzir mais bicarbonato. Isso ocorre por dois processos: aumento de pressão dos transportadores (contra-
transportador Na+/H+) e mudança de célula intercalada B (secretora de bicarbonato) para célula intercalada A
(secretora de H+), por meio troca de posição dos transportadores na membrana. O transportador de bicarbonato
sai da membrana apical e vai para a basolateral e o de prótons sai da basolateral e vai pra apical. Então o
aumento do transportador tem um resultado líquido de aumento da excreção dos prótons, inserção exocitótica
de estoques intracelulares de transportadores na membrana plasmática (Poteínas transportadoras que já estão
sintetizadas e guardadas em vesículas dentro da célula. Essas vesículas abrem na superfície da membrana e
expõe essa proteína que já está pronta), o aumento da amioniogênese irá colocar mais bicarbonato pra corrente
sanguínea, aumento da disponibilidade de tampões urinários (principalmente o fosfato, seu processo de
reabsorção será diminuído para estar mais disponível no líquido tubular servindo como tampão urinário)
10. Ureia e creatinina são marcadores utilizados na avaliação da função renal. Como isso é possível e destaque
possíveis limtações desses marcadores?
R: A ureia e a cretinina sempre são moléculas de primeira escolha para avaliar a função renal, pois sempre estão
tendentes a estarem em grandes concentrações na urina e em pequenas concentrações no sangue. Caso haja
uma descompensação, é indicativo de problema renal. A uréia é a nossa forma de excretar composto
nitrogenado, a creatinina é um metabólito muscular que não tem mais função fisiológica. Uma limitação em
relação à uréia é que sua concentração varia muito de acordo com a alimentação, como ela é um subproduto
da degradação de aminoácidos, caso estejamos em uma dieta rica em aminoácidos, produz-se mais uréia mais
plasmática sem problema renal, pois haverá também um aumento de excreção, por isso é importante fazer
sempre uma análise comparativa da presença da uréia na urina e no plasma. Em relação à creatinina suas
limktações são massa muscular elevada, um halterofilista tem muito mais creatinina plasmática do que uma
pessoa que não é musculosa, porém ele irá excretar mais, portanto assim como no caso da uréia deve-se analisar
a concentração de creatinina tanto no plasma quanto na urina.
11. Explique os mecanismos básicos de instalação da proteinúria relacionando com seu significado clínico:
Aumento da permeabilidade glomerular não seletiva. Significado clínico: proteinúria de média intensidade à
proteinúria maciça podendo chegar a uma síndrome nefrótica.
Medicina UFPA D 2015 – Urinário
Aumento da permeabilidade glomerular seletiva. Significado clínico: proteinúria média, os poros estão íntegros,
porém houve perda de carga negativa, repulsão eletrostática, logo passam apenas proteínas pequenas que
antes eram repelidas pela carga negativa.
Reabsorção tubular. Significado clínico: proteinúria de baixa intensidade, porque vai ser equivalente à presença
de proteínas no filtrado.
Imunoglobulinas. Significado clínico: não são causas renais, ocorre proteinúria decorrente de filtração de
proteínas anômalas, malformadas por outra patologia, como mioloma múltiplo. Formam imunoglobulinas com
deficientes, menores, com cargas alteradas, que conseguem passar através dos poros. Pode-se chegar a uma
proteinúria maciça, atingindo níveis nefróticos, porém não é caracterizado como síndrome nefrótica porque não
há hipoalbuminemia, há muita proteína no sangue, mas nenhuma vai ser albumina, serão as imunoglobulinas
malformadas.
Medicina UFPA D 2015 – Urinário
You might also like
- Série Eletroquímica - o Caso Dos MetaisDocument5 pagesSérie Eletroquímica - o Caso Dos MetaisSaraFDRodriguesNo ratings yet
- mt-1009 - SulfitoDocument12 pagesmt-1009 - Sulfitopamelarayelle50% (2)
- Materiais Ortodontia EssenciaisDocument3 pagesMateriais Ortodontia EssenciaisBruna SouzaNo ratings yet
- Catalogo de MangotesDocument8 pagesCatalogo de MangotesIvo NunesNo ratings yet
- Aulas à distância de Química sobre nomenclatura de compostos orgânicosDocument6 pagesAulas à distância de Química sobre nomenclatura de compostos orgânicosANDRESSA MORAIS WALDOWNo ratings yet
- Anais Do Congresso de AbracorDocument336 pagesAnais Do Congresso de AbracorRosangelaReis100% (2)
- Ácidos, alcalis e solventes orgânicosDocument14 pagesÁcidos, alcalis e solventes orgânicosCanchale JoseNo ratings yet
- Relatorio de Tanino @@@Document14 pagesRelatorio de Tanino @@@Diane JorgeNo ratings yet
- Ficha de Exercícios de Química OrgânicaDocument3 pagesFicha de Exercícios de Química OrgânicabrgloriaNo ratings yet
- Solubilidade e Insaturação em LipidiosDocument2 pagesSolubilidade e Insaturação em LipidiosFelipe Assis100% (1)
- Revisão GeralDocument12 pagesRevisão GeralFrancisco nettoNo ratings yet
- Biologia - Fascículo 05 - Fisiologia VegetalDocument10 pagesBiologia - Fascículo 05 - Fisiologia VegetalConcurso Vestibular100% (4)
- Fósforo: elemento químico essencial na vidaDocument20 pagesFósforo: elemento químico essencial na vidalinynhaline0% (2)
- Mapa mental sobre a química orgânicaDocument1 pageMapa mental sobre a química orgânicaDaniela Correia FernandesNo ratings yet
- Artigo Da Glicoproteina P PDFDocument6 pagesArtigo Da Glicoproteina P PDFLuana CarvalhoNo ratings yet
- Estudo de plantas medicinais da família AsteraceaeDocument25 pagesEstudo de plantas medicinais da família AsteraceaeHemerson PataxóNo ratings yet
- Aula 4 - Transcrição e TraduçãoDocument40 pagesAula 4 - Transcrição e Traduçãolesianelemoss0% (1)
- 5 - Prática #5 - Síntese e Purificação Do Ácido Acetilsalicílico (Aspirina)Document5 pages5 - Prática #5 - Síntese e Purificação Do Ácido Acetilsalicílico (Aspirina)Fedegos_tosoNo ratings yet
- COTEMOL BDS/1 evita amarelecimento tecidos poliésterDocument3 pagesCOTEMOL BDS/1 evita amarelecimento tecidos poliésterJosé Augusto MarquesNo ratings yet
- Acidez Do LeiteDocument3 pagesAcidez Do LeiteMauroArantesNo ratings yet
- AnorexigenosDocument12 pagesAnorexigenosJordania De OliveiraNo ratings yet
- Pneumonia UpdateDocument74 pagesPneumonia UpdateTalita MeloNo ratings yet
- IsomeriaDocument7 pagesIsomeriaNeide Amada Por DeusNo ratings yet
- Identificação Dos PlásticosDocument16 pagesIdentificação Dos Plásticosmafalda_silva92100% (3)
- Exercícios de Química Orgânica com Fórmulas EstruturaisDocument6 pagesExercícios de Química Orgânica com Fórmulas EstruturaisLuiz Carlos Soares Fernandes0% (1)
- Biosíntese da escopoletina e escopolina em mandioca na deterioração pós-colheita: isomerização E-ZDocument41 pagesBiosíntese da escopoletina e escopolina em mandioca na deterioração pós-colheita: isomerização E-ZInaiara CasapulaNo ratings yet
- 5 OxireducaoDocument36 pages5 OxireducaoGleison Paulino GonçalvesNo ratings yet
- Síntese e Purificação da AcetanilidaDocument4 pagesSíntese e Purificação da AcetanilidaFedegos_tosoNo ratings yet
- Lista 03 PQFDocument7 pagesLista 03 PQFHeitor BarrosNo ratings yet
- Formulário - Agentes Químicos Levantamento CampiDocument12 pagesFormulário - Agentes Químicos Levantamento CampiDemetrio de AbreuNo ratings yet