Professional Documents
Culture Documents
Manual Civil 2014 2 B 1 PDF
Uploaded by
Daniel Gastañaduí YicaOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Manual Civil 2014 2 B 1 PDF
Uploaded by
Daniel Gastañaduí YicaCopyright:
Available Formats
Química General - Laboratorio
MANUAL DE PRÁCTICAS DE
QUÍMICA GENERAL
ALUMNO(A):…………………………………………
DÍA:………………………HORA:…..…….....……
Ing. Víctor A. Campos Linares Período 2014-20
1
Química General - Laboratorio
Ing. Víctor A. Campos Linares Período 2014-20
2
Química General - Laboratorio
ÍNDICE
PRÓLOGO....................................................................................................04
Normas de seguridad e higiene en el laboratorio de química.................................05
PRIMERA PARTE
SEMINARIO Nº 01. Nomenclatura inorgánica de compuestos binarios
SEMINARIO Nº 02. Nomenclatura inorgánica de compuestos ternarios
PRÁCTICA Nº 01 (Semana 03)......................................................................19
Reconocimiento y manipulación de materiales y equipos de laboratorio.
PRÁCTICA Nº 02 (Semana 04)..................................................................... 25
Propiedades físicas de la materia.
PRÁCTICA Nº 03 (Semana 05)...................................................................... 31
Separaciones físicas.
PRÁCTICA Nº 04 (Semana 06)...................................................................... 37
Conductividad eléctrica y solubilidad.
SEMINARIO Nº 03. (Semana 07). Hoja de ejercicios: Aritmética química
SEGUNDA PARTE
PRÁCTICA Nº 05 (Semana 09)…................................................................... 43
Reacciones químicas.
PRÁCTICA Nº 06 (Semana 10)...................................................................... 51
Reacciones redox.
PRÁCTICA Nº 07 (Semana 11)...................................................................... 55
Rendimiento porcentual de una reacción química.
PRÁCTICA Nº 08 (Semana 12)...................................................................... 59
Preparación de soluciones.
PRÁCTICA Nº 09 (Semana 13)...................................................................... 65
Análisis de aguas.
A. Determinación de la dureza total en el agua.
B. Determinación de sólidos totales.
PRÁCTICA Nº 10 (Semana 14)...................................................................... 77
Determinación del pH.
SEMINARIO Nº 04. (Semana 15). Hoja de ejercicios: Reacciones, estequiometría y
soluciones.
APÉNDICE 01: Autoevaluaciones...................................................................83
APÉNDICE 02: Hoja de ejercicios. Tabla Periódica y tabla de conversiones….105
REFERENCIAS BIBLOGRÁFICAS...................................................................107
Ing. Víctor A. Campos Linares Período 2014-20
3
Química General - Laboratorio
PRÓLOGO
Este manual nace con la idea de ser un texto de apoyo al trabajo
experimental de la asignatura de Química General que se imparte en la Escuela
Profesional de Ingeniería Civil. En él los estudiantes encontrarán un abanico de
prácticas que les permitirá adquirir experiencia en las situaciones más
habituales de la vida diaria.
Cada una de las prácticas descritas en este manual está estructurada en
08 partes: en primer lugar, las capacidades que se pretenden alcanzar con el
desarrollo de la práctica. Tras ellos se incluye un breve y conciso fundamento
teórico del por qué se va a realizar. A continuación, se enumera el material,
equipo y reactivos necesarios para realizar el experimento. Seguidamente se
detalla el procedimiento experimental y luego se presenta un informe con un
apartado de cálculos y resultados donde el alumno anota todos los resultados
obtenidos. Luego elabora las conclusiones, responde a un cuestionario y escribe
toda la bibliografía consultada para elaborar su informe.
También se ha incluido a manera de introducción un capítulo de seguridad
en el laboratorio y procedimientos de actuación en caso de accidente que es
conveniente leer antes de iniciarse en el trabajo propiamente dicho.
Al final del manual se ha incluido un apéndice con hojas de ejercicios
relacionadas con la parte teórica de la asignatura, así como una tabla de
conversiones de unidades y otra con las masas atómicas de los principales
elementos.
Ing. Víctor A. Campos Linares Período 2014-20
4
Normas de Seguridad
NORMAS DE SEGURIDAD E HIGIENE EN EL
LABORATORIO DE QUÍMICA
Normas referentes a las instalaciones
1. Las ventanas y puertas han de abrir adecuadamente, ya que en caso de humos
excesivos es necesaria la máxima ventilación y en caso de incendio, la mínima.
2. Las mesas, sillas taburetes, suelos, etc., y el mobiliario en general deben estar en
buen estado para evitar accidentes.
3. Los grifos de agua y los desagües no deben tener escapes que hagan resbaladizo el
suelo y pudran la madera. Los desagües deben permitir bien el paso de agua.
4. Los enchufes o cables eléctricos no deben estar rotos o pelados; en caso de que sea
así deben sustituirse inmediatamente o protegerse para que no puedan tocarse.
Nunca deben ir por el suelo de forma que se puedan pisar.
5. Los armarios y estanterías deben ofrecer un almacenamiento para aparatos y
productos químicos y estar siempre en perfecto orden.
Normas personales
1. Cada grupo se responsabilizará de su zona de trabajo y de su material.
2. La utilización del mandil es muy conveniente, ya que evita que posibles derrames
de sustancias químicas lleguen a la piel.
3. Es muy aconsejable, si se tiene el pelo largo, llevarlo recogido.
4. En el laboratorio no se podrá fumar, ni tomar bebidas, ni comidas.
Normas referentes al orden
1. Las sustancias tóxicas permanecerán en armario con llave.
2. Es imprescindible la limpieza del laboratorio, de su instrumental y utensilios, así
como que esté ordenado.
3. En las mesas de laboratorio o en el suelo, no pueden depositarse prendas de
vestir, apuntes, etc., que pueden entorpecer el trabajo.
Normas referentes a la utilización de productos químicos
1. Antes de utilizar un determinado compuesto, asegurarse bien de que es el que se
necesita; para ello leeremos, si es preciso un par de veces, el rótulo que lleva el
frasco.
2. Como regla general, no coger ningún producto químico. El profesor los
proporcionará.
3. No devolver nunca a los frascos de origen los sobrantes de los productos utilizados
sin consultar al profesor.
4. Es de suma importancia que cuando los productos químicos de desecho se viertan
en las pilas de desagüe, aunque estén debidamente neutralizados, enseguida
circule por el mismo abundante agua.
5. No tocar con las manos, y menos con la boca, los productos químicos.
6. No pipetear con la boca los productos tóxicos. Utilizar la bomba manual o una
bombilla de succión.
7. Los ácidos requieren un cuidado especial. Cuando queramos diluirlos, nunca
echaremos agua sobre ellos; siempre al contrario, es decir, ácido sobre el agua.
8. Los productos inflamables no deben estar cerca de fuentes de calor, como estufas,
hornos, radiadores, etc.
Ing. Víctor A. Campos Linares Período 2014-20
5
Normas de Seguridad
9. Cuando se vierta cualquier producto químico debe actuarse con rapidez, pero sin
precipitación.
10. Si te cae cualquier ácido o producto corrosivo, lávate inmediatamente con mucha
agua y avisa al profesor.
11. Al preparar cualquier disolución, se colocará en un frasco limpio y rotulado
convenientemente.
Normas referentes a la utilización del material de vidrio
1. Cuidado con los bordes y puntas cortantes de tubos u objetos de vidrio. Alisarlos al
fuego. Mantenerlos siempre lejos de los ojos y de la boca.
2. El vidrio caliente no se diferencia a simple vista del vidrio frio. Para evitar
quemaduras, dejarlo enfriar antes de tocarlo (sobre ladrillo, arena, planchas de
material aislante).
3. Las manos se protegerán con guantes o trapos cuando se introduzca un tapón en
un tubo de vidrio.
Normas referentes a la utilización de balanzas
1. Cuando se determinen masas de productos químicos con balanzas, se colocará un
papel o "luna de reloj" para evitar el ataque de los platos por parte de sustancias
corrosivas.
2. Se debe evitar cualquier perturbación que conduzca a un error, como vibraciones
debidas a golpes, aparatos en funcionamiento, soplar sobre los platos de la
balanza, etc.
Normas referentes a la utilización de gas
1. El uso del gas butano requiere un cuidado especial: si se advierte su olor, cerrar la
llave y avisar al profesor.
2. Si se vierte un producto inflamable, córtese inmediatamente la llave general de gas
y ventilar por un largo tiempo el local.
Sustancias químicas peligrosas
Las sustancias químicas se clasifican, en función de su peligrosidad, en:
Explosivos
Sustancias y preparados que pueden explosionar bajo el efecto de una llama.
Comburentes.
Sustancias y preparados que, en contacto con otros, particularmente con los
inflamables, originan una reacción fuertemente exotérmica.
Extremadamente inflamables
Sustancias y productos químicos cuyo punto de ignición sea inferior a 0°C, y su
punto de ebullición inferior o igual a 35°C.
Fácilmente inflamables
Se definen como tales:
Sustancias y preparados que, a la temperatura ambiente, en el aire y sin aporte de
energía, puedan calentarse e incluso inflamarse.
Sustancias y preparados en estado líquido con un punto de ignición igual o
superior a 0°C e inferior a 21°C.
Ing. Víctor A. Campos Linares Período 2014-20
6
Normas de Seguridad
Sustancias y preparados sólidos que puedan inflamarse fácilmente por la acción
breve de una fuente de ignición y que continúen quemándose o consumiéndose
después del alejamiento de la misma.
Sustancias y preparados gaseosos que sean inflamables en el aire a presión
normal.
Sustancias y preparados que, en contacto con el agua y el aire húmedo,
desprendan gases inflamables en cantidades peligrosas.
Inflamables
Sustancias y preparados cuyo punto de ignición sea igual o superior a 21°C e
inferior a 55°C.
Muy tóxicos
Sustancias y preparados que por inhalación, ingestión o penetración cutánea
puedan entrañar riesgos graves, agudos o crónicos, e incluso la muerte.
Nocivos
Sustancias y preparados que por inhalación, ingestión o penetración cutánea
puedan entrañar riesgos de gravedad limitada.
Corrosivos
Sustancias y preparados que en contacto con los tejidos vivos puedan ejercer sobre
ellos una acción destructiva.
Irritantes
Sustancias y preparados no corrosivos que por contacto inmediato, prolongado o
repetido con la piel o mucosas pueden provocar una reacción inflamatoria.
Peligrosos para el medio ambiente
Sustancias y preparados cuya utilización presente o pueda presentar riesgos
inmediatos o diferidos para el medio ambiente.
Carcinógenos
Sustancias y preparados que por inhalación, ingestión o penetración cutánea
puedan producir cáncer o aumento de su frecuencia.
Teratogénicos
Sustancias y preparados que por inhalación, ingestión o penetración cutánea
puedan inducir lesiones en el feto durante su desarrollo intrauterino.
Mutagénicos
Sustancias y preparados que por inhalación, ingestión o penetración cutánea
puedan producir alteraciones en el material genético de las células.
Algunas de estas sustancias se reflejan en el etiquetado de los productos químicos
mediante un símbolo o pictograma, de manera que se capte la atención de la
persona que va a utilizar la sustancia.
Ing. Víctor A. Campos Linares Período 2014-20
7
Normas de Seguridad
Ing. Víctor A. Campos Linares Período 2014-20
8
Seminario Nº 01 y 02
SEMINARIO N° 01 Y 02
FUNCIONALIDAD Y NOMENCLATURA INORGÁNICA
1.- Función química: Conjunto de sustancias que poseen estructura y propiedades químicas
similares; por ejemplo:
Óxidos: MgO, Na2O, Cl2O7, etc.
Hidróxidos: LiOH, Ca(OH)2, Al(OH)3, etc.
Ácidos: HCl, H2SO4, HNO3, etc.
Sales: NaCl, FeSO4, AlPO4, etc.
Hidruros: KH, CH4, CaH2, etc.
2.- Número o estado de oxidación: Es el número de electrones que gana o pierden los
elementos para formar un compuesto; así:
Fe3+ + O2- Fe2O3
3.- Estados de oxidación de los principales elementos: Existe una correlación definida
entre los números de oxidación y los grupos donde están ubicados los elementos en la
tabla periódica; así:
IA IIA IIIA IVA VA VIA VIIA
Li Be B C N S Cl
Na Mg Al Si P Te Br
K Ca I
Ba +4,+2 +5,+3,+1 +6,+4,+2 +7,+5,+3,+1
+1 +2 +3 -4 -3 -2 -1
Otros metales de interés:
Ag Cd, Zn Cu, Hg Au Fe, Co, Ni Sn, Pb
+1 +2 +1, +2 +1, +3 +2, +3 +2, +4
Casos especiales:
Mn +2 +3 +4 +6 +7
Metal No metal
Cr +2 +3 +6
-2 O2- En la mayoría de compuestos
Oxígeno
-1 O2-2 En los peróxidos
+1 H+ En la mayoría de los compuestos
Hidrógeno
-1 H- En los hidruros metálicos
4.- Reglas para asignar estados de oxidación:
a) Los elementos libres o sin combinar tienen el cero, como estado de oxidación; ejemplo:
Na, Fe, Ca, B, Al, Cl2, O2, N2, Br2, I2, S8, etc.
b) La suma algebraica de los números de oxidación de todos los elementos de un compuesto
neutro es igual a cero; ejemplo:
Determine el estado de oxidación del elemento subrayado, Mg3(PO4)2
(3)(+2) + (2)(X) + (8)(-2) = 0
X= +5 (Estado de oxidación del P)
Ing. Víctor A. Campos Linares Período 2014-20
9
Seminario Nº 01 y 02
c) La suma algebraica de los números de oxidación de todos los elementos que forman un
IÓN igual a la carga del ión; ejemplo:
Determine el estado de oxidación del elemento subrayado, (Cr2O7)2-
(2)(X) + (7)(-2) = -2
X = +6 (Estado de oxidación del Cr)
5.- Nomenclatura:
a) Tradicional:
Para los E. de O. positivos
04 Per…ico 03 ico 02 01
ico
Estados ico Estados oso Estados Estado
ico
de oso de de de
Hipo…oso oso
oxidación Hipo…oso oxidación oxidación oxidación
Ejemplos:
Ni2O3 Óxido niquélico
Cl2O7 Anhidrido perclórico
Para los E. de O. negativos se utiliza la terminación URO; por ejemplo en los
aniones:
Br- Ión bromuro I Ión yoduro
Cl- Ión cloruro N 3- Ión nitruro
2-
F- Ión fluoruro S Ión sulfuro
2-
H- Ión hidruro O Ión óxido
Ejemplos:
Ca3N2 Nitruro de calcio o nitruro cálcico
Al2S3 Sulfuro de aluminio o sulfuro alumínico
b) Stock: Uso de los números romanos, que se obvia cuando el elemento tiene un solo
estado de oxidación; ejemplo:
Fe2O3 Óxido de hierro (III)
CaO Óxido de calcio
Cu(OH) Hidróxido de cobre (I)
c) Sistemática: Uso de los prefijos de cantidad; así:
mono di tri tetra penta hexa hepta octa nona deca
1 2 3 4 5 6 7 8 9 10
Ejemplos:
Fe2O3 Trióxido de dihierro Cl2O5 Pentóxido de dicloro
Li2O Monóxido de dilitio SF6 Hexafluoruro de azufre
CO2 Dióxido de carbono SO2 Dióxido de azufre
Ing. Víctor A. Campos Linares Período 2014-20
10
Seminario Nº 01 y 02
6.- Compuestos binarios:
a) Óxidos metálicos
b) Óxidos no metálicos
c) Peróxidos
d) Ácidos hidrácidos
e) Sales (haloideas y de los ácidos hidrácidos)
f) Hidruros (metálicos y no metálicos)
7.- Compuestos ternarios:
a) Hidróxidos
b) Ácidos oxácidos
c) Sales oxisales
Ing. Víctor A. Campos Linares Período 2014-20
9
Seminario Nº 01 y 02
HOJA DE EJERCIOS Nº 01-A
UNIDAD I: NOMENCLATURA DE QUÍMICA INORGÁNICA – COMPUESTOS BINARIOS
1.- Para establecer la fórmula de cada compuesto, combine cada catión con el anión
como muestra el ejemplo, teniendo en cuenta el cruce de los estados de oxidación.
- -
Cl O2- S2- Br
CuCl2
Cu2+
Cloruro cúprico
Al3+
K+
Pb4+
Ni2+
H+
Fe3+
Na+
Cd2+
Ba2+
Ni2+
Cr2+
Ing. Víctor A. Campos Linares Período 2014-20
10
Seminario Nº 01 y 02
2. Nombrar los siguientes compuestos binarios e indicar la función química correspondiente:
Fórmula Función Química Nombre del compuesto
K2O2 Peróxido Peróxido de potasio
Na2O
CaO
H2S(ac)
Fe2O3
PbO2
PbI2
Cl2O7
NiO
ZnCl2
N2O5
Li2O
Na2O2
SO3
FeO
HCl(g)
HI (ac)
HgO
Fe2S3
SO2
HF(g)
FeS
FeCl3
Hg2Cl2
CdI2
NaH
NH3
Mn2O3
Ing. Víctor A. Campos Linares Período 2014-20
11
Seminario Nº 01 y 02
3. Formular los siguientes compuestos químicos binarios:
Nombre Fórmula Nombre Fórmula
Bromuro de bario BaBr2 Óxido cúprico CuO
Óxido de nitrógeno (III) Óxido de plomo (IV)
Anhidrido clórico Sulfuro de cromo (II)
Cloruro de hierro (II) Anhídrido carbónico
Sulfuro de calcio Sulfuro de hierro (III)
Óxido de cobre (I) Cloruro potásico
Anhídrido sulfuroso Peróxido de sodio
Óxido de carbono (II) Yoduro de mercurio (I)
Óxido de mercurio (II) Nitruro de litio
Anhidrido perbrómico Peróxido de litio
Bromuro de hidrógeno Óxido de bromo (V)
Anhídrido clórico Anhídrido hipoyodoso
Peróxido de hidrógeno Metano
Anhídrido cloroso Anhidrido sulfuroso
Peróxido sódico Óxido de nitrógeno (V)
Óxido de plomo (II) Yoduro de mercurio (I)
Anhídrido nítrico Peróxido de potasio
Cloruro de hidrógeno Óxido de yodo (I)
Anhídrido brómico Yoduro de zinc
Óxido de manganeso (II) Anhídrido peryódico
Peróxido de calcio Sulfuro de aluminio
Anhídrido carbonoso Peróxido de calcio
Óxido de yodo (V) Bromuro de zinc
Anhídrido yódico Óxido de calcio
Sulfuro férrico Anhídrido carbónico
Ing. Víctor A. Campos Linares Período 2014-20
12
Seminario Nº 01 y 02
HOJA DE EJERCIOS Nº 01- B
UNIDAD I: NOMENCLATURA DE QUÍMICA INORGÁNICA – COMPUESTOS TERNARIOS
1. Nombrar los siguientes iones:
Ión Nombre del ión Ión Nombre del ión
- 2-
NO2 Nitrito Cr2O7
2-
SO4 PO43-
MnO4- NO3-
ClO3- SO32-
CO32- ClO - Hipoclorito
HCO3- CrO42-
IO2- BrO3-
BrO - BrO4-
2. Determine el estado de oxidación solamente del elemento en negrita en los siguientes
compuestos:
Compuesto Estado de Oxidación
KMnO4 (1)(+1) + (1)(x) + (4)(-2) = 0 x = +7
Ca3(PO4)2 (3)(+2) + (2)(x) + (8)(-2) = 0 x = +5
H2SO4
NaClO3
Cu2SO4
KIO
HNO2
AlPO4
HNO3
HClO
H2SO3
CaSO4
H2CO3
HClO4
K3PO4
Ing. Víctor A. Campos Linares Período 2014-20
13
Materiales y Equipos de Laboratorio
3. Para establecer la fórmula de cada compuesto, combine cada catión con el anión
como muestra el ejemplo, teniendo en cuenta el cruce de los estados de
oxidación.
NO3- SO42- PO43- BrO3-
AgNO3
Ag+ Nitrato de plata
CuSO4
Cu2+ Sulfato cúprico
AlPO4
Al3+ Fosfato de aluminio
Mg(BrO3)2
Mg2+ Bromato de magnesio
Fe3+
K+
Au3+
Li+
Cd2+
Ba2+
Ni3+
Ca2+
Na+
Ing. Víctor A. Campos Linares Período 2014-20
19
Materiales y Equipos de Laboratorio
4. Nombrar los siguientes compuestos ternarios e indicar la función química:
Fórmula Función Química Nombre del compuesto
Fe(OH)2 Hidróxido Hidróxido ferroso
K3PO4
Na2CO3
HNO2
HClO4
HNO3
Na 2SO4
MgCO3
NaOH
H3PO4
Mg3(PO4)2
HIO3
NaClO3
H2SO4
HIO
HBrO2
CuSO4
LiNO2
HClO
NaNO3
Ca3(PO4)2
Cu2SO4
CaSO4
KIO
H2CO3
Mg SO4
Al(OH)3
HBrO3
KNO2
NaClO
LiNO3
Zn3(PO4)2
CuSO4
BaSO4
KClO
Li3PO4
Al2(SO4)3
HClO
KMnO4
K2Cr2O7
Ing. Víctor A. Campos Linares Período 2014-20
20
Materiales y Equipos de Laboratorio
5. Formular los siguientes compuestos químicos ternarios:
Nombre Fórmula Nombre Fórmula
Carbonato de bario BaCO3 Hidróxido de plomo (IV)
Sulfato cúprico Sulfato de calcio
Ácido nítrico Ácido perclórico
Hidróxido de cobre (I) Hidróxido de amonio
Nitrito de sodio Clorato de potasio
Permanganato de potasio Fosfato cúprico
Hipoclorito de sodio Carbonato de calcio
Ácido nitroso HNO2 Sulfato de aluminio
Hidróxido de plomo (II) Sulfito de calcio
Ácido brómico Hidróxido de magnesio
Hidróxido ferroso Nitrato de calcio
Bromato de potasio Dicromato de potasio
Hipoclorito de litio Fosfato cuproso
Ácido sulfúrico Fosfato alumínico
Nitrato mercurioso Nitrato mercúrico
Sulfato cálcico Bicarbonato de sodio
Ácido carbónico Sulfato de cobre (II)
Hidróxido magnésico Dicromato lítico
Nitrato de plomo (II) Fosfato sódico
Cromato de potasio Ácido sulfúrico
Sulfito de cobre (I) Sulfito cúprico
Ing. Víctor A. Campos Linares Período 2014-20
21
Materiales y Equipos de Laboratorio
PRÁCTICA N° 01
RECONOCIMIENTO Y MANIPULACIÓN DE MATERIALES Y
EQUIPOS DE LABORATORIO
I. CAPACIDADES:
a) Reconoce los materiales y equipos que se usan en un laboratorio de Química.
b) Manipula y utiliza apropiadamente los materiales y equipos de laboratorio.
c) Mide con precisión masas y volúmenes de diferentes muestras.
II. FUNDAMENTO TEÓRICO:
Los experimentos realizados durante el desarrollo de una práctica de laboratorio
constituyen una oportunidad para familiarizarse con los hechos y leyes que rigen
el desarrollo de las ciencias químicas, conlleva a realizar mediciones de masa de
objetos y reactivos con poca o rigurosa precisión, utilizando para ello diferentes
tipos de balanza.
También se efectúan mediciones de volúmenes de líquidos en forma aproximada o
con mayor precisión y por último también mediciones de propiedades físicas y
químicas con la ayuda de materiales auxiliares y equipos de laboratorio, acoplados
adecuadamente.
La exactitud se refiere a la proximidad entre un valor medido y un valor correcto y
la precisión se refiere a la cercanía entre valores medidos; idealmente, todas las
mediciones deberían ser exactas y precisas.
Descripción de los principales materiales y equipos de laboratorio
a) Para medición de masa
Debemos conocer claramente la diferencia de los conceptos de masa y peso. Masa
es una medida de cantidad de materia invariable, y el peso que corresponde a la
atracción gravitacional está sujeto a la variación geográfica, con la altitud y la
latitud. Se relacionan por la expresión conocida:
W= m.g = masa x aceleración de la gravedad (9,81 m /seg2)
En el laboratorio de química, se pueden encontrar varios tipos de balanzas que
pueden ser mecánicas o eléctricas.
Balanza de triple brazo : Sensibilidad = ± 0,1
Balanza de dos platillos : Sensibilidad = ± 0,1 g
Balanza de precisión : Sensibilidad = ± 0,001 g
Balanza analítica : Sensibilidad = ± 0,0001 g
b) Para medición de volúmenes
Para la determinación de volúmenes líquidos se usan diferentes instrumentos de
vidrio.
Ing. Víctor A. Campos Linares Período 2014-20
22
Materiales y Equipos de Laboratorio
Menisco: La superficie de un líquido no es horizontal, puede ser cóncava o
convexa.
Lectura exacta
Pipetas graduadas: Existen de diversos volúmenes de 1mL, 5mL, 10mL
Buretas: Se utilizan para realizar titulaciones.
Fiolas o matraces volumétricos: Sirven para la preparación de soluciones.
Lectura aproximada
Probeta o cilindros graduados.
Matraz Erlenmeyer.
Vaso de precipitados.
c) Equipo para la separación de mezclas
Separación líquido-líquido
Destilación.- Operación para separar los componentes de una mezcla
homogénea líquida (solución); los cuales tienen puntos de ebullición
marcadamente diferentes.
Equipo para destilación simple
- Balón Engler
- Tubo refrigerante o condensador
- Termómetro
- Vaso de precipitados
- Medio de calentamiento
Equipo para destilación por arrastre con vapor
- Matraz Erlenmeyer
- Balón Engler
- Tubo refrigerante
- Vaso de precipitados
- Medio de calentamiento
Decantación.- Operación empleada para separar los componentes de una
mezcla líquida heterogénea.
- Embudo de decantación
- Vaso de precipitados
Ing. Víctor A. Campos Linares Período 2014-20
23
Materiales y Equipos de Laboratorio
Separación sólido – líquido
Filtración.- Es la separación de sólidos suspendidos en un líquido,
haciendo pasar la mezcla a través
de un papel de filtro.
- Papel de filtro
- Embudo simple de vidrio
- Matraz Erlenmeyer
Sedimentación.- Operación para separar sólidos suspendidos en un
líquido, al dejar en reposo la mezcla. Se realiza en los vasos de
precipitados. La fuerza gravitacional hará que los sólidos más pesados
vayan primero al fondo del recipiente y al final los livianos. Se emplea
este método para tratar muestras grandes.
- Vaso de precipitados
- Gotero capilar
Centrifugación.- Operación que se basa en el aumento de la velocidad
de sedimentación de las partículas, incrementando la aceleración de la
gravedad, debido al aumento de la velocidad rotacional.
- Centrífuga
- Tubos de centrífuga
- Gotero capilar
Vaporización.- Operación que consiste en calentar una mezcla hasta
lograr la eliminación parcial o total del disolvente, según se requiera.
- Cápsula de porcelana
- Medio de calefacción (mechero con alcohol)
- Trípode
- Rejilla con asbesto
- Luna de reloj
d) Material para reacciones químicas
- Balón simple
- Tubos de ensayo
e) Material para calentamiento
- Mechero Bunsen - Estufa
- Mechero con alcohol - Horno de mufla
- Cocina eléctrica
f) Material auxiliar
- Pinzas - Triángulo refractario
- Soporte universal - Rejilla porta tubos de
- Nuez ensayo
- Grapa - Varilla de agitación
- Trípode - Espátula
Ing. Víctor A. Campos Linares Período 2014-20
24
Materiales y Equipos de Laboratorio
- Rejilla con asbesto - Luna de reloj
- Frasco lavador
Ing. Víctor A. Campos Linares Período 2014-20
20
Materiales y Equipos de Laboratorio
INFORME DE PRÁCTICA Nº 01
Alumno: .................................................................................. Turno: ............
V. Dibuja y/o da nombre a lo que se indica:
a) Equipos para determinar la masa:
b) Material para determinar:
Volumen exacto
Volumen aproximado
c) Componentes del equipo de destilación, dando nombre a sus partes:
Ing. Víctor A. Campos Linares Período 2014-20
20
Materiales y Equipos de Laboratorio
d) Dibuje y nombre a otros materiales presentados en la práctica.
VI. CONCLUSIONES:………………………………………………………………………….…
……………………………………………………………………………………………………..…
.……………………………………………………………………………………………………..
VII. CUESTIONARIO:
a) ¿Cuál es la diferencia entre masa y peso?
b) ¿Qué diferencia encuentras en el procedimiento de pesar un objeto cualquiera y
pesar una cantidad determinada de una sustancia?
c) ¿Qué es el menisco de un líquido? Dibuje una superficie cóncava y otra convexa
en una probeta.
d) ¿Cuál es la diferencia de exactitud y precisión?
VIII. BIBLIOGRAFÍA:
…………………………………………………………………………………………………
……………………………………………………………………………………………….
Ing. Víctor A. Campos Linares Período 2014-20
21
Propiedades Físicas de la Materia
PRÁCTICA N° 02
PROPIEDADES FÍSICAS DE LA MATERIA
I. CAPACIDADES:
a) Determina la densidad de sólidos irregulares (arena, gravilla y Fe) y de algunas
sustancias líquidas.
b) Calcula el porcentaje de error en la determinación de densidades de sustancias
conocidas.
c) Determina el punto de ebullición del etanol.
d) Compara la conductividad térmica de algunos metales.
II. FUNDAMENTO TEÓRICO:
Todas las sustancias tienen propiedades físicas que se observan, al margen de
cualquier cambio en la composición; por ejemplo: el color, la densidad, la dureza,
el punto de fusión, el punto de ebullición y la conductividad eléctrica la
conductividad calorífica y otras.
2.1. Densidad: relación que existe entre la masa (g) y el volumen (mL) que ocupa
una sustancia u objeto. Masa (g)
Densidad = -------------------
Volumen (mL)
Suele expresarse en g/cm3 o g/mL para sólidos y líquidos y g/L para los gases.
Tabla de densidad de sustancias comunes
Sustancia Densidad(g/cm3) Sustancia Densidad(g/cm3)
Hidrógeno(gas) 0,000089 arena 2,32
CO2(gas) 0,0019 aluminio 2,70
corcho 0,21 hierro 7,86
CH3CH2OH 0,789 cobre 8,92
agua 1 plata 10,50
magnesio 1,74 plomo 11,34
sal de mesa 2,16 oro 19,30
Porcentaje de error: El porcentaje de error para la densidad de muestras
sólidas y líquidos se calcula con la fórmula siguiente:
Densidad experimental – Densidad teórica
% error = x 100
Densidad teórica
Ing. Víctor A. Campos Linares Período 2014-20
25
Propiedades Físicas de la Materia
2.2. Punto de ebullición: Es la temperatura a la que una sustancia cambia de
estado de líquido a gas (la fase vapor y la fase líquida coexisten) y es una propiedad
característica de cada sustancia, así, el punto de ebullición del agua es de 100 ºC,
y del hierro es de 2750 ºC. a la presión de una atmósfera (760 mm Hg).
Se dice que un líquido hierve cuando su presión de vapor es igual a la presión
externa que actúa sobre la superficie del líquido. En este punto se hace posible la
formación de burbujas de vapor en la superficie del líquido.
Las moléculas del agua en la fase líquida se encuentran unidas por
fuerzas de atracción moderadamente fuertes llamadas puentes de
hidrógeno.
El calentamiento es necesario para romper estas fuerzas y permitir que
el líquido pase a la fase de vapor.
2.3. Conductividad térmica: Es la capacidad que tienen las sustancias de
permitir el paso del calor.
2.4. Punto de fusión: Es la temperatura a la que el sólido se transforma en
líquido a la presión de una atmósfera. La sustancia pasa del estado sólido
(ejemplo el hielo) al estado líquido (agua) y todo el calor se invierte en ese cambio
de estado, no variando la temperatura.
El punto de fusión se altera sensiblemente por la presencia de impurezas por lo
tanto esta constante constituye además un valioso criterio de pureza, ya que un
sólido casi puro funde en un intervalo muy pequeño de temperaturas.
Sustancia Punto de fusión (ºC)
Agua 0
Plomo 328
III. MATERIALES:
- Probetas de 100 mL y fiolas de 10 mL
- Balanza analítica y de precisión
- Mechero con alcohol
- Alcohol, CH3CH2OH y vinagre, CH3COOH
- Arena, gravilla y trozos de Fe
- Varilla de agitación
- Parafina, placas de cobre, fierro y aluminio
- Cubos de hielo
- Vasos de precipitados
- Termómetro
IV. PROCEDIMIENTO:
4.1. Densidad de sólidos
Ing. Víctor A. Campos Linares Período 2014-20
26
Propiedades Físicas de la Materia
En la presente práctica se determinará la densidad de tres sustancias de
forma irregular (arena, gravilla y Fe), cuyos volúmenes se determinan con el
Principio de Arquímedes.
Vs= Vf - Vo
Los pasos son:
a) Pesar aproximadamente 40 gramos de arena y gravilla por separado
(Peso de la muestra) y todos los trozos de Fe. Anotar cada lectura de
masa.
b) Agregar agua en tres probetas de 100mL hasta la línea de 60mL.
(Volumen inicial = Vi)
c) Sumergir las muestras en las probetas con agua y dar lectura al nuevo
volumen. (Volumen final = Vf)
d) Calcular el volumen de la muestra.
Volumen de muestra = Vf – Vi
e) Determinar la densidad de la muestra.
Peso de la muestra
Densidad de muestra (g/mL)=
Volumen de muestra
f) Cálculo del porcentaje de error. La densidad teórica se obtiene de la
tabla periódica y de la bibliografía respectiva.
4.2. Densidad de líquidos
a) Pesar las fiolas de 10 mL y anotar. (mi)
b) Llenar las fiolas de 10 mL con las muestras de etanol y vinagre.
c) Pesar la fiola más la muestra líquida respectiva. (mf l)
d) Calcular la masa de la muestra líquida.
Masa de la muestra = masa final (mf l) – masa inicial (mi)
e) Calcular la densidad de la muestra.
Peso de la muestra
Densidad de muestra (g/mL) =
Volumen de muestra
f) Calcular el porcentaje de error con la fórmula respectiva.
Ing. Víctor A. Campos Linares Período 2014-20
27
Propiedades Físicas de la Materia
4.3. Punto de ebullición
a) Armar el equipo para el experimento.
b) Colocar en un vaso de precipitados de 100 mL un
volumen suficiente de alcohol que permita mantener
sumergido el bulbo del termómetro sin topar el fondo del vaso.
c) Encender el mechero y calentar.
d) Realizar lecturas de temperatura cada 30 segundos en forma continua.
Anotar.
e) Repetir el mismo procedimiento con el agua.
4.4. Conductividad térmica
a) En el extremo de cada lámina metálica (Cu, Al y Fe), impregnar unas
gotas de parafina y luego dejar secar.
b) Con la pinza adecuada coger la lámina metálica y someterlo al calor por
el extremo contrario a donde se encuentra depositada la parafina.
c) Controlar el tiempo que tarda en derretir la parafina para cada metal.
d) Hacer las comparaciones respectivas con respecto al tiempo.
4.5. Determinación del punto de fusión
a) Colocar 10 mL de agua en una bandeja, y luego colocar dos vasos A y B.
b) En cada vaso colocar igual cantidad de cubos de hielo.
c) En el vaso B añadir un par de cucharadas de sal común.
d) Acondicionar un termómetro en cada vaso y efectuar lecturas de la
temperatura cada dos minutos.
e) Observar y registrar la temperatura en que se funde el hielo en ambos
vasos.
Ing. Víctor A. Campos Linares Período 2014-20
28
Propiedades Físicas de la Materia
INFORME DE PRÁCTICA Nº 02
Alumno: .................................................................................. Turno: ............
V. CÁLCULOS Y RESULTADOS:
a) Densidad de sólidos
Masa Volumen Volumen Volumen Densidad Densidad %
Muestra (g) inicial final de la experimental teórica Error
(mL) (mL) muestra (g/mL) (g/mL)
Arena 2,53
Gravilla 2,60
Fierro 7,86
b) Densidad de líquidos
Volumen Peso Peso fiola Peso de Densidad Densidad
fiola fiola vacía + muestra experimental teórica % Error
Muestra (mL) vacía líquido (g) (g) (g/mL) (g/mL)
(g)
Alcohol 10 mL 0,80
Vinagre 10 mL 1,05
c) Diagrama del punto de ebullición del etanol.
t (seg) 0 30 60 90
T(0C)
T (°C)
t (seg)
Ing. Víctor A. Campos Linares Período 2014-20
29
Propiedades Físicas de la Materia
d) Datos de la conductividad térmica
Muestra Tiempo (seg) Orden
Aluminio
Fierro
Cobre
e) Temperatura de fusión del hielo
min 0 2 4 6 8
VASO A
ºC
VASO B min 0 2 4 6 8
(con sal) ºC
VI. CUESTIONARIO:
1. Un frasco contiene 4,50 mL de un sólido metálico. La masa total del frasco y el
sólido es de 35,66 g. El frasco vacío pesa 14,24 g. Calcular la densidad del sólido.
2. Se requieren 95 g de una solución de etanol para una reacción química ¿Qué
volumen de esta solución debe medirse si se sabe que su densidad es 0,789
g/mL?
3. El peso experimental de 50 mL de gasolina es 41 g. Al calcular su densidad se
encontró un porcentaje de error de 4,52 %. ¿Cuál es el valor de la densidad
teórica?
4. La densidad del mercurio, Hg es 850 lb/pie3 y la del plomo, Pb es 11,3 g/cm3
¿Cuál de las sustancias tiene mayor densidad?
5. ¿Cuál es el punto de ebullición y de fusión del mercurio en grados Fahrenheit y en
grados kelvin?
Pto. ebullición Pto. fusión
Mercurio, °C °F °K °C °F °K
Hg 357 -38,4
VII. BIBLIOGRAFÍA:
Ing. Víctor A. Campos Linares Período 2014-20
30
Separaciones Físicas
PRÁCTICA N° 03
SEPARACIONES FÍSICAS
I. CAPACIDADES:
a) Diferencia los métodos de separación más comunes.
b) Propone el método de separación más adecuado para efectuar la separación de
los componentes de mezclas homogéneas o heterogéneas.
II. FUNDAMENTO TEÓRICO:
Casi toda la materia que nos rodea consiste en mezclas de sustancias. Cada
sustancia de una mezcla conserva su identidad química y por lo tanto sus
propiedades, podemos separar una mezcla en sus componentes aprovechando la
diferencia en estas sus propiedades. Así basándonos en la diferencia en las
propiedades físicas de los componentes de una mezcla, propondremos los
métodos de separación más apropiados.
Por otra parte, existen actualmente cientos de miles de sustancias químicas y es
fácil de comprender que el número de combinaciones que se pueden tener
simplemente mezclando en parejas, es ya prácticamente infinito.
Sería absolutamente imposible crear métodos para la separación de todas estas
mezclas, Sin embargo existen una serie de procedimientos más o menos generales
para hacer separaciones y entre los más comunes están:
Filtración
Operación mediante el cual se separan las partículas sólidas del seno del líquido,
haciendo pasar la mezcla a través de un medio filtrante (papel filtro, algodón,
embudo bÜchner) que sirve para retener los sólidos suspendidos.
El líquido que atraviesa el medio filtrante se llama filtrado y el sólido retenido se
llama residuo.
Sedimentación
Al dejar en reposo un líquido que contiene sólidos en suspensión, las partículas
sólidas se depositan en el fondo debido a la gravedad. Este método es muy
utilizado, cuando las muestras son grandes; como por ejemplo en la obtención del
agua potable.
Centrifugación
Operación para separar un sólido de un líquido. La separación se fundamenta en
que se aumenta la velocidad de sedimentación de las partículas sólidas en
suspensión, incrementando la aceleración de la gravedad.
Se efectúa utilizando un equipo electromecánico, llamado centrífuga cuya parte
móvil gira a una velocidad mínima de 1800 r.p.m. y su uso es para con pequeñas
muestras.
Secado
Método que permite eliminar el contenido de humedad de una muestra sólida.
Ing. Víctor A. Campos Linares Período 2014-20
31
Separaciones Físicas
Destilación
Operación que involucra vaporización y condensación de un líquido. Este método
consiste en separar los componentes de una mezcla homogénea basándose en las
diferencias en los puntos de ebullición de dichos componentes. Un compuesto de
punto de ebullición bajo se considera "volátil" en relación con los otros
componentes de puntos de ebullición mayor.
Los tipos de destilación más comunes son: la destilación simple (de baja eficiencia),
la destilación fraccionada y la destilación por arrastre con vapor.
Evaporación
Es uno de los principales métodos utilizados en la industria química para la
concentración de disoluciones acuosas. Normalmente implica la separación de agua
de una disolución mediante la ebullición de la misma en un recipiente adecuado. Si
el líquido contiene sólidos disueltos, la disolución concentrada resultante puede
convertirse en saturada, depositándose cristales.
Decantación
Permite separar dos líquidos inmiscibles (mezcla heterogénea) empleando un
embudo de decantación donde se dejan reposar los líquidos que por acción de la
gravedad y la diferencia en la densidad se puede efectuar la separación.
* La selección de un método en particular dependerá del problema específico que
se tenga teniendo en cuenta también que hay mezclas que en principio se pueden
separar por varios métodos.
III. MATERIALES Y REACTIVOS:
Materiales
Equipo de filtración Sedimentación: agua + arena
Equipo de evaporación Filtración: agua+ arena
Equipo de destilación simple Evaporación: agua + NaCl
Equipo de decantación Centrifugación: agua + arena
Estufa Destilación: agua + etanol
Vaso de precipitados 250mL Decantación: agua + aceite
Varilla de agitación.
IV. PROCEDIMIENTO:
En un vaso de precipitados de 250 mL agregar 150 mL de agua y una cantidad
adecuada de arena fina, luego agitar con la varilla de agitación. Usted determine
qué tipo de mezcla se obtiene al combinar dichos materiales.
4.1. Sedimentación
a) Verter aproximadamente la tercera parte (1/3) de la mezcla resultante en un
vaso pequeño de precipitados.
b) Dejar reposar la mezcla por 5 minutos.
Ing. Víctor A. Campos Linares Período 2014-20
32
Separaciones Físicas
c) Observar, luego separar cada componente con un gotero capilar y anotar.
4.2. Filtración
a) Armar el equipo de filtración.
b) Doblar y colocar el papel de filtro en forma
adecuada, adicionando unas gotas de agua para
fijarlo al embudo.
c) Agregar con cuidado aproximadamente la mitad de lo que queda de la mezcla
original, empleando la varilla de agitación.
d) Continuar hasta efectuar la separación de toda la mezcla.
4.3. Centrifugación
a) De lo que queda de la mezcla original, añadir a un tubo de
ensayo pequeño y llevarlo a la centrífuga.
b) Colocar otro tubo con agua con igual nivel que el de la
muestra para contrapesar y deberán ser ubicados en
posición diametralmente opuestos.
c) Conectar y encender la centrífuga, dejar funcionar por 2 minutos.
d) Apagar y retirar la muestra.
e) Observar y anotar.
4.4. Secado
a) Retirar el papel filtro más el residuo obtenido en la parte
b) Colocarlo en una luna de reloj.
c) Introducir en la estufa a 80 C.
d) Verificar la pérdida de la humedad en su totalidad.
4.5. Decantación
a) Armar el equipo de decantación.
b) Colocar en el embudo de decantación aprox. 50 mL de aceite y
100 mL de agua del caño.
c) Tapar y agitar.
d) Eliminar burbujas formadas.
e) Dejar reposar 5 minutos y efectuar la separación cuidadosamente mediante la
apertura de la llave.
Ing. Víctor A. Campos Linares Período 2014-20
33
Separaciones Físicas
4.6. Evaporación
a) Armar el equipo de evaporación.
b) En un vaso de precipitados de 100 mL, mezclar NaCl y agua hasta su
disolución.
c) Colocar la mezcla en una cápsula de porcelana.
d) Encender el mechero y calentar hasta eliminación del líquido.
e) Apagar el mechero, observar y anotar.
4.7. Destilación
a) Instalar el equipo de destilación.
b) Verificar la conexión de agua.
c) Colocar la mezcla (alcohol más agua) en el balón Engler.
d) Encender la cocina eléctrica.
e) Controlar hasta la obtención de primera gota del líquido (vapor condensado).
f) Leer la temperatura y anotar.
g) Apagar la fuente de calor y cerrar la conexión de agua.
Ing. Víctor A. Campos Linares Período 2014-20
34
Separaciones Físicas
INFORME DE PRÁCTICA Nº 03
Alumno: .................................................................................. Turno: ............
V. Dibuje los equipos de separación física, debidamente ensamblados, que se
indican a continuación. Indique el nombre de las partes componentes:
a) Equipo de filtración
b) Equipo de evaporación
c) Equipo de decantación
d) Equipo de destilación
VI. CONCLUSIONES:……………………………………………………………………………….
……………………………………………………………………………………………………..
VII. CUESTIONARIO:
Ing. Víctor A. Campos Linares Período 2014-20
35
Separaciones Físicas
1) ¿Por qué se dice que la destilación simple es una operación de baja eficiencia?
2) ¿A qué temperatura empezaron a condensar los primeros vapores de la destilación?
Reporte la respuesta en ºC, ºK y en ºF
3) Explique la propiedad en que se basa para realizar una centrifugación,
sedimentación y una filtración.
4) Se desea obtener por separado cada uno de los componentes de las siguientes
mezclas. Indique los métodos de separación más adecuados para la obtención de
cada uno de ellos.
a) Agua –alcohol –sal
b) Azúcar – kerosene – agua
5) Identificar como verdadero (V) o falso (F) cada una de las siguientes proposiciones:
a) Para destilar los puntos de ebullición de los componentes de una mezcla tienen
cercanía .................................................................................................. ( )
b) La sedimentación, filtración y centrifugación tienen un fin similar ............ ( )
c) Al separar arena y agua se utiliza la sedimentación ................................. ( )
d) La centrifugación permite separar mezclas líquido-líquido ...................... ( )
e) Se utiliza el tubo refrigerante en la destilación .......................................... ( )
f) La cápsula de porcelana forma parte del equipo de secado ........................ ( )
g) Se destila los componentes de una mezcla heterogénea ............................. ( )
h) La sedimentación, filtración y centrifugación tienen un fin similar ............ ( )
i) Al destilar se realiza primero una condensación y luego la evaporación… ... ( )
i) El trípode forma parte del equipo de evaporación ...................................... ( )
VIII. BIBLIOGRAFÍA:
……………………………………………………………………………………………………………
………………………………………………………………………………………………………….
Ing. Víctor A. Campos Linares Período 2014-20
36
Conductividad eléctrica
PRÁCTICA Nº 04
CONDUCTIVIDAD ELÉCTRICA Y SOLUBILIDAD
I. CAPACIDADES:
a) Interpreta el papel de los iones en la conducción de la corriente
eléctrica.
b) Clasifica las diversas soluciones acuosas o solutos disueltos en agua de
acuerdo a sus características electrolíticas como electrolitos fuertes,
débiles y no electrolitos.
c) Explica la solubilidad de compuestos iónicos y covalentes.
II. FUNDAMENTO TEÓRICO:
2.1. Conductividad eléctrica: es la capacidad que tienen las sustancias
para conducir la corriente eléctrica; para que suceda esto, una
solución debe contener IONES (positivos y negativos).
2.2. Enlace químico: es la fuerza de carácter eléctrico que une a los
átomos para formar moléculas. Los átomos al enlazarse ganan,
pierden o comparten electrones en su capa de valencia, para llegar a
tener la configuración electrónica de un gas noble.
Fuerzas Interatómicas
- Enlace iónico: donde los metales transfieren electrones a los no
metales (mayor electronegatividad). Los compuestos iónicos fundidos
o en solución acuosa conducen la corriente eléctrica y la mayoría son
solubles en agua. Son sólidos cristalinos a temperatura ambiente y
tienen alta temperatura de fusión; ejemplo: NaCl, KNO3, Al (OH)3,
LiOH.
- Enlace covalente: donde los no metales comparten sus electrones.
Los compuestos covalentes disueltos en agua encontramos que los
hay buenos, débiles y en su mayoría no conducen la corriente
eléctrica. Además algunos son miscibles, parcialmente miscibles e
inmiscibles en agua; ejemplo: HCl, HNO 3, H2SO4, CH3COOH, fenol,
kerosene, petróleo, aceite, etc.
- Enlace metálico: la unión se debe a los electrones de valencia que
están deslocalizados a lo largo de todo el sólido. La movilidad de los
electrones explica por qué los metales son buenos conductores del
calor y de la electricidad; ejemplo: Ag, Cu, Fe, Al, etc.
Fuerzas Intermoleculares
- Interacción dipolo - dipolo: se presenta cuando el extremo positivo de una
molécula está cerca al extremo negativo de otra, caso especial es el puente
de hidrógeno (EPH).
- Interacción ión - dipolo: se presenta entre un ión y la carga parcial de un
extremo de una molécula polar.
Ing. Víctor A. Campos Linares Período 2014-20
37
Conductividad eléctrica
- Fuerzas de London: se deben a la atracción del núcleo con carga positiva
de un átomo, hacia la nube electrónica de otro átomo de alguna molécula
cercana; ésta induce dipolos temporales en los átomos y moléculas.
2.3. Electrolitos: solutos que en agua se disocian (se separan en sus
iones) o ionizan (formación de iones) y que permiten el paso de la
corriente eléctrica.
- Electrolitos fuertes: permiten el paso de la corriente eléctrica con
alta intensidad.
Algunos compuestos iónicos se disocian totalmente; así:
NaOH(s) + H2O Na+(ac) + OH-(ac)
Algunos compuestos covalentes se ionizan totalmente; así:
HNO3 + H2O H3O+ + NO3-
- Electrolitos débiles: permiten el paso de la corriente eléctrica con
baja intensidad.
Algunos compuestos covalentes se ionizan parcialmente; así:
HNO2 + H2O H3O+ + NO2-
2.4. No electrolitos: solutos que en agua o puros no conducen la
corriente eléctrica; por ejemplo: agua destilada, etanol, kerosene,
azúcar, NaCl(s), CH3OH(ac).
Tabla de ácidos fuertes y débiles
Ácidos Ácidos Bases Bases
fuertes débiles fuertes Débiles
H2SO4 CH3COOH NaOH NH3
HNO3 HNO2 LiOH CH3NH2
HClO4 HClO KOH
HI HCN Ca(OH)2
HBr HF Ba(OH)2
HCl
2.5. Solubilidad: es la capacidad de una sustancia de disolverse en otra.
Este hecho se explica por la naturaleza química de ambas sustancias.
Existen disoluciones de un sólido en un líquido, de un gas en líquido y
de dos líquidos; ejemplo: el azúcar en agua, el dióxido de carbono en
agua y el etanol en agua.
Ing. Víctor A. Campos Linares Período 2014-20
38
Conductividad eléctrica
2.6. Miscibilidad: es la capacidad de un líquido para mezclarse con otro y
así formar una sola fase. Podemos decir que lo semejante disuelve a lo
semejante.
Reglas de solubilidad para compuestos iónicos comunes.
Compuestos iónicos
Excepciones importantes
solubles en agua
Compuestos que contienen
NO3- Ninguna
(CH3COO)- Ninguna
Cl- Compuestos de Ag+, Hg22+ y Pb2+
Br- Compuestos de Ag+, Hg22+ y Pb2+
I- Compuestos de Ag+, Hg22+ y Pb2+
(SO4)2- Compuestos de Sr2+, Hg22+, Ba2+ y Pb2+
Compuestos iónicos
Excepciones importantes
insolubles en agua
Compuestos de NH4+, los
S2- cationes de metales alcalinos,
también Ca2+, Sr2+ y Ba2+
(CO3)2- Compuestos de NH4+ y los
cationes de metales alcalinos.
(PO4)3- Compuestos de NH4+ y los
cationes de metales alcalinos
OH- Compuestos de los cationes de
metales alcalinos, Ca2+, Sr2+ y Ba2+
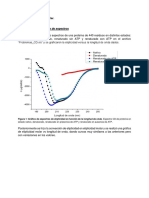
Gráficas de solubilidad con respecto a la temperatura de
diferentes sustancias en agua.
Ing. Víctor A. Campos Linares Período 2014-20
39
Conductividad eléctrica
III. MATERIALES Y EQUIPOS:
Equipo de conductividad NaCl (s) y NaCl (ac ) Agua destilada
Vasos de precipitados CH3COOH (ac) Agua potable
Franela NaOH (ac) Sacarosa
Tubos de ensayo HCl (ac) Etanol
Petróleo, azufre, naftaleno, aceite.
PROCEDIMIENTO:
CONDUCTIVIDAD
4.1. Anotar en orden las disoluciones propuestas para la práctica.
4.2. Comprobar el buen funcionamiento del equipo de
conductividad, uniendo los electrodos se encenderá el foco.
4.3. Sumergir los electrodos en forma paralela en cada muestra. Si el
foco da luz, anotar si la intensidad es alta o baja en el respectivo
recuadro; si no enciende la luz indicar la intensidad como nula.
4.4. Cada vez que cambie de muestra, limpie los electrodos con la
franela.
4.5. Finalizada la parte experimental, desconectar el equipo de
conductividad eléctrica y en su mesa procesar toda la
información.
SOLUBILIDAD
4.1. En nueve tubos de ensayo preparar las siguientes mezclas:
Cloruro de sodio – agua
Cloruro de sodio – petróleo
Azufre – ácido acético
Azufre – petróleo
Naftaleno – petróleo
Petróleo – agua
Petróleo – aceite
Etanol – agua
Etanol – aceite
Ing. Víctor A. Campos Linares Período 2014-20
40
Conductividad eléctrica
INFORME DE PRÁCTICA Nº 04
Apellidos y Nombres: ………………………………………………….Turno: ………………
V. CÁLCULOS Y RESULTADOS:
5.1. CONDUCTIVIDAD
Intensidad del foco Compuesto Electrolito No
Muestras
Alta Baja Nula Iónico Covalente Fuerte Débil electrolito
NaCl(s)
K2Cr2O7 (ac)
KClO3 (ac)
HCl (ac)
H2O destilada
NaOH (ac)
C2H5OH(ac)
CH3COOH (ac)
NaCl (ac)
CuSO4 ac)
H2O potable
Sacarosa
5.2. SOLUBILIDAD Y MISCIBILIDAD
Sustancia 1 Sustancia 2 Solubilidad Miscibilidad
Mezclas
EI ECP ECNP EI ECP ECNP Sol. Ins. Misc. Inm.
Cloruro de sodio – agua
Cloruro de sodio– petróleo
Azufre – ácido acético
Azufre – petróleo
Naftaleno – petróleo
Petróleo – agua
Petróleo – aceite
Etanol – agua
Etanol - aceite
Ing. Víctor A. Campos Linares Período 2014-20
41
Conductividad eléctrica
VI. CONCLUSIONES:………………………………………………………………………………
………………………………………………………………………………………………………..
………………………………………………………………………………………………………..
VI. CUESTIONARIO:
1) Explique la diferencia entre disociación e ionización. Proponer dos ejemplos:
2) Explicar el fenómeno por el cual el agua potable, permite el paso de la corriente
eléctrica; pero no por el agua químicamente pura como es el agua destilada.
3) Enumere cinco ejemplos de electrolitos fuertes, débiles y no electrolitos. También
enumere cinco ejemplos de compuestos con enlace iónico y enlace covalente.
4) La ecuación de disociación del KCl (s) (compuesto iónico) es:
5) La ecuación de ionización del HBr (ácido fuerte) es:
6) La ecuación de ionización parcial del NH3(base débil) es:
7) La ecuación de ionización parcial del HNO2(ácido débil) es:
VIII. BIBLIOGRAFÍA:
………………………………………………………………………………………………………
………………………………………………………………………………………………………
……………………………………………………………………………………………………….
Ing. Víctor A. Campos Linares Período 2014-20
42
Conductividad eléctrica
Ing. Víctor A. Campos Linares Período 2014-20
43
Reacciones químicas
PRÁCTICA N° 05
REACCIONES QUÍMICAS
I. CAPACIDADES:
a) Verifica una reacción química al observar cambio de color, formación de un
precipitado, formación de gas o liberación de calor.
b) Diferencia las reacciones de combinación o síntesis, de descomposición, de
desplazamiento simple y de doble desplazamiento.
c) Formula y balancea por tanteos las reacciones químicas experimentales.
II. FUNDAMENTO TEÓRICO:
Una reacción química es un cambio químico, donde dos o más sustancias
interaccionan para formar nuevas sustancias.
Una reacción química se representa por una ecuación química, la
cual se escribe colocando en la izquierda, los compuestos o elementos
que van a interaccionar llamados reactantes, luego una flecha que
indica el sentido de la reacción y a la derecha, las sustancias
producidas llamadas productos.
aA + bB cC + dD
Reactantes Productos
Las reacciones químicas se clasifican en:
A. Reacciones de combinación o síntesis
Dos o más reactantes forman un solo producto
A+B C
Ejemplo
4 Fe + 3O2 2Fe2O3
Na2O + H2O 2NaOH
B. Reacciones de descomposición
Sólo un reactante por acción de un factor energético como puede ser la luz, calor (Δ)
o corriente eléctrica, se descompone formando dos o más productos.
AB A+B
Ejemplo:
CaCO3 CaO + CO2
2KClO3 2KCl + 3O2
Ing. Víctor A. Campos Linares Período 2014-20
44
Reacciones Químicas
C. Reacciones de desplazamiento simple
Se caracteriza por tener a un elemento y un compuesto como reactante y productos.
El elemento reactante desplaza a un elemento del compuesto, que forma parte de los
productos en forma libre.
A + BC AC + B
Orden de actividad de los metales de menor a mayor
Au, Pt, Ag, Hg, Cu, H, Pb, Sn, Ni, Co, Cd, Fe, Cr, Zn, Al, Mg, Na, Ca, Ba, K, Li
Desplazan al hidrógeno de los ácidos
Desplazan al hidrógeno del vapor de agua
Desplazan al hidrógeno
del agua fría
Ejemplo:
Zn + H2SO4 ZnSO4 + H2
Fe + CuSO4 FeSO4 + Cu
D. Reacciones de desplazamiento doble o de metátesis
Los reactantes se reacomodan y forman nuevas parejas. Es importante resaltar que
ningún elemento varía en su estado de oxidación.
AB + CD AD + CB
Si en los productos se forma un sólido que precipita, la reacción se
denomina de precipitación. El producto que precipita se indica con
una flecha hacia abajo y corresponde al metal más pesado; ejemplo:
Hg2(NO3)2 + K2CrO4 Hg2CrO4 + KNO3
Si los reactantes son un ácido y una base para producir una sal y agua, la reacción
se le conoce como reacción de neutralización; ejemplo:
H2SO4 + Ca(OH)2 CaSO4 + H2O
II. MATERIALES Y REACTIVOS:
Materiales
Tubos de ensayo
Mechero
Luna de reloj
Pinzas para tubo de ensayo
Clavos oxidados
Ing. Víctor A. Campos Linares Período 2014-20
45
Reacciones Químicas
Reactivos
Cinta de magnesio Gránulos de Zn Sulfato cúprico (ac)
Sulfato cúprico pentahidratado Nitrato de Plomo (II) Yoduro de potasio
Hidróxido de calcio Ácido sulfúrico Bicarbonato de sodio
Ácido clorhídrico Tiocianato de amonio
III. PROCEDIMIENTO:
a. Coger un trozo de cinta de magnesio con una pinza y acercar a la llama azul
del mechero, el magnesio reacciona con el oxígeno del aire para formar el
producto con la aparición de una luz blanca muy intensa, a la cual no se le
debe mirar directamente. La persona que quema la cinta de magnesio debe
sostener un tubo de ensayo para recibir el producto blanco formado (cenizas).
b. Coger el tubo de ensayo que contiene las cenizas de la reacción anterior y
adicionarle agua destilada en cantidad suficiente para cubrir las cenizas.
Agitar vigorosamente hasta disolver y adicionar 2 ó 3 gotas de fenolftaleína.
Observar y anotar. Luego agregar HClcc para neutralizar, hasta que se observe
un cambio de color.
c. En un tubo de ensayo colocar un trozo de zinc y añadir sulfato cúprico, CuSO4
hasta cubrir totalmente el trozo de zinc. Sin agitar, dejar en reposo por lo
menos 5 minutos, luego observar y anotar.
d. Colocar en un tubo de ensayo una pequeña cantidad de cristales de sulfato de
magnesio heptahidratado, MgSO4.7H2O acercarlo a la llama del mechero,
calentar y agitar hasta observar cambio. Observar y anotar.
e. Colocar en un tubo de ensayo 1 mL de nitrato de plomo (II), Pb(NO3)2 y
adicionar gota a gota yoduro de potasio, KI hasta observar cambio. Agitar,
observar y anotar.
f. Colocar en un tubo de ensayo 1 mL de hidróxido de calcio, Ca(OH)2 y agregar
2 ó 3 gotas de fenolftaleína. Adicionar gota a gota ácido sulfúrico concentrado,
HClcc hasta observar cambio de color.
g. En un tubo de ensayo, colocar 1 mL de bicarbonato de sodio, NaHCO3 y luego
ácido clorhídrico concentrado, HClcc gota a gota hasta observar cambio.
Observar y anotar.
h. En una luna de reloj, colocar un clavo oxidado y agregar 4 gotas de ácido
clorhídrico concentrado. Observar y anotar.
i. De la reacción anterior, retirar el clavo con la pinza y añadir 3 ó 4 gotas de
tiocianato de amonio, NH4.SCN a la solución. Observar y anotar.
j. En un tubo de ensayo agregue aproximadamente 20 mL de agua, luego añada
un trozo pequeño de sodio, Na evite agitar, observe que hay desprendimiento
de un gas, el producto obtenido será un ácido o una base, usted verifique con
el indicador respectivo, para luego proceder a su neutralización respectiva.
Ing. Víctor A. Campos Linares Período 2014-20
46
Reacciones Químicas
Ing. Víctor A. Campos Linares Período 2014-20
47
Reacciones Químicas
INFORME DE PRÁCTICA N° 05
Alumno: .................................................................................. Turno: ............
V. RESULTADOS:
a) Ecuación Química…………………………………………………………………………….
Tipo de Reacción Química………………………………..………………………………..
Nombre de los productos …………………………………………………………………..
Observaciones………………………………………………………………………………….
……………………………………………………………………………………………………..
b) Ecuación Química……………………………………………………………………………..
Tipo de Reacción Química………...………………………………………………………..
Nombre de los productos …………...………………………………………………………
Observaciones…………………………...…………………………………………………….
……………………………………….......................................................................
c) Ecuación Química……………………………………………………………………………...
Tipo de Reacción Química………………………………....………………………………..
Nombre de los productos ………………………………....…………………………………
Observaciones………………………………………………...………………………………..
…………………………………………………………….......………………………………..
d) Ecuación Química…………………………………………………………………..………...
Tipo de Reacción Química…………………...……………………………………………..
Nombre de los productos ……………....……………………………………………………
Observaciones……………………………......………………………………………………..
…………………………………………………………………………………………………..
e) Ecuación Química……………………………………………………………………………..
Tipo de Reacción Química………………………...………………………………………..
Nombre de los productos ………………....…………………………………………………
Observaciones………………………….......…………………………………………………..
………………………………………………………………………………………………......
f) Ecuación Química………………………………………………………………..…………….
Tipo de Reacción Química………………...………………………………………………..
Nombre de los productos ………………...…………………………………………………
Observaciones……………………………...…………………………………………………..
…………………………………………………………………………………………………..
g) Ecuación Química………………………………………………………………………..…….
Tipo de Reacción Química…………………………...……………………………………..
Nombre de los productos …………………………...………………………………………
Observaciones…………………………………………...……………………………………..
…………………………………………………………………………………………………..
Ing. Víctor A. Campos Linares Período 2014-20
48
Reacciones Químicas
h) Ecuación Química………………………………………………………….………………….
Tipo de Reacción Química………………...………………………………………………..
Nombre de los productos …………………...……………………………………………….
Observaciones……………………………….......……………………………………………..
………….......……………………………………………………………………………………….
i)Ecuación Química……………………………………………………………………………..
Tipo de Reacción Química……………………..………...……………….……………….....
Nombre de los productos ……………...………..…………………………………………….
Observaciones…………………………...………..………………………………………………
…..…………………………………………………………………………………………………..
j)Ecuación Química………………………..…………………………………………………….
Tipo de Reacción Química……………………..………...……………….……………….....
Nombre de los productos ……………...………..…………………………………………….
Observaciones…………………………...………..………………………………………………
…..…………………………………………………………………………………………………..
VI. CONCLUSIONES:
………………………………………………………………………………………………………………
………………………………………………………………………………………………………………
……………………………………………………………………………………………………………..
VII. CUESTIONARIO:
a) Proponer tres ecuaciones químicas balanceadas para cada tipo de reacción
química. Deben ser diferentes a las realizadas en la práctica.
Ing. Víctor A. Campos Linares Período 2014-20
49
Reacciones Químicas
b) Completar y balancear por tanteos las siguientes ecuaciones químicas. Identificar
el tipo de reacción.
Al2O3 + H2O
Ca + O2
Fe(OH)3 + HNO3
Mg + H2SO4
Pb(NO3)2 + NaI
Zn + HCl
C4H10O + O2 CO2 + H2O
Fe(OH)3 + H2SO4 Fe2(SO4)3 + H2O
MgO + H2O Mg(OH)2
Li + N2 Li3N
Na2SO4 + BaCl2 BaSO4 + NaCl
AgNO3 + Na2SO4 Ag2SO4 + NaNO3
c) Indicar las siguientes proposiciones como verdadero (V) o falso (F):
- Cuando el Na reacciona con el H2O desprende gas molecular O2 ........................ ( )
- En una reacción exotérmica se produce liberación de calor ....................... ( )
- La fenolftaleína nos permite identificar la presencia de una base .............. ( )
- En una ecuación química los reactantes se encuentran a la izquierda de la
flecha ..................................................................................................... ( )
- El sodio es un metal que puede conservarse sumergido en agua ............... ( )
- Cuando el Na reacciona con el H2O desprende gas molecular N2 ........................ ( )
- En una reacción exotérmica se produce absorción de calor ....................... ( )
- En una reacción de doble desplazamiento no se producen cambios en los
estados de oxidación en ningún elemento reaccionante ....................... ( )
VII. BIBLIOGRAFÍA:
Ing. Víctor A. Campos Linares Período 2014-20
50
Reacciones Químicas
Ing. Víctor A. Campos Linares Período 2014-20
51
Reacciones Redox
PRÁCTICA N° 06
REACCIONES REDOX
I. CAPACIDADES:
a) Describe las características de una reacción de óxido – reducción.
b) Identifica el agente oxidante y reductor en las reacciones redox.
c) Balancea las ecuaciones de las reacciones de óxido - reducción por el método
del ión electrón.
II. FUNDAMENTO TEÓRICO:
Las reacciones en las cuales los elementos experimentan cambios del número de
oxidación se llaman reacciones de óxido – reducción o reacciones redox.
Estas reacciones se producen en todas las áreas de la química y la bioquímica.
La oxidación es el aumento algebraico del número de oxidación y corresponde a
la pérdida electrones. La reducción es una disminución algebraica del número de
oxidación y corresponde a una ganancia de electrones. La oxidación y la reducción
son procesos que suceden simultáneamente.
Ejemplo:
+2 +6 -2 +1 +7 -2 +1 +6 -2 +3 +6 -2 +2 +6 -2 +1 +6 -2 +1 -2
FeSO4 + KMnO4 + H2SO4 Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
Analizando los elementos que cambian en su estado de oxidación son:
Fe: +2 +3 aumenta estado de oxidación, entonces se oxida
Mn: +7 +2 disminuye estado de oxidación, entonces se reduce
Otros ejemplos:
Los agentes oxidantes se reducen y oxidan a otras sustancias y los agentes
reductores se oxidan y reducen a otras sustancias.
Las reacciones de óxido – reducción necesitan al igual que cualquier otro tipo de
reacciones ser balanceadas. El método a usar para el balance es el método del ión
electrón.
Balance por el método del ión electrón:
a) Identificar los elementos que cambian en sus estados de oxidación.
b) Dividir la ecuación en dos semirreacciones, una de oxidación y en otra de
reducción.
c) Balancear la materia y la parte eléctrica, así:
Balancear los elementos que son diferentes al hidrógeno (H) y al oxígeno (O).
Luego balancear los átomos de O añadiendo H2O.
Enseguida balancear los átomos de H, agregando H+.
Ing. Víctor A. Campos Linares Período 2014-20
52
Reacciones Redox
d) Por último, equilibrar las cargas sumando electrones (e-) al lado más positivo,
con el propósito de igualar la carga iónica neta. Multiplicar cada semirreacción
por el número de electrones transferidos.
e) Sumar las dos semirreacciones y simplificar solo los términos comunes que
aparecen en ambos lados de la ecuación.
f) Toda la información obtenida trasladar a la ecuación principal. Comprobar por
simple inspección el balance final y si fuera necesario reajustar algún
coeficiente por tanteo.
Ejemplo de aplicación del M.I.E. en medio ácido
+1 +4 -2 +1 +6 -2 +1 +6 -2 +1 +6 -2 +3 +6 -2 +1 +6 -2 +1 -2
Na2SO3 + K2Cr2O7 + H2SO4 Na2(SO4) + Cr2(SO4)3 + K2SO4 + H2O
H2O + SO3 2- [O] SO42- + 2H+ + 2e- x6 3
6e- + 14 H+ + Cr2O7 2- [R] 2Cr 3+ + 7H2O x2 1
3 H2O + 3 SO3 2- 3 SO42- + 6H+ + 6e-
6e- + 14 H+ + Cr2O7 2- 2Cr 3+ + 7H2O
3H2O+ 3SO3 2- + 6e- +14H+ + Cr2O7 2- 3SO42- + 6H+ + 6e- + Cr3+ + 7H2O
3SO3 2- + 8H+ + Cr2O7 2- 3SO42- + 2Cr3+ + 4H2O
Esta última información se traslada a la ecuación principal; así:
3Na2SO3 + K2Cr2O7 + 4H2SO4 3Na2(SO4) + Cr2(SO4)3 + K2SO4 + 4H2O
III. MATERIALES Y REACTIVOS:
- Materiales - Reactivos
Tubos de ensayo NaNO2 (ac) HCl cc KMnO4(ac)
K2Cr2O7(ac) FeSO4(ac)
NH4SCN(ac)
IV. PROCEDIMIENTO:
4.1. En un tubo de ensayo colocar aproximadamente 0,5 mL de nitrito de sodio,
NaNO2; luego 5 gotas de HClcc y gota a gota del agente oxidante permanganato
de potasio, KMnO4. Visualizar que el contenido del tubo de ensayo se torna
ligeramente lila.
4.2. En un tubo de ensayo colocar 1 mL de peróxido de hidrógeno, H2O2; luego 5
gotas de HClcc y gota a gota del agente oxidante dicromato de potasio, K2Cr2O7.
Agitar y si fuera necesario calentar con el mechero. Visualizar un color verde
azulado.
4.3. En un tubo de ensayo colocar 1 mL de peróxido de hidrógeno, H2O2; luego 5
gotas de HClcc. Y gota a gota del agente oxidante, KMnO4. Visualizar la
presencia de oxígeno que se libera como producto.
4.4. En un tubo de ensayo colocar 1 mL de sulfato ferroso, FeSO 4; luego 5 gotas de
HNO3cc. Para identificar al Fe3+ ya presente, adicione 3 gotas de tiocianato de
amonio, NH4(SCN); si cambia a color rojo sangre indicará la presencia de Fe3+.
Ing. Víctor A. Campos Linares Período 2014-20
53
Reacciones Redox
INFORME DE PRÁCTICA N° 06
Alumno: .................................................................................. Turno: ............
V. RESULTADOS:
NaNO2 + HCl + KMnO4 NaNO3 + MnCl2 + KCl + H2O
5.1
H2O2 + HCl + K2Cr2O7 CrCl3 + KCl + O2 + H2O
5.2
H2O2 + HCl + KMnO4 02 + MnCl2 + KCl + H2O
5.3
FeSO4 + HNO3 NO + Fe2(SO4)3 + Fe(NO3)3 + H2O
5.4
VI. CONCLUSIONES:……………………………………………………………………………………
…………………………………………………………………………………………………………
……………….……………………………………………………………………………………….
Ing. Víctor A. Campos Linares Período 2014-20
54
Reacciones Redox
VII. CUESTIONARIO:
7.1. Balancear las siguientes semirreacciones y especificar si corresponden a un
proceso de oxidación o reducción.
I- I2
H2SO3 (SO4)2 -
NO3- N2
PbO2 Pb2+
7.2. Balancear las siguientes ecuaciones químicas por el método del ión – electrón.
Identificar el agente oxidante y reductor, la semirreacción de oxidación y
reducción.
Ca (ClO)2 + KI + HCl I2 + CaCl2 + KCl + H2O
I- I2
ClO- Cl-
FeSO4 + KMnO4 + H2SO4 Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
Fe2+ Fe3+
MnO4- Mn2+
KMnO4 + KI + H2O MnO2 + KIO3 + KOH
MnO4- MnO2
I- IO3-
VIII. BIBLIOGRAFÍA:
Ing. Víctor A. Campos Linares Período 2014-20
55
Rendimiento Porcentual
PRÁCTICA N° 07
RENDIMIENTO PORCENTUAL DE UNA REACCIÓN QUÍMICA
I. CAPACIDADES:
a) Determina el rendimiento teórico y real de una reacción química.
b) Evalúa y justifica el rendimiento experimental obtenido.
II. FUNDAMENTO TEÓRICO:
La interpretación cuantitativa de las reacciones químicas es la parte de la química
denominada estequiometría. En varios procesos químicos, las cantidades de los
reactivos que se usan son tales que la cantidad de producto que se forma depende
del reactivo que no está en exceso, denominado reactivo limitante.
Para solucionar problemas donde no se conoce el reactivo limitante, un enfoque
alternativo es el de calcular el rendimiento teórico de uno de los productos para cada
reactivo por separado. El reactivo que produciría la menor cantidad de producto es el
reactivo limitante.
Ejemplo:
Si 20 g de CaO reaccionan con 10 g de H2O el peso teórico de producto obtenido es:
CaO + H2O Ca(OH)2
74 g de Ca (OH)2
20 g CaO x -------------------------- = 26,4 g Ca(OH)2
56 g de CaO
Reactivo limitante Rendimiento teórico
74 g de Ca (OH)2
10 g H2O x ------------------------- = 41,1 g Ca (OH)2
18 g de H2O
Reactivo en exceso
El peso de producto obtenido es de 26,4 g de Ca (OH)2 por ser el menor valor y
que corresponde al rendimiento teórico.
El rendimiento teórico de una reacción es el rendimiento calculado considerando
que la reacción se produce en forma completa, es decir, se consume todo el
reactivo limitante. La cantidad de producto que realmente se obtiene en una
reacción se denomina rendimiento real o experimental que siempre es menor
que el rendimiento teórico.
El rendimiento porcentual se calcula de la siguiente manera.
Ing. Víctor A. Campos Linares Período 2014-20
56
Rendimiento Porcentual
III. MATERIALES Y REACTIVOS:
MATERIALES
Espátula
Vaso de precipitación
Varilla de agitación
Papel de filtro
Embudo simple
Matraz Erlenmeyer
Balanza analítica o de precisión
Luna de reloj
Estufa
REACTIVOS
Nitrato de plata, AgNO3
Cloruro de sodio, NaCl
Agua destilada
IV. PROCEDIMIENTO:
1. Pesar en una luna de reloj aproximadamente 0,4 gramos de NaCl.
2. En otra luna de reloj pesar aproximadamente 0,2 gramos de AgNO3.
3. Colocar ambos reactivos en un vaso de precipitados de 50 mL, luego añadir
30 mL de agua destilada y agitar por 3 minutos.
4. Ensamblar el equipo de filtración.
5. Pesar el papel de filtro antes de colocarlo en el equipo de filtración.
6. Filtrar cuidadosamente la mezcla evitando que se queden restos en el vaso de
precipitación para esto agregar agua destilada hasta que no queden sólidos.
Luego, agregar agua destilada unas tres veces sobre el papel de filtro.
7. Retirar cuidadosamente el papel de filtro, colocarlo en una luna de reloj y
secar en la estufa.
8. Posteriormente al secado, pesar nuevamente el papel de filtro con los sólidos
incluidos y por diferencia de los pesos con el paso 5 obtener el rendimiento
real de la reacción.
9. Calcular el rendimiento teórico, experimental y el porcentaje de rendimiento.
Ing. Víctor A. Campos Linares Período 2014-20
57
Rendimiento Porcentual
INFORME DE PRÁCTICA N° 07
Alumno: .................................................................................. Turno: ............
V. CÁLCULOS:
5.1. Ecuación química balanceada
5.2. Cálculo del rendimiento teórico
5.3. Cálculo del rendimiento real
5.4. Cálculo del porcentaje de rendimiento.
VI. RESULTADOS:
Gramos de Gramos Peso (g) Peso (g) Peso(g) Rendimiento Rendimiento %
AgNO3 de NaCl papel filtro papel filtro + AgCl AgCl experimental teórico Rendimiento
g de AgCl g de AgCl
VII. CONCLUSIONES:
VIII. CUESTIONARIO:
a) ¿Considera que el rendimiento porcentual obtenido es óptimo? Explicar.
b) ¿Qué consideraciones tendría en cuenta para mejorar el rendimiento real obtenido?
c) Calcular el peso de reactivo en exceso que al final de la reacción queda sin reaccionar.
(referido al experimento)
Ing. Víctor A. Campos Linares Período 2014-20
58
Rendimiento Porcentual
d) Identifique el reactivo limitante en la reacción:
6Na + Al2O3 2Al + 3Na2O
Cuando 5,52 gramos de sodio se calientan con 5,10 gramos de Al2O3.
- ¿Qué masa de aluminio puede producirse?
- ¿Qué masa de reactivo en exceso permanece al final de la reacción?
e) En la reacción: NO2 + O2 + H2O HNO3
¿Cuántos gramos de cada sustancia reaccionante se necesitan para producir 2000
g de HNO3?
f) En la reacción: Na2CO3 + Ba(NO3)2 BaCO3 + 2 NaNO3
Si se hacen reaccionar 750 gramos de cada uno de los reactantes, finalizada la
reacción...
-¿Cuántos gramos de BaCO3 se obtendrán al final de la reacción?
-¿Cuántos moles de NaNO3 se obtendrán al final de la reacción?
- Si experimentalmente se obtuvieron 2,1 moles de BaCO 3. Determine el % de rendimiento.
g) Marque las siguientes proposiciones como verdadera (V) o falsa (F):
-La estequiometría implica el estudio cuantitativo de una reacción química ( )
-El rendimiento real siempre es mayor al rendimiento teórico ( )
-El reactivo limitante se consume totalmente en una reacción química ( )
-La eficiencia de una reacción química se mide con el porcentaje de rendimiento ( )
-Porcentaje de rendimiento = (Rend. Teórico / Rend. Real) x 100 ( )
IX.BIBLIOGRAFÍA:……………………………………………………………………………………
…………………………………………………………………………………………………………
Ing. Víctor A. Campos Linares Período 2014-20
59
Rendimiento Porcentual
Ing. Víctor A. Campos Linares Período 2014-20
60
Preparación de Soluciones
PRÁCTICA N° 08
PREPARACIÓN DE SOLUCIONES
I. CAPACIDADES:
a) Calcula la cantidad de soluto necesario para una solución.
b) Prepara una solución acuosa a una concentración determinada.
c) Realiza cálculos para preparar una solución por disolución.
II. FUNDAMENTO TEÓRICO:
Una solución es una mezcla homogénea de dos a más sustancias.
Frecuentemente, en las soluciones se identifica al soluto, que está disuelto en otra
sustancia llamado disolvente.
Las soluciones que se utilizan en el laboratorio son líquidas y el disolvente más
empleado es el agua. Por ejemplo las soluciones de hidróxido de sodio se preparan
disolviendo NaOH sólido en agua.
La concentración de las soluciones expresa la cantidad de soluto disuelto en una
masa específica o volumen de solución.
Unidades de Concentración
Porcentaje peso/peso:
Peso de soluto (g)
% en peso (w/w) = ------------------------------ x 100
Peso de solución (g)
Peso de solución = Peso de disolvente + Peso de soluto
Ejemplo:
Solución de NaCl al 5%(w/w), significa que 5 gramos de NaCl están contenidos
en 100 gramos de solución; expresado como factor sería 5 g NaCl / 100 g de
solución.
Porcentaje peso/volumen:
Peso de soluto (g)
% en peso (w/v) = ---------------------------------- x 100
Volumen de solución (mL)
Ejemplo:
Solución de KCl al 8%(w/v), significa que 8 gramos de KCl están contenidos en
100 mL de solución; expresado como factor sería 8 g de KCl / 100 mL de
solución.
Ing. Víctor A. Campos Linares Período 2014-20
61
Preparación de Soluciones
Partes por millón (ppm)
Miligramos de soluto en un litro de solución.
Peso de soluto (mg)
ppm = ------------------------------------
Volumen de solución (L)
Ejemplo:
Solución de AgNO3 800 ppm, significa que 800 mg de AgNO3 están contenidos
en 1L de solución; como factor sería 800 mg de AgNO 3 / 1 L de solución.
Ing. Víctor A. Campos Linares Período 2014-20
62
Preparación de Soluciones
Molaridad (M)
Moles de soluto en un litro de solución
moles de soluto (moles)
M = ---------------------------------------
Litro de solución (L)
Ejemplo:
Solución de NaOH 0,9 M, significa que 0,9 moles de NaOH están contenidos en
un litro de solución, como factor 0,9 moles de NaOH / L de solución.
Normalidad (N)
Equivalentes de soluto en un litro de solución
Equivalentes de soluto (equivalentes)
N = ---------------------------------------------------------
Litro de solución (L)
Ejemplo:
Solución de NaOH 0,8 N, significa que 0,8 equiv. de NaOH están contenidos
en un litro de solución, como factor 0,8 equiv. de NaOH / L de solución.
Factor “i”; es el # equivalentes de soluto/mol de soluto y cuyo valor se
determina; así:
Para los ácidos depende del número de H+ que pueda perder.
Para las bases depende del número de grupos OH- y
Para las sales depende de la carga total positiva o negativa.
Para los agentes oxidantes o reductores depende de los e- ganados o perdidos.
Ejemplo:
SOLUTO FACTOR “i” SOLUTO FACTOR “i”
H2SO4 2 FeCl3 3
HNO3 1 K2SO4 2
HBr 1 KMnO4 1
HCl 1 KNO3 1
CH3COOH 1 Fe2(SO4)3 6
NaOH 1 Na2SO4 2
Ca(OH)2 2 CuSO4.5H2O 2
Ing. Víctor A. Campos Linares Período 2014-20
63
Preparación de Soluciones
Ecuación de dilución
Preparación de una solución adicionando un volumen determinado de agua a otro
volumen de solución de mayor concentración.
La fórmula de dilución es la siguiente:
(C x V) sol. concentrada = (C x V) sol. diluida
Donde: C es la concentración de la solución diluida y concentrada, debe estar en
las mismas unidades.
III. MATERIALES Y REACTIVOS:
Materiales Pipeta de 10 mL
Balanza analítica Bombilla de succión
Embudo simple Reactivos
Fiolas de 50 mL y 100 mL NaCl
Vaso de Precipitación Sacarosa
Luna de reloj HCl 6N
IV. PROCEDIMIENTO:
4.1. Preparar 50 mL de una solución de NaCl al 2% (w/v)
a) Calcular la cantidad necesaria de NaCl y pesar en la balanza analítica
b) Agregar el NaCl en la fiola de 50 mL y añadir suficiente cantidad de agua
destilada para disolver el sólido.
c) Luego agregar agua destilada hasta la línea de aforo. Agite para homogenizar.
4.2. Preparar 50 mL de una solución de NaCl 0,08 N
a) Calcular la cantidad necesaria de NaCl y pesar en la balanza analítica
b) Agregar el NaCl en la fiola de 50 mL y añadir suficiente cantidad de agua
destilada para disolver el sólido.
c) Luego agregar agua destilada hasta la línea de aforo. Agite para homogenizar.
4.3. Preparar 50 mL de una solución de C12H22O11 0,1M
a) Calcular la cantidad necesaria de sacarosa y pesar en la balanza analítica
b) Agregar el C12H22O11 en la fiola de 50 mL y añadir suficiente cantidad de agua
para disolver el sólido.
c) Luego agregar agua destilada hasta la línea de afora. Agite para homogenizar.
4.4. Preparar 50 mL de una solución de HCl 0,5 M a partir de HCl 6 N
a) Calcular el volumen necesario de HCl concentrado.
b) Medir el volumen calculado con una pipeta y con la ayuda de la bombilla de
succión.
c) Agregar el HCl concentrado en la fiola de 50 mL y agregar agua destilada hasta
la línea de aforo.
Ing. Víctor A. Campos Linares Período 2014-20
64
Preparación de Soluciones
Ing. Víctor A. Campos Linares Período 2014-20
65
Preparación de Soluciones
INFORME DE PRÁCTICA N° 08
Alumno: .................................................................................. Turno: ............
V. CÁLCULOS Y RESULTADOS:
5.1. Preparar 50 mL de una solución de NaCl al 2% (w/v)
5.2. Preparar 50 mL de una solución de NaCl 0,08N
5.3. Preparar 50 mL de una solución de C12H22O11 0,1 M
5.1. Preparar 50 mL de una solución de HCl 0,5 M a partir de HCl 6 N
VI. CONCLUSIONES:…………………………………………………………………………………
...........................................................................................................................
....................................................................................................................
..................................................................................................................
VII. CUESTIONARIO:
1. ¿Qué peso de soluto y de solvente, contienen 80 gramos de una solución de
KCl al 7,5%(w/w)?
Ing. Víctor A. Campos Linares Período 2014-20
66
Preparación de Soluciones
2. Calcule la cantidad de soluto en gramos contenidos en:
a) 0,5 equivalentes de NaOH
b) 0,8 moles de Ca(NO3)2
c) 0,05 equivalentes de Fe2(SO4)3
d) 0,08 mol de CuSO4
3. Se añaden 12 g de NaCl puro a 120 g de una solución de NaCl al 5 %(w/w).
Calcule el %(w/w) de la nueva solución. Rpta. 13,63 %
4. Marque las siguientes proposiciones como verdaderas (V) o falsas (F):
a) Una solución es una mezcla homogénea de dos o más sustancias .......... ( )
b) El soluto es el que está en mayor proporción en una solución ................ ( )
c) El factor “i” para el soluto, FeCl3 es igual a 3 equiv-gramo / mol ............ ( )
d) La molaridad es igual a la normalidad, cuando el factor “i” es igual a 1 .. ( )
e) Una solución saturada, contiene la máxima cantidad de soluto disuelto . ( )
f) En toda solución el solvente siempre es el agua ...................................... ( )
g) La concentración de una solución siempre es la relación soluto/solvente ( )
e) El aire es una solución gaseosa ............................................................. ( )
5. Para los compuestos dados a continuación indique el factor “i” (equiv./mol)
Fe(NO3)3 Al2(SO4)3
BaCl2.2H2O HNO3
Cu2(SO4) LiOH
H2SO4 Fe(SO4)
VIII. BIBLIOGRAFÍA:…………………………………………………………………………………
……………………………………………………………………………………………………………..
Ing. Víctor A. Campos Linares Período 2014-20
67
Dureza Total del Agua
PRÁCTICA N°09
ANÁLISIS DE AGUAS
Generalidades.- El agua es uno de los compuestos químicos más importantes para los
seres humanos y la vida en general, tal como se desarrolla en nuestro planeta puramente
cuantitativo, debemos indicar que el agua cubre aproximadamente 72 % de la superficie de
la tierra y el contenido en agua aproximado en agua en el hombre adulto es del 60 %.
Una característica singular del agua es la de ser la única sustancia química que en estado
natural se presenta en los tres estados físicos.
Parámetros Generales Indicadores de Contaminación.- Los podemos dividir en:
Parámetros de Parámetros de Parámetros de Parámetros de
carácter físico carácter químico carácter radioactivo carácter microbiológico
Características Salinidad y dureza
Radiación Bacterias
organolépticas
Turbidez y materias en pH: Acidez y Elementos
Virus
suspensión Alcalinidad individuales
Oxígeno disuelto
Hongos
Temperatura
Medidores de materia
Algas
Conductividad orgánica e inorgánica
Ing. Víctor A. Campos Linares Período 2014-20
68
Dureza Total del Agua
PRÁCTICA N° 09
DETERMINACIÓN DE LA DUREZA TOTAL EN EL AGUA
I. CAPACIDADES:
a) Determina la dureza cálcica y total de una muestra de agua en ppm de CaCO3.
II. FUNDAMENTO TEÓRICO:
La Dureza es una característica química del agua que está determinada por el
contenido de carbonatos, bicarbonatos, cloruros, sulfatos y ocasionalmente
nitratos de calcio y magnesio, pero principalmente, es debida a la presencia de los
cationes alcalinotérreos mayoritarios, Ca 2+ y Mg2+.
Agua, nombre común que se aplica al estado líquido del compuesto de hidrógeno y
oxígeno H2O. El agua pura es un líquido inodoro e insípido. Tiene un matiz azul,
que sólo puede detectarse en capas de gran profundidad. El agua es uno de los
agentes ionizantes más conocidos. Puesto que todas las sustancias son de alguna
manera solubles en agua, se le conoce frecuentemente como el disolvente
universal. El agua combina con ciertas sales para formar hidratos, reacciona con
los óxidos de los metales formando hidróxidos y actúa como catalizador en muchas
reacciones químicas importantes.
En su circulación por encima y a través de la corteza terrestre, el agua reacciona
con los minerales del suelo y de las rocas. Los principales componentes disueltos
en el agua superficial y subterránea son los sulfatos, los cloruros, los bicarbonatos
de sodio y potasio, y los óxidos de calcio y magnesio. Las aguas de la superficie
suelen contener también residuos domésticos e industriales.
Esta propiedad del agua es la que se estudiará en esta práctica; hay que decir que
la dureza del agua, además de ser la suma de las concentraciones de calcio y
magnesio, es la propiedad que tiene de precipitar el jabón y la formación de
sedimentos y costras en tuberías.
Definamos algunos términos:
Dureza Total: es la suma total de las concentraciones de sales de calcio y
magnesio, se mide por volumetría de complejación con EDTA (Ácido
etilendiaminotetracético), se expresa numéricamente en forma de carbonato de
calcio, CaCO3, principalmente en mg CaCO3 /L.
Dureza Temporal: es la que corresponde a la proporcionada por los
hidrógenocarbonatos de calcio y magnesio, desaparece por ebullición, pues
precipitan los carbonatos.
Dureza Permanente: es la que existe después de la ebullición del agua, corresponde
a la diferencia entre las dos anteriores. No puede ser eliminada por ebullición del
agua, su remoción únicamente es por medio de ablandamiento con cal, cal-soda e
intercambiadores iónicos como zeolitas y ciertas resinas.
Interpretación de la Dureza: el agua se clasifica generalmente en términos al
grado de dureza que posea de la siguiente forma:
Ing. Víctor A. Campos Linares Período 2014-20
69
Dureza Total del Agua
El Ministerio de Salud y la Organización Mundial de Salud clasifican y
establecen los siguientes límites para el agua potable.
Una elevada dureza del agua puede causar fundamentalmente problemas en
procesos de lavado y en calderas de vapor.
III. MATERIALES Y REACTIVOS:
Bureta de 50 mL Solución EDTA 0,02 N Negro de Eriocromo T (NET)
Matraz Erlenmeyer de 250 mL Solución NaOH al 10 % (w/v) Buffer dureza
Probeta de 50 mL Murexida Muestras de agua
IV. PROCEDIMIENTO:
4.1. Determinación de la dureza cálcica
En una probeta de 50 mL medir 40 mL de agua de su muestra y viértala en el
Matraz Erlenmeyer.
Adicionar aproximadamente 20 gotas de la solución de NaOH al 10 % con una
pizca del indicador murexida en el Matraz Erlenmeyer (color rojo vino).
Titular con la solución EDTA (Ácido etilendiaminotetracético) 0,02 N, hasta que
la solución se torne de color lila. Anote el volumen gastado.
Hacer los cálculos respectivos para determinar los mg de CaCO 3 / L de agua
(ppm).
4.2. Determinación de la dureza total
En una probeta de 50 mL medir 40 mL de agua de su muestra y viértala en el
Matraz Erlenmeyer.
Adicionar aproximadamente 5 mL de la solución de buffer dureza con una
pizca del indicador Negro de Eriocromo T en el Matraz Erlenmeyer (color rojo
vino).
Titular con la solución EDTA 0,02 N, hasta que la solución se torne de color
azul. Anote el volumen gastado.
Hacer los cálculos respectivos para determinar los mg de CaCO 3 / L de agua.
4.3. Determinación de la dureza magnésica
Se obtiene por diferencia de la dureza total menos la dureza cálcica.
Ing. Víctor A. Campos Linares Período 2014-20
70
Dureza Total del Agua
Ing. Víctor A. Campos Linares Período 2014-20
71
Dureza Total del Agua
INFORME DE PRÁCTICA N° 09
Alumno: .................................................................................. Turno: ............
V. CÁLCULOS Y RESULTADOS:
5.1. Dureza cálcica.
# equiv - g CaCO3 = # equiv – g EDTA
ppm de CaCO3 =
5.2. Dureza total.
# equiv - g CaCO3 = # equiv – g EDTA
ppm de CaCO3 =
Ing. Víctor A. Campos Linares Período 2014-20
72
Dureza Total del Agua
5.3. Dureza magnésica.
Dureza magnésica (ppm de CaCO3) = Dureza total - Dureza cálcica.
VI. CONCLUSIONES:…………………………………………………………………………………..
……………………………………………………………………………………………………………….
………………………………………………………………………………………………………………
………………………………………………………………………………………………………………
VII. CUESTIONARIO:
Se ha recibido 3,5 L de agua de regadío del valle de Jequetepeque para su
determinación y análisis en el Laboratorio de Química de la UPAO.
Una muestra de 30 mL. fue titulada con 21,7 mL de EDTA 0,02 N , usando como
indicador Negro de Eriocromo T más 5 mL. de una solución “Buffer dureza”
( pH=10,5)
Otra muestra con el mismo volumen fue titulada con 9,4 ml de EDTA con la misma
concentración, usando una pizca de murexida como indicador, más 0,5 mL (10
gotas) de NaOH al 10% (pH = 12,5). Datos: Ca = 40 C = 12 O = 16
Calcular:
a) La dureza cálcica en ppm de CaCO3
b) La dureza total en ppm de CaCO3
c) La dureza magnésica en ppm de CaCO3 y en ppm de MgCO3
VIII. BIBLIOGRAFÍA:………………………………………………………………………………
Ing. Víctor A. Campos Linares Período 2014-20
73
Determinación del pH
PRÁCTICA N° 10
DETERMINACIÓN DEL pH
I. CAPACIDADES:
a) Determina el grado de acidez o basicidad de una muestra mediante el uso de
papel indicador y de soluciones indicadoras.
b) Mide el pH de diferentes muestras en solución acuosa utilizando el papel
universal, la cinta multicolor y el pH-metro.
II. FUNDAMENTO TEÓRICO:
2.1. pH
El grado de acidez o basicidad de una solución indica la concentración de iones
hidrógeno (H+), la que se puede expresar en términos de pH. El pH de una
solución es el valor negativo del logaritmo decimal de la concentración, en mol/L,
del ión hidronio; así:
pH = - log [H3O +] = - log [H+]
Luego: [H +] = antilog [pH] = 10 - pH
Los niveles muy bajos de iones H+ en una solución acuosa se describen más
fácilmente en términos de valores de pH.
2.2. Escala de pH
Para soluciones acuosas es de 0 a 14. En soluciones ácidas la concentración de
[H+] es mayor que 10-7 y el pH tiene valores menores que 7.
En soluciones básicas, la concentración de [H+] es menor que 10-7 y el pH tiene
valores mayores que 7.
Solución pH pOH
Ácida <7 >7
Neutra 7 7
Básica >7 <7
Ing. Víctor A. Campos Linares Período 2014-20
74
Determinación del pH
2.3. Medición del pH
El pH es medido con instrumentos especiales llamados potenciómetros o pH-
metros. El pH aproximado de una solución puede ser determinado también
usando la cinta multicolor o el papel universal. La cinta multicolor y el papel
universal adquieren colores de acuerdo al pH del medio, el que se determina por
comparación con una escala de colores establecidos.
* El papel de tornasol solo determina si el medio acuoso es ácido o básico. El
cambio de azul a rojo indica que el medio es ácido y de rojo a azul indica que el
medio es alcalino.
III. MATERIALES Y REACTIVOS:
- pH – metro
- Cinta multicolor
- Papel universal
- Papel de tornasol
- Soluciones indicadoras
- Muestras diversas, etc.
IV. PROCEDIMIENTO:
4.1. Uso de la cinta multicolor y el papel universal
- Colocar cada muestra en su respectivo tubo de ensayo.
- Humedecer la cinta multicolor en cada muestra y determinar el valor del
pH por comparación de los colores que adquiere. Anotar la lectura.
- Repetir el procedimiento anterior con el papel universal para cada
muestra y determine el valor del pH por comparación de los colores que
adquiere. Anotar la lectura.
4.2. Uso del pH – metro
- Colocar cada muestra en un tubo de ensayo.
- Introducir el electrodo del pH – metro y anotar la lectura.
- Cada vez que cambie de muestra, lavar el electrodo con agua destilada y
secarlo.
4.3. Uso del papel de tornasol
- Introducir el papel de tornasol rojo en una muestra ácida y otro en una
muestra básica. Anotar el color final del papel.
- Repetir el mismo procedimiento para el papel de tornasol azul.
Ing. Víctor A. Campos Linares Período 2014-20
75
Determinación del pH
4.4. Uso de soluciones indicadoras
- La muestra ácida disponible, separarlo en tres partes aproximadamente
iguales.
- Añadir a cada muestra y por separado tres gotas de fenolftaleína,
anaranjado de metilo y verde de bromo cresol. Anote los colores
resultantes.
- A la muestra básica también separarlo en tres partes aproximadamente
iguales.
- Añadir a cada muestra y por separado tres gotas de fenolftaleína,
anaranjado de metilo y verde de bromo cresol. Anote los colores
resultantes.
Ing. Víctor A. Campos Linares Período 2014-20
76
Determinación del pH
Ing. Víctor A. Campos Linares Período 2014-20
77
Determinación del pH
INFORME DE PRÁCTICA N° 10
Alumno: .................................................................................. Turno: ............
V. CÁLCULOS Y RESULTADOS:
5.1. Lectura del pH
Papel Cinta [H+]
Muestra pH- metro
universal multicolor (Mol/L)
HCl(ac)
NaOH(ac)
leche gloria
cerveza
sprite
leche magnesia
jugo envasado
vinagre
5.2. Acidez y Basicidad
Papel de tornasol Soluciones indicadoras
Muestra
Rojo Azul A.M. Fenolftaleína V. bromo cresol
Ácida (HCl)
Básica (NaOH)
VI. CONCLUSIONES:……………………………………………………………………………..
………………………………………………………………………………………………………….
…………………………………………………………………………………………………………
VII. CUESTIONARIO:
7.1. Calcular el pH de cada una de las siguientes soluciones a 25ºC y
clasificarlas como ácidas, básicas o neutras.
a) Una solución con [H+] = 3,65 X 10 –8 M
Ing. Víctor A. Campos Linares Período 2014-20
78
Determinación del pH
b) Una solución con [OH-] = 9,53 X 10 –7 M
c) Una solución con pOH = 10,15
7.2. Calcular el pOH y la [H+] de las siguientes soluciones:
a) Una solución de HNO3 0,20 M
b) Una solución preparada por adición de 2,5 gramos de NaOH en agua
completando 250 mL de solución.
7.3. Determine el valor de pH, [OH-], [H+] y pOH en una disolución acuosa de
KOH cuya concentración es 850 mg de KOH / 850 mL de solución.
7.4. Indague los valores de pH para las siguientes sustancias:
Sustancia pH Sustancia pH
jugo de limón jugo de naranja
cerveza orina
sangre leche
jugo gástrico lágrimas
saliva vinagre
VIII. BIBLIOGRAFÍA: ………………………………………………………………………….
……………………………………………………………………………………………………….
……………………………………………………………………………………………………….
Ing. Víctor A. Campos Linares Período 2014-20
79
Apéndice 01
HOJA DE EJERCICIOS Nº 02
UNIDAD II: MATERIA Y MEDICIÓN
1. Materia: Clasificación y propiedades
1.1. Clasifique cada una de lo siguiente como sustancias puras o mezclas; si es
mezcla especificar si es homogénea o heterogénea.
a) agua de mar b) gasolina c) magnesio d) arroz con leche
e) aire f) arena g) jugo de tomate h) oro blanco
1.2. Escriba el símbolo químico de los siguientes elementos:
a) aluminio b) sodio c) cobre d) carbono e) cloro f) yodo
g) bromo h) oxígeno i) nitrógeno j) mercurio
1.3. Clasifique en elementos y compuestos:
a) NaCl b) Cl2 c) O2 d) HCl e) Au
f) KMnO4 g) NaHCO3 h) NaOH i) K2Cr2O7
1.4. Identifique como fenómeno físico o químico:
a) fundir hielo b) pulverizar una aspirina c) digerir una golosina
d) corrosión de un clavo e) explosión de nitroglicerina
1.5. Se enciende un fósforo y se sostiene bajo un trozo de metal frío. Se hacen las
siguientes observaciones:
a) El fósforo arde b) El metal se calienta c) se condensa agua sobre el metal
d) se deposita hollín
1.6. Prediga si los cambios siguientes son químicos o físicos:
a) Combustión del gas natural b) emisión de luz por foco incandescente
1.7. Cuál de los siguientes procesos es exotérmico y cual endotérmico:
a) combustión b) congelación del agua c) ebullición de agua
d) condensación del vapor.
1.8. Clasifique cada uno de los términos siguientes como elemento, compuesto o
mezcla
a) oxígeno b) te c) metano d) dióxido de carbono e) una uva
f) bronce g) acero h) amalgama dental
Ing. Víctor A. Campos Linares Período 2014-20
80
Apéndice 01
1.9. Establezca la diferencia entre:
a) Masa y peso d) Congelación y fusión
b) Elementos y compuestos e) Cambio físico y químico
c) Vaporización y condensación f) Mezclas homogéneas y
heterogéneas
1.10. Enumere cinco propiedades intensivas y cinco propiedades extensivas de la
materia.
1.11. Es una proposición falsa:
a) La lejía y el ácido muriático son mezclas homogéneas .............................. ( )
b) Todos los compuestos químicos están formados sólo por dos elementos ... ( )
c) La comprensión de un resorte es un fenómeno químico ........................... ( )
d) Una aleación es un ejemplo de solución sólida ....................................... ( )
e) Todas las sustancias homogéneas presentan dos o más fases .................. ( )
1.12. Identifique como verdadero (V) o falso (F) cada una de las siguientes
proposiciones:
a) Cuando la materia sufre un cambio físico no se produce modificación alguna en
su composición ....................................................................................... ( )
b) De un trozo de plata se han elaborado cadenas y aretes; se puede afirmar que la
plata ha sufrido un cambio químico ........................................................ ( )
c) Todo cambio de estado corresponde a un cambio físico ........................... ( )
d) Cuando se disuelve azúcar en un volumen de agua, se obtiene la formación de
nuevas sustancias .................................................................................. ( )
e) La representación NH3 corresponde a un elemento químico .................... ( )
f) La ductibilidad y maleabilidad son propiedades químicas de la materia .... ( )
g) Una mezcla homogénea se considera una disolución ............................... ( )
h) Algunas propiedades físicas de la materia son cuantificables ................... ( )
i) La Química Analítica Cualitativa identifica los elementos de una sustancia( )
j) La expansibilidad es una propiedad específica de la materia ..................... ( )
k) El sabor es una propiedad intensiva de la materia ................................... ( )
1.13. Llene el espacio efectuando la conversión que se indica:
a) 1822 m Km g) 130 °K °F
b) 526 L mL h) 80 °F °C
c) 345 galones cm3 i) 2.63 g/cm3 lb/pie3
d) 68 libras g j) 5.57 g/cm3 lb/pie3
e) 48 °F °C k) 2 atm mmHg
f) 285 °F °K l) 970 mmHg lb/pulg2
Ing. Víctor A. Campos Linares Período 2014-20
81
Apéndice 01
g) 9.58 m Km m) 330 °K °F
h) 126 L mL n) 50 °F °C
i) 200 galones cm3 o) 5.63 g/cm3 lb/pie3
j) 2.50 libras g p) 2.57 g/cm3 lb/pie3
k) 28 °F °C q) 5 atm mmHg
l) 485 °F °K r) 770 mmHg lb/pulg2
1.14. Análisis dimensional:
a) Una libra de café en grano rinde 50 tazas de café (4 tazas = 946 mL) ¿Cuántos
mililitros de café se pueden preparar con 1 gramo de café en grano?
b) Una varilla cilíndrica de silicio tiene 16,8 cm de longitud y una masa de 2,17 Kg.
La densidad del silicio es de 145,3 lb/pies3. ¿Qué diámetro en cm tiene el
cilindro? El volumen de un cilindro esta dado por 3,1416(r)2(h), donde r es el
radio y h es la altura.
c) Un pronosticador del tiempo predice que durante el día la temperatura alcanzará
31°C. Exprese esa temperatura en °K y °F.
d) Se ha estimado que la explotación del oro (Au) en la Minera Yanacocha para el
año 2011será de 20,4 TN. Si en el mercado internacional el precio del oro es de
1685 dólares por onza y el costo de producción es de 525 dólares/onza ¿Cuál es
la utilidad o ganancia anual en soles, proyectada para dicha empresa?
Datos: 1 onza = 28, 35 gramos; 1 dólar = 2, 80 soles; 1 TN = 1000 Kg
e) Se dispone de un tanque esférico para almacenar alcohol metílico. Si es llenado
completamente en 4400 segundos con una alimentación continua de 0,6 m 3 de
alcohol por cada 15 segundos.
Determine el diámetro en metros de dicho tanque. V tanque= (4/3).π.r3
Ing. Víctor A. Campos Linares Período 2014-20
82
UNIVERSIDAD PRIVADA ANTENOR ORREGO Apéndice 01
HOJA DE EJERCICIOS N° 03
UNIDAD III: ESTRUCTURA ATÓMICA Y TABLA PERIÓDICA
1. ¿Cuántos protones y neutrones tiene el azufre de Z= 31?
a) 2 protones, 16 neutrones b) 16 protones, 31 neutrones
c) 16 protones, 15 neutrones d) 15 protones, 16 neutrones
2. Con ayuda de una Tabla Periódica, llenar los espacios vacíos del cuadro,
suponiendo que cada columna representa un átomo neutro.
52
Símbolo Cr
Protones (Z) 33 77
Neutrones (nº) 42 20
Electrones (e-) 20 86
Número masa (A) 222 193
3. Llenar los espacios vacíos de la tabla, suponiendo que cada columna representa un
átomo neutro.
121
Sb
Símbolo
Protones(Z) 38 94
Neutrones(nº) 50 108
Electrones(e-) 74 57
Número masa(A) 139 239
4. El cloro de origen natural se compone de dos isótopos: 35Cl y 37Cl. ¿Cuántos
neutrones hay en cada isótopo?
a) 17, 17 b) 17,19 c) 19, 21 d) 18,20 e) 18,18
5. Un elemento tiene 22 protones, 20 electrones y 26 neutrones. ¿De cuál isótopo se
trata?
a) 4726Fe b) 4826Fe c) 4822Ti d) 4822T i2+
Ing. Víctor A. Campos Linares Período 2014-20
83
Apéndice 01
6. Uno de los componentes más dañinos de los residuos nucleares es un isótopo
radiactivo del estroncio 90Sr (Z=38); puede depositarse en los huesos, donde
sustituye al calcio. ¿Cuántos protones y neutrones hay en el núcleo del Sr-90?
a) protones 90; neutrones 38 b) protones 38; neutrones 90
c) protones 38; neutrones 52 d) protones 52; neutrones 38
7. El elemento oxígeno se compone de tres isótopos cuyas masas son de 15,994915,
16,999133 y 17,99916. Las abundancias relativas de estos tres isótopos son de
99,7587, 0,0374 y 0,2049, respectivamente. A partir de estos datos calcule la
masa atómica media del oxígeno.
8. Definir los números cuánticos: n, l, m, s y cuáles son los valores permitidos
para cada uno de ellos.
9. Determine los valores numéricos cuánticos para:
a) El segundo electrón añadido a un átomo de Li (Z = 3)
b) El último electrón añadido a un átomo de P (Z =15)
c) El décimo electrón añadido a un átomo de Ca (Z = 20)
d) El quinto electrón añadido a un átomo de O (Z = 8)
e) El octavo electrón añadido a un átomo de Al (Z = 13)
10. Cite los valores de n y l que corresponden a:
a) 2p b) 6d c) 4f d) 7s e) 5p
11. Considerando el Principio de Exclusión de Pauli y las Reglas de Hund; escriba la
configuración electrónica de los siguientes elementos, sugerencia no usar la Tabla
Periódica:
a) S (Z = 16) b) B (Z = 5) c) F (Z = 9) d) Zn (Z = 30) e) I (Z = 53)
12. Defina: Paramagnetismo y Diamagnetismo.
13. Cuántos electrones hay en:
a) En el tercer nivel (n = 3) del elemento con Z = 30
b) En el cuarto nivel (n = 4) del elemento con Z = 40
c) En el segundo nivel (n = 2) del elemento con Z = 10
14. Cuál es el Número Atómico (Z) del elemento cuya configuración electrónica finaliza
en:
a) 6s1 b) 5p5 c) 4s1 d) 3d 6 e) 5f 3
15. ¿Cuántos electrones hay en el cuarto nível energético del elemento com número
atômico 23?
16. El elemento químico cuya configuración electrónica finaliza em 4p 4 tiene La
siguiente distribución electrónica:
a) 2,8,18,4,2 b) 2,8,8,14,2 c) 2,18,8,6 d) 2,8,8,12,6 e) 2,8,18,6
17. Cuál de los siguientes es un conjunto de números cuánticos posibles para un
electrón que se encuentra en el orbital 3d.
a) 3 , 3 , 2 , +1 / 2 b) 3 , 2 , 0 , - 1 / 2 c) 4 , 3 , 2 , - 1/ 2
Ing. Víctor A. Campos Linares Período 2014-20
84
Apéndice 01
Ing. Víctor A. Campos Linares Período 2014-20
85
Apéndice 01
HOJA DE EJERCICIOS Nº 04
UNIDAD II: GASES IDEALES
1.- Una cantidad de gas ocupa un volumen de 80 mL a una presión de 750 mm Hg
¿Qué volumen ocupará a una presión de 1,2 atm si la temperatura no cambia ?
2.- El volumen inicial de una cierta cantidad de gas es de 200 mL a la temperatura de
20ºC. Calcula el volumen a 90ºC si la presión permanece constante.
3.- Una cierta cantidad de gas se encuentra a la presión de 790 mm Hg cuando la
temperatura es de 25ºC. Calcula la presión que alcanzará si la temperatura sube
hasta los 200ºC.
4.- Disponemos de un recipiente de volumen variable. Inicialmente presenta un
volumen de 500 mL y contiene 34 g de amoníaco. Si manteniendo constante la P y la
T, se introducen 68 g de amoníaco. ¿Qué volumen presentará finalmente el recipiente?
Rpta: 1,499 L
5.- Si tenemos 1,0 mol de gas a 1,0 atm de presión a 0°C (273,15 °K) ¿Cuál será el
volumen? Rpta: 22,41 L
6.- Calcular lo que se indica:
a) El volumen en litros ocupado por 0,460 moles de CO a 2,54 atm y 26 °C.
b) El volumen que ocupan 3,50 g Cl 2 (g) a 25 °C y 1,80 bar.
c) ¿Cuál es la masa molar de un gas si 1,81 g del gas ocupa un volumen de 1,52 L
a 25 °C y 737 mm Hg?
d) ¿Cuál es el volumen que ocupará una muestra de 10,25 g de gas ozono, O3 a 24
°C y 750 torr?
7.- ¿Qué volumen ocuparían 3,15 moles de hexafluoruro de azufre, SF 6 si la
temperatura y la presión del gas son 18 ºC y 2,40 bar?
8.- Calcule la densidad del gas acetileno (C 2H2) en las siguientes condiciones:
a) A TPE (0°C y 1 atm) b) A 25 °C y 1,40 atm c) A 20 °C y 1,013 bar
9.- Calcule la densidad del anhídrido sulfúrico, SO3 en las siguientes condiciones:
a) A TPE b) A 23 °C y 0,970 atm c) A 25 °C y 830 torr
10.- Calcule la densidad del gas monóxido de dinitrógeno, N 2O en las siguientes
condiciones: a) A TPE b) A 27 °C y 0,985 atm
11.- ¿Cuántos gramos pesará una muestra de 8,0 L de gas propano (C3H8) que está a
25 °C y 1,0 atm?
12.- Calcule la masa molar de un gas sabiendo que una muestra de 50,0 g este gas se
encuentra en un cilindro de 100 L a 30 °C y 4,78 atm.
13.- Calcule el peso molecular del aire (g/mol) suponiendo que su composición
volumétrica es 79% de N2 y 21% de O2.
14.- ¿Cuál es la densidad del aire (g/L) a condiciones estándar? Suponga que el aire
se comporta como gas ideal. Rpta: 0, 7762 g/L
15.- Se tienen 375 litros de gas medidos a 25ºC y 10 atm de presión. Sufre una
transformación isocórica al elevarse la temperatura a 263 º C. Hallar la presión final
del sistema. Rpta: 17,98 atm
16.- En un recipiente de 100 L hay 25 g de oxígeno y 75 g de nitrógeno a 0 ºC. ¿Cuál
es la presión que ejerce la mezcla gaseosa? ¿Cuál es la presión que ejerce
cada gas? Rpta: PT = 0,77 atm; P(O2) = 0,17 atm; P(N2) = 0,60 atm
Ing. Víctor A. Campos Linares Período 2014-20
86
Apéndice 01
17.- Una muestra de O2, contenida en un recipiente de 1 L, ejerce una presión de 800
mm Hg a 25 ºC. En otro recipiente de 3 L, una muestra de N2 ejerce una presión de
1,5 atm a 50 ºC. Se mezclan las dos muestras introduciéndolas en un frasco de 9 L a
40 ºC. Calcular: a) La presión parcial de cada gas y, b) La presión total.
Rpta: a) PN2 = 0,485 atm; PO2 = 0,123 atm b) 0,608 atm
18.- En un recipiente de volumen fijo se introducen 10 g de NO 2, que ejercen una
presión de 430 mm Hg a una determinada temperatura, T. Si se añaden 3 g de CO 2 y
6 g de N2, y se duplica la temperatura: a) ¿Cuál será la presión parcial de cada gas en
la mezcla? Y b) ¿Cuál la presión total? Rpta: a) PCO2 = 0,355 atm; PN2 = 1,115 atm;
PNO2 = 1,132 atm; b) PT= 2,602 atm
19.- Una mezcla de O2 y H2, con un 15% en peso de este último, se encuentra en un
recipiente cerrado a 120 ºC y 1 atm. Calcule: a) La presión parcial de cada gas y b) La
densidad de la mezcla. Rpta: a) PH2 = 0,738 atm; PO2 = 0,262 atm b) 0,306 g/L
20.- Sabiendo que 3,5 moles de NH3 ocupan 5,20 L a 47°C, calcule la presión del gas
en atm utilizando la ecuación del gas ideal y la ecuación de van der Waals.
Rpta: 17,7 atm y 16,2 atm
Ing. Víctor A. Campos Linares Período 2014-20
87
Apéndice 01
HOJA DE EJERCICIOS N° 05
UNIDAD IV: ARITMÉTICA QUÍMICA
Haciendo uso de la tabla periódica de los elementos, desarrollar los ejercicios siguientes:
1. Determinar los pesos moleculares de cada uno de los compuestos siguientes:
a) H2S b) N2O5 c) Mg(OH)2 d) KNO3 e) Al(NO3)3 f) NH4SO4
2. Calcular el porcentaje en masa de oxígeno (%O), en cada uno de los compuestos
siguientes:
a) SO2 b) K3PO4 c) BaSO4 d) Mg(OH)2
3. Calcular lo que se le indica:
a) Masa (g) de 1,73 mol CO2
b) Moles de Mg(NO3)2 en 240 g de esta sustancia
c) Número de moléculas en 0,56 mol CH3OH
d) Número de átomos de hidrógeno en 0,988 mol C4H10
4. Calcular las masas de lo siguiente:
a) 4,11 mol He b) 1,5 mol Fe c) 4,5 mol Ag d) 0,3 mol Pb
5. Calcular el número de moles en:
a) 35,2 g de CaS b) 110 g de N 2O c) 1,8 g de CO2 d) 1,5 g de NaNO3
6. Calcular el peso en gramos presente en:
a) 1,34 mol Na2SO4 b) 2,5 mol NaCl c) 2,8 mol NaOH d) 1,8 mol CuO
7. Determinar:
a) Peso de calcio contenido en 1,2 mol de Ca(NO 2)2. (Ca = 40; N = 14; O = 16)
b) Peso de magnesio contenido en 150 g de MgO. (Mg = 24; O = 16)
c) Peso de sodio contenido en 4 moles de NaOH. (Na = 23; O = 16; H = 1)
8. Determine el peso formular del siguiente compuesto: Ba3(PO4)2
9. Con base en la fórmula estructural siguiente, calcule el porcentaje de carbono
presente en el ácido benzoico, C6H5(COOH).
10. Calcular el número de átomos de oxígeno en:
a) 20 g de H2O2 b) 25 g de HNO3 c) 2 moles de H2O2 d) 7 moles de HNO3
Ing. Víctor A. Campos Linares Período 2014-20
88
Apéndice 01
11. Calcular el número de moléculas en:
a) 0,38 g NaOH b) 1,69 g Ca(OH)2 c) 0,83 moles NaOH d) 0,82 moles
Ca(OH)2
12. ¿Cuál es la masa en gramos de 0,257 mol de sacarosa, C12H22O11?
13. Una muestra de glucosa C6H12O6, contiene 4,0 x 1022 átomos de carbono. ¿Cuántos
átomos de hidrógeno y cuántas moléculas de glucosa contiene la muestra?
14. Calcule el número de moléculas presentes en 1,75 g de propano, CH3CH2CH3
15. Se mezclan 750 g de K2Cr2O7 con 300 g de K2CrO4 y 20 g de K2O. Calcule el
porcentaje de Cr y de K en la mezcla resultante.
16. Los moles de NaCl y de NaBr a fin de preparar 120 g de una mezcla con 18% de Na.
Ing. Víctor A. Campos Linares Período 2014-20
89
Apéndice 01
HOJA DE EJERCICIOS N° 06
UNIDAD IV: REACTIVIDAD QUÍMICA
I. Escriba ecuaciones químicas balanceadas que correspondan a cada una de las
descripciones siguientes:
1. El carburo de calcio sólido, CaC2, reacciona con agua para formar una
disolución acuosa de hidróxido de calcio, Ca(OH)2 y acetileno gaseoso, C2H2.
2. Cuando se calienta clorato de potasio sólido, KClO3 se descompone para formar
cloruro de potasio sólido y oxígeno gaseoso.
3. El zinc metálico sólido reacciona con ácido sulfúrico, H2SO4 para formar
hidrógeno gaseoso y una disolución acuosa de sulfato de zinc.
4. Si se agrega tricloruro de fósforo, PCl3 líquido a agua, reacciona para formar
ácido fosforoso acuoso, H3PO3(ac) y ácido clorhídrico acuoso.
5. Cuando se hace pasar sulfuro de hidrógeno, H2S sobre hidróxido de hierro (III)
sólido caliente, la reacción resultante produce sulfuro de hierro (III) sólido y agua
gaseosa.
6. Cuando trióxido de azufre gaseoso, SO3 reacciona con agua, se forma una
disolución de ácido sulfúrico.
7. La fosfina, PH3(g) se quema en oxígeno gaseoso para formar agua gaseosa y
decóxido de tetrafósforo sólido, P4O10 .
8. Si se calienta nitrato de mercurio (II) sólido, se descompone para formar óxido de
mercurio(II) sólido, dióxido de nitrógeno gaseoso, NO2 y oxígeno.
Ing. Víctor A. Campos Linares Período 2014-20
90
Apéndice 01
9. El cobre metálico reacciona con una disolución concentrada caliente de ácido
sulfúrico para formar sulfato de cobre(II) acuoso, dióxido de azufre gaseoso, SO2
y agua.
10. Hidróxido de níquel (II) se descompone para dar óxido de níquel(II), NiO y agua al
calentarse.
11. El aditivo para gasolina MTBE (metil ter-butil éter), C5H12O (l), se quema en aire.
12. Un “volcán artificial” puede fabricarse calentando dicromato de amonio sólido,
(NH4)2Cr2O7, que se descompone en nitrógeno, óxido de cromo(III), Cr2O3 y vapor
de agua.
13. El carbono reacciona con el ácido nítrico, HNO 3, para producir dióxido de
nitrógeno, dióxido de carbono y agua.
14. El ácido sulfúrico reacciona con el yoduro de hidrógeno, HI para producir
dióxido de azufre, SO2, yodo, I2 y agua.
15. A altas temperaturas el nitrato de sodio (un fertilizante), forma nitrito de sodio,
NaNO2 y oxígeno.
16. Los compuestos de mercurio son muy venenosos. El nitrato mercúrico reacciona
con sulfuro de sodio, Na2S para formar sulfuro de mercurio (II), HgS que es muy
insoluble y nitrato de sodio.
Ing. Víctor A. Campos Linares Período 2014-20
91
Apéndice 01
17. Los huesos humanos están formados, principalmente, por fosfato de calcio,
Ca3(PO4)2. El cloruro de calcio reacciona con fosfato de potasio, K3(PO4) para
formar fosfato de calcio y cloruro de potasio.
18. El heptóxido de dicloro, Cl2O7 reacciona con agua para formar ácido perclórico.
19. El peróxido de hidrógeno, H2O2, se emplea como antiséptico. La sangre ocasiona
que se descomponga en agua y oxígeno.
20. La combustión completa para la acetona, C3H6O (l).
21. La nitroglicerina, C3H5N3O9, es un explosivo que se descompone en nitrógeno,
dióxido de carbono, agua y oxígeno.
22. La combustión completa del combustible Diesel, C14H30.
23. Cuando el nitrato de amonio sólido, NH4NO3, se encuentra con
combustóleo, C17H36 líquido, hacen una mezcla altamente explosiva, dando
como productos nitrógeno, N2, dióxido de carbono y agua, todos en estado
gaseoso.
Ing. Víctor A. Campos Linares Período 2014-20
92
Apéndice 01
HOJA DE EJERCICIOS N° 07
UNIDAD IV: REACTIVIDAD QUÍMICA
I. Balancear las siguientes ecuaciones por tanteos e indicar el tipo de
reacción:
a) Fe(s) + O2(g) Fe2O3
b) Ca + HCl CaCl2 + H2
c) SO2(g) + O2(g) SO3(g)
d) Ca(OH)2 + HNO3 Ca(NO3)2 + H2O
e) C4H10O(l) + O2(g) CO2(g) + H2O(g)
f) Fe(OH)3(s) + H2SO4(ac) Fe2(SO4)3(ac) + H2O(l)
g) Mg3N2(s) + H2SO4(ac) MgSO4(ac) + (NH4)2SO4(ac)
h) Li(s) + N2(g) Li3N(s)
i) Ca3P2(s) + H2O(l) Ca(OH)2(ac) + PH3(g)
j) Al(OH)3(s) + HClO4(ac) Al(ClO4)3(ac) + H2O(l)
k) AgNO3(ac) + Na2SO4(ac) Ag2SO4(s) + NaNO3(ac)
II. Clasificar las siguientes reacciones como de: combinación, descomposición
o combustión y balancear por tanteos.
a) Al(s) + Cl2(g) AlCl3(s)
b) BaCO3(s) + calor BaO(s) + CO2(g)
c) C2H4(g) + O2(g) CO2(g) + H2O(g)
d) Li(s) + N2(g) Li3N(s)
e) PbCO3(s) PbO(s) + CO2(g)
f) C3H6(g) + O2(g) CO2(g) + H2O(g)
g) H2O2(l) λ H2O(l) + O2(g)
h) Fe(NO3)2(ac) + Al (s) Fe (s) + Al(NO3)3 (ac)
i) PbS(s) + H2O2(ac) PbSO4 (s) + H2O(l)
Ing. Víctor A. Campos Linares Período 2014-20
93
Apéndice 01
HOJA DE EJERCICIOS N° 08
UNIDAD V: REACCIONES REDOX
I. Balancear las siguientes ecuaciones Redox. Indique los procesos de
oxidación y de reducción. Usar el método del ión electrón.
a) H2S + HNO3 S + NO + H2O
b) KMnO4 + FeSO4 + H2SO4 MnSO4 + Fe2(SO4)3 + K2SO4 + H2O
c) NaI + Fe2(SO4)3 I2 + FeSO4 + Na2SO4
d) KMnO4 + H2O2 + H2SO4 O2 + MnSO4 + K2SO4 + H2O
e) KI + H2SO4 H2S + H2O + I2 + K2SO4
f) HNO3 + HI NO + I2 + H2O
g) NaNO2 + H2SO4 + KMnO4 NaNO3 + K2SO4 + MnSO4 + H2O
h) CH3CH2OH + H2SO4 + K2Cr2O7 CH3CHO + Cr2(SO4)3 + K2SO4 + H2O
i) KBr + K2Cr2O7 + H2SO4 Br2 + K2SO4 + Cr2(SO4)3 + H2O
j) Cr2(SO4)3 + Ca(MnO4)2 + H2O H2Cr2O7 + MnSO4 + CaSO4 + H2SO4
l) MnO + PbO2 + HNO3 HMnO4 + Pb(NO3)2 + H2O
ll) Cr(OH)3 + NaClO + NaOH Na2CrO4 + NaCl + H2O
m) S + K2Cr2O7 + H2O SO2 + Cr2O3 + KOH
n) KMnO4 + Fe(HCO3)2 + H2O MnO2 + Fe(OH)3 + CO2 + KHCO3
o) NaCN + NaClO + NaOH Na 2CO3 + N2 + NaCl + H2O
p) KMnO4 + Zn + H2O MnO2 + Zn(OH)2 + KOH
q) Pb + Sb + KOH PbO + KSbO 2 + H2O
r) Cr2(SO4)3 + KI + KIO3 + H2O Cr(OH)3 + K2SO4 + I2
s) Cl2 + KOH KCl + KClO3 + H2O
t) HSCN + KMnO4 + H2SO4 MnSO4 + K2SO4 + HCN + H2O
u) Ca(IO3)2 + KI + HCl CaCl2 + KCl + I2 + H2O
v) CeO2 + KI + HCl CeCl3 + KCl + I2 + H2O
w) Pb + Cu2S + HNO3 Pb(NO3)2 + Cu(NO3)2 + NO2 + S + H2O
x) KClO3 + HI + H2SO4 KHSO4 + HCl + I2 + H2O
Ing. Víctor A. Campos Linares Período 2014-20
94
Apéndice 01
HOJA DE EJERCICIOS N° 09
UNIDAD VI: ESTEQUIOMETRÍA
I. Calcular lo que se le indica:
1. El gasohol contiene alcohol etílico, C2H5OH, el cual arde según la siguiente
reacción: C2H5OH + O2 2CO2 + H2O
a) Si se queman 500 g de alcohol etílico de esta forma ¿Cuántos gramos de O 2 se
necesitan?
b) Si en una prueba con esta reacción se formaron 350g de CO 2 ¿Cuántos gramos
de alcohol etílico se quemaron?
c) Si esta reacción consume 100gramos de O2 ¿Cuántos gramos de agua se forman?
2. Una muestra de 4,5 moles de aditivo para gasolina llamado t – butilmetiléter,
C3H12O, se quema en presencia de aire. Calcule la masa de cada uno de los
productos que se forman.
3. El combustible Diesel, C14H30, el cual se quema según la siguiente reacción:
C14H30 + O2 CO2 + H2O
a) Si se queman 800 g de combustible Diesel de esta forma ¿Cuántos gramos de O2
se necesitan?
4. Un elemento X forma un yoduro XI3 y un cloruro XCl3. El yoduro se convierte
cuantitativamente en I2 cuando se calienta en una corriente de cloro en exceso;
así: 2XI3 + 3Cl2 2XCl3 + I2
Si se trata 0,5 g de XI3, se obtiene 0,236 g de XCl3.
a) Calcule el peso atómico del elemento X. Rpta: 138,62
b) Identifique al elemento X.
5. Las bolsas de aire de los automóviles se inflan cuando la azida de sodio, NaN3 se
descompone rápidamente en sus elementos componentes.
a) Escriba y balancee la ecuación química para esta reacción.
b) ¿Cuántos gramos de azida de sodio se requieren para producir 45 mL de
nitrógeno gaseoso, si la densidad de este gas es de 1,25 g/mL?
6. La combustión completa de octano, C8H18, un componente de la gasolina, procede
así: 2C8H18(l) + 25O2(g) 16 CO2(g) + 18H2O(g)
a) ¿Cuántos moles de O2 se necesitan para quemar 0,676 mol de C8H18?
b) ¿Cuántos gramos de O2 se necesitan para quemar 2000 g de C8H18?
7. Un fabricante de bicicletas tiene 4250 ruedas, 2755 armazones y 2255 pedales.
a) ¿Cuántas bicicletas pueden fabricar?
b) ¿Cuántas componentes de cada tipo sobran?
c) ¿Cuál componente limita la producción de bicicletas?
Ing. Víctor A. Campos Linares Período 2014-20
95
Apéndice 01
8. Cuando se calienta, el litio reacciona con nitrógeno formando nitruro de litio:
6 Li(s) + N2(g) 2 Li3N(s)
a) ¿Cuál es el rendimiento teórico, en gramos de Li3N, cuando 12 g de Li se
calientan junto con 33 g de N2?
b) Si el rendimiento real en Li3N es de 5,5 g, ¿Cuál es el rendimiento porcentual
para la reacción?
9. Las soluciones de carbonato de sodio y nitrato de plata reaccionan para formar
carbonato de plata sólido y una solución de nitrato de sodio. Una disolución
que contiene 10 g de carbonato de sodio se mezcla con otra que contiene 10g de
nitrato de plata ¿Cuántos gramos de Na2CO3, AgNO3, Ag2CO3 y NaNO3 están
presentes al término de la reacción?
10. La plata se oscurece en presencia de sulfuro de hidrógeno al formarse un
sulfuro de plata; así: 4Ag + 2H2S + O2 2Ag2S + 2H2O
¿Cuánto Ag2S se obtiene al mezclar 3 g de Ag, 5 g de H2S y 7 g de O2?
11. El amoniaco se obtiene a partir del H2(g) y el N2(g) . Si se mezclan 50 gramos de
cada reactivo.
a) ¿Cuál es el reactivo limitante?
b) ¿El rendimiento teórico y el porcentaje de rendimiento si sólo se obtiene 30 g de
NH3?
c) ¿Qué cantidad del reactivo en exceso queda sin reaccionar?
12. Cuando el benceno (C6H6), reacciona con bromo (Br2), se obtiene bromobenceno
(C6H5Br); así: C6H6 + Br2 C6H5Br + HBr
a) Calcule el rendimiento teórico de bromobenceno en esta reacción si 40 g de
benceno reacciona con 75 g de bromo.
b) Si el rendimiento real de bromobenceno fue de 56,7 g. Calcule el porcentaje de
rendimiento.
13. El óxido de etileno, C2H4O, un fumigante que se emplea en ocasiones como
exterminador de plagas, se sintetiza con rendimiento del 89 % mediante la
reacción:
C2H5OBr + NaOH C2H4O + NaBr + H2O
¿Cuántos gramos de etilenbromohidrina se consumirán para producir 255 g de
óxido de etileno con rendimiento de 89 %?
14. En la industria el hidrógeno gaseoso se prepara por la reacción del
propano,C3H8, gaseoso con vapor a 400°C. Los productos son monóxido de
carbono e hidrógeno gaseoso.
Ing. Víctor A. Campos Linares Período 2014-20
96
Apéndice 01
a) Escriba la ecuación balanceada.
b) ¿Cuál es el rendimiento de la reacción a partir de 2,90 toneladas de propano si
se producen 400 Kg de gas hidrógeno?
15. El titanio, un metal fuerte, ligero y resistente a la corrosión, se utiliza en la
construcción de naves espaciales, aviones, en sus motores y para la fabricación de
bicicletas.
Se obtiene mediante la reacción siguiente:
TiCl4(g) + 2Mg(l) Ti(s) + 2MgCl2(l)
En cierto proceso industrial 3,54X107 g de TiCl4 se hacen reaccionar con 1.13X107 g
de Mg.
a) Calcule el rendimiento teórico de Ti, en gramos.
b) Calcule el rendimiento porcentual si en la práctica se obtienen 7,91X106 g de
Ti.
16. Cuando se calienta, el litio reacciona con nitrógeno formando nitruro de litio:
6 Li(s) + N2(g) 2 Li3N(s)
a) ¿Cuál es el rendimiento teórico, en gramos de Li3N, cuando 12 g de Li se calientan
junto con 33 g de N2?
b) Si el rendimiento real en Li3N es de 5,5 g, ¿Cuál es el rendimiento porcentual
para la reacción?
17. Dada la ecuación: Mg 3N2 + H2O Mg(OH)2 + NH3
a) ¿Cuál será el peso en gramos de Mg(OH)2 y la cantidad de NH3 en moles que puedan
producirse por la reacción de 80 g de Mg3N2 y 3,1 moles de H2O?
18. En la reacción: 4NO2 + O2 + 2H2O 4HNO3
a) Si se hacen reaccionar 10 gramos de cada uno de los reactantes, finalizada la
reacción ¿Cuántos gramos de cada sustancia quedan al final de la reacción?
19. Se lleva a cabo la siguiente reacción:
3A + 4B 2C + 3D + 3E
Los pesos moleculares son: A= 100; B= 150; C=85. Se dejó reaccionar una muestra de
50 g de A con 75 g de B.
a) ¿Cuántos gramos de C pueden producirse?
b) Calcule la cantidad de moles del reactivo en exceso que queda al final de la
reacción.
Ing. Víctor A. Campos Linares Período 2014-20
97
Apéndice 01
HOJA DE EJERCICIOS Nº 10
UNIDAD VII: CONCENTRACIÓN DE SOLUCIONES
1.-¿Cuántos gramos de soluto son necesarios para preparar cada una de las
siguientes soluciones?
a) 500 g de una solución de NaCl al 3 % (w/w)
b) 250 g de una solución de NaOH al 2,5 % (w/w)
c) 100 mL de una solución de KI al 5 % (w/v)
d) 50 mL de una solución de Ca(NO3)2 al 3,5 % (w/v)
e) 300 mL de una solución de AgNO3 500 ppm
f) 1000 mL de una solución de Pb(NO3)2 750 ppm
g) 350 mL de una solución de Ca(OH)2 0,2 M
h) 350 mL de una solución de Ca(OH) 2 0,2 N
2.-Calcule la concentración molar, M de cada disolución que contiene:
a) 4,75 g de NaOH en 0,2 L de solución
b) 7,88 g de Na2CO3 en 250 mL de solución
c) 540 mg de NaCl en 50 mL de solución
d) 660 mg de KClO3 en 100 mL de solución
e) 0,18 mol de HNO3 en 2000 mL de solución
f) 0,04 equiv de Fe(NO3)3 en 50 mL de solución
3.- 400 gramos de una solución acuosa contiene 20 g de NaOH. Determinar su
concentración en por ciento en peso.
4.- En 600 g de agua se disuelven 15 g de NaNO3. Su concentración en por ciento
en peso es:
5.- ¿Cuántos gramos de FeCl3 están disueltos en 1,5 Kg de solución al 25 %(w/w)?
6.- En 1,4 L de solución hay 95,08 g de ácido sulfúrico. Determine la normalidad y
molaridad.
7.- Peso de soluto esta disuelto en:
a) 250 mL de solución de KOH 0,4 M
b) 500 mL de solución de HNO3 1,1070 N
c) 750 mL de solución de Al(OH)3 600 ppm
8.- A 200 mL de NaOH 1,4 M se le añade 50 mL de agua. La molaridad de la
solución resultante es:
9.-Se dispone de 50 mL de una solución de CuSO4 0,1 M. ¿Cuál será la molaridad
de 10 mL de esta solución?
10.- Se mezclan 150 mL de una solución de HCl 2,0 M con 350 mL de una
solución de HCl 1,0 M. Determine la molaridad de la solución resultante.
Ing. Víctor A. Campos Linares Período 2014-20
98
Apéndice 02
11.- Calcular el % de HNO3 que contendrá una mezcla de 2 litros de HNO3 con una
densidad 1,42 g/mL y 69,6 %(w/w) de HNO3 con 4 litros del mismo ácido de
densidad 1,106 g/mL y 18,16 %(w/w) de HNO3. Resp: 38,27%(w/w)
Preparación de soluciones por dilución.
12.-El ácido acético concentrado, CH3COOH es 17 M ¿Cómo podrían prepararse 100
mL de CH3COOH 1,8 N?
13.- El ácido nítrico concentrado, HNO3 es 16 M ¿Cómo podría prepararse 500 mL de
HNO3 2 M?
14.- En el laboratorio de química se dispone de HClcc con las siguientes
especificaciones: 36,5 %(w/w) ; densidad = 1,19 g soluc./ mL soluc.
¿Cuántos mL de HClcc se necesitan para preparar 2 L de una solución de HCl 2 M?
15.- Se dispone del ácido sulfúrico comercial (96,4% en peso, densidad= 1,84 g/ mL)
¿Cuántos mililitros de este ácido se requieren para preparar 1,5 L de una solución
de H2SO4 2,5 M?
16.- La densidad de una disolución de ácido nítrico del 32% en peso es de 1,19 g/mL.
a) ¿Cuántos gramos de ácido nítrico puro están presentes en 250 mL de disolución?
b) ¿Cuántos moles de ácido nítrico hay en este volumen de disolución?
c) ¿Cuál es la molaridad de dicha disolución?
d) ¿Qué volumen se necesitará de esta disolución para preparar 0,5 L de ácido nítrico
0,2 M?
e) ¿Y para preparar 1 L de acido nítrico al 12% en peso, cuya densidad sería 1,069
g/mL?
17.- ¿Qué volumen de ácido fosfórico de densidad 1,45 g/mL y 62,8% de ácido fosfórico
(H3PO4 = 98 g/mol) es necesario para preparar 800 mL de disolución 0,40 M?
(Resp: 34,3 mL)
18.- ¿Qué cantidad de agua debe agregarse a 25 mL de una solución 0,5 M de KOH para
obtener una solución de concentración 0,35 M? (Resp: 10,7 mL se agua)
19.- ¿Cómo se prepararían 200 mL de una disolución 0,866 M de NaOH, a partir de una
disolución 5,07 M disponible en el almacén?
Ing. Víctor A. Campos Linares Período 2014-20
99
Apéndice 02
HOJA DE EJERCICIOS N° 11
UNIDAD VIII: EQUILIBRIO QUÍMICO
1.- Calcule el valor del pH, la concentración de iones [H+] y la concentración de iones
[OH-] de cada una de las siguientes soluciones de ácidos y bases fuertes:
a) HCl 0,001 M b) KOH 0,76 M c) HNO3 5,2x10-4 M d) Ba(OH)2 2,8x10-4 M
e) HNO3 0,125 M f) HClO4 2,1x 10-4 M
2.- Calcule las concentraciones de iones [H+] y de iones [OH-], en mol/L, para las
disoluciones con los siguientes valores de pH :
a) 2,42 b) 5,73 c) 6,96 d) 8,7 e) 11,2 f) 12,61
3.- ¿Cuál es el valor del pH en cada una de las soluciones?
a) 0,30 M HNO2 Ka = 4,5x10-4
b) 1 M HF Ka = 6,5x10-4
c) 0,15 M NH3 Kb = 1,8x10-5
d) 0,025 M HCN Ka = 4,0x10-10
4.- Calcule las concentraciones en el equilibrio de las diversas especies del ácido acético
0,2 M, CH3COOH para el cual Ka = 1,8x10 -5
5.- Calcule el porcentaje de ionización para el HCN 0,025 M, si Ka = 4,0x10 -10
6.- Calcule la ionización porcentual de una solución 0.10 M de ácido acético, si Ka =
1,8x10-5
(Rpta: % de ionización: 1,3 %)
7.- Se determina que el pH de una solución 0,115 M de ácido cloroacético, CH 2ClCOOH,
es 1,92. Calcule la constante de equilibrio. (Rpta: Ka: 1,398x10 -3 )
8.- Determine el valor de pH, [OH-], [H+] y pOH en una disolución acuosa de Ca(OH)2
cuya concentración es 80 mg / 850 mL de solución.
9.- Complete el siguiente cuadro realizando los cálculos necesarios:
Solución H3O+ OH- pH pOH
Solución A 5,2 x 10-5
Solución B 4,2
Solución C 4,8x10-6
Solución D 8,2
Ing. Víctor A. Campos Linares Período 2014-20
100
Apéndice 02
APÉNDICE 02
MASAS ATÓMICAS INTERNACIONALES (Escala basada en el Carbono – 12)
Elemento Símbolo Nº Atómico Masa
Aluminio Al 13 26,98
Antimonio Sb 51 121,75
Azufre S 16 32,06
Bario Ba 56 137,33
Berilio Be 4 9,01
Boro B 5 10,81
Bromo Br 35 80,00
Cadmio Cd 48 112,41
Calcio Ca 20 40,08
Carbono C 6 12,01
Cloro Cl 17 35,45
Cobre Cu 29 63,55
Cromo Cr 24 52,00
Fluor F 9 18,99
Fósforo P 15 30,97
Hidrógeno H 1 1,00
Hierro Fe 26 55,85
Litio Li 3 6,94
Magnesio Mg 12 24,31
Manganeso Mn 25 54,94
Mercurio Hg 80 200,95
Níquel Ni 28 58,69
Nitrógeno N 7 14,00
Oro Au 79 196,97
Oxígeno O 8 16,00
Plata Ag 47 107,87
Plomo Pb 82 207,20
Potasio K 19 39,09
Silicio Si 14 28,09
Sodio Na 11 22,99
Telurio Te 52 127,60
Titanio Ti 22 47,87
Yodo I 53 126,90
Ing. Víctor A. Campos Linares Período 2014-20
101
Apéndice 02
COMPARACIÓN DE LOS SISTEMAS DE MEDICIÓN: MÉTRICO, INGLÉS, SI
Magnitud Unidad Unidad SI Conversión de unidades
Física Métrica
1 m = 39,37 pulg = 1,09 yardas
1pulg = 0,025 m = 2,54 cm
Longitud Metro (m) Metro (m) 1 km = 0,6215 millas
1 yarda = 0,9144 m
1 milla = 1,609 km
1 pie = 0,3048 m
1g = 0,0353 onzas
1 kg = 2,205 lbs
1 Tn métrica = 1000 kg
Masa Gramo (g) Kilogramo ( kg) 1Tn métrica = 2205 lbs
1 onza = 28,35 g
1 lb = 453,6 g
1 arroba = 11,34 Kg
1 L = 1000 cm3 = 1000 mL
Volumen Litro (L) Metro cúbico (m3) 1 m3 = 1000 dm3 = 1000 L
1 pie3 = 28,32 L = 7,475 galones
1 pie3 = 0,0283 m3
1 atm = 1,013 bars
Presión Atmósfera Pascal (Pa) 1 atm = 760 mm Hg = 760 torr
1 atm = 29,92 pulg Hg
1 atm = 14,70 lb / pulg2
Temperatura Celcius Kelvin ºK = º C + 273,15
ºF = 1,8 (ºC) + 32
“Cuando vayas subiendo, saluda a todos. Son los mismos
que vas a encontrar cuando vayas bajando”.
Papa Francisco…
Ing. Víctor A. Campos Linares Período 2014-20
102
Referencias Bibliográficas
REFERENCIAS BIBLIOGRÁFICAS
a) Brown, T. L.; LeMay, H.E. Jr. & Bursten, B.E. Químíca. La Ciencia Central. 7ma. ed.
Prentice-Hall Hispanoamericana. S.A. México 1998.
b) Martínez Urreaga, Joaquín; Narros Sierra, Adolfo; Fuente García Soto, María.
Experimentación en Química General. International Thomson Editores Spain Paraninfo,
S. A. Madrid. 2006.
c) Chang, R. Química. Novena edición. McGraw-Hill. México. 2007.
d) Seese, W.S.; Daub. G. W. Química. 5ta. ed. Prentice-Hall Hispanoamericana. S.A.
México. 1989.
e) Whitten, K.W.; Gailev, K.D. & Davies, R.E. Química General. 3ra. ed. McGraw-Hill.
México. 1991.
f) Atkins, Peter; Jones, Loretta. Principios de Química: Los Caminos del Descubrimiento.
Editorial Médica Panamericana S. A. Buenos Aires. Tercera Edición. 2006.
g) Armas Ramírez, C.E.; Armas Romero, C.E. & Díaz Camacho, J. Ciencia Química.
Conceptos Fundamentales. 1ra. ed. Editorial Libertad EIRL. Trujillo (Perú). 1996.
Páginas Web:
Química General. http://cwx.prenhall.com/bookbind/pubbooks/blb_la/
PRÁCTICA:
a) Armas R.; Díaz C. Experimentos de Química. Primera edición. Editorial Libertad
EIRL. Trujillo. 1996.
b) Campos Linares V. A. Manual de Prácticas de Laboratorio de Química. Trujillo. 2013.
Ing. Víctor A. Campos Linares Período 2014-20
103
You might also like
- Mediciones y métodos de uso común en el laboratorio de QuímicaFrom EverandMediciones y métodos de uso común en el laboratorio de QuímicaRating: 4.5 out of 5 stars4.5/5 (3)
- Chorros Contra Incendios PDFDocument27 pagesChorros Contra Incendios PDFDORA HERNANDEZ100% (1)
- Taller de Flujo Multifasico-2008 - (v6) PDFDocument78 pagesTaller de Flujo Multifasico-2008 - (v6) PDFarmando0212-1100% (1)
- Explotación Del Petróleo y Optimización de La ProducciónDocument63 pagesExplotación Del Petróleo y Optimización de La ProducciónWilson Lobo Davila Z0% (1)
- Componentes Rectangulares de La Velocidad y de La AceleraciónDocument5 pagesComponentes Rectangulares de La Velocidad y de La AceleraciónSebastian Martinez Cuautenco100% (2)
- Tratamiento de Aguas para CalderasDocument104 pagesTratamiento de Aguas para CalderasGerardo Diaz100% (2)
- Grandes Obras Subterráneas. Diferentes Tuneles 2019Document152 pagesGrandes Obras Subterráneas. Diferentes Tuneles 2019Sergio Rodriguez RojasNo ratings yet
- Solucion 6-10 Practica2Document3 pagesSolucion 6-10 Practica2Esteban Távara HidalgoNo ratings yet
- Estructura AtomicaDocument6 pagesEstructura Atomicaelmer aguilar huaman100% (1)
- Practica 01 Grupo 3Document28 pagesPractica 01 Grupo 3Orson Rojas CáceresNo ratings yet
- Prueba de Hipotesis para La Diferencia de ProporcionesDocument3 pagesPrueba de Hipotesis para La Diferencia de ProporcionesSegundo Elvis Huanca FloresNo ratings yet
- Silabo de Fisica Aplicada A La Ingenieria Civil Fic-UnfvDocument9 pagesSilabo de Fisica Aplicada A La Ingenieria Civil Fic-UnfvFernando Torres VillegasNo ratings yet
- Informe Laboratorio Fisica Teoria de ErroresDocument8 pagesInforme Laboratorio Fisica Teoria de ErroresMaria Paula LuboNo ratings yet
- Curvas y EcuacionesDocument9 pagesCurvas y EcuacionesVictor BosNo ratings yet
- Contenidos CV 2017-B PDFDocument1 pageContenidos CV 2017-B PDFTefani TroyaNo ratings yet
- Tuanama G - 2 Monografia DiatereòmeroDocument11 pagesTuanama G - 2 Monografia DiatereòmeroRichard Antony Alva RuizNo ratings yet
- Protección de Circuitos EléctricosDocument26 pagesProtección de Circuitos EléctricosHarinhol MFNo ratings yet
- Informe de FuncionesDocument4 pagesInforme de FuncionesCarlos Rojas PinedaNo ratings yet
- CampoDocument10 pagesCampoLuis Alberto Huancollo CoaquiraNo ratings yet
- Lab - 1 Equilibrio de FuerzasDocument3 pagesLab - 1 Equilibrio de FuerzasCRISTEL ARIADNA LATORRE HURTADONo ratings yet
- Ingeniería Civil en El Siglo XXIDocument7 pagesIngeniería Civil en El Siglo XXILuis Loyola ArquerosNo ratings yet
- Ejercicios de EstadisticaDocument5 pagesEjercicios de Estadisticasaul M.cNo ratings yet
- Contenido de Humedad de La Arena y Porcentaje 2Document12 pagesContenido de Humedad de La Arena y Porcentaje 2Daniel HernandezNo ratings yet
- Practica 7 Quimica General PDFDocument3 pagesPractica 7 Quimica General PDFAlexis Diaz100% (1)
- TallerITM PDFDocument10 pagesTallerITM PDFEdwin García0% (1)
- 01-01 Recuperatorio de Tarea #1 de P y E 2020 - (B)Document1 page01-01 Recuperatorio de Tarea #1 de P y E 2020 - (B)Iván CarrizoNo ratings yet
- Ejemplode Plan de Tesis EPNDocument6 pagesEjemplode Plan de Tesis EPNMayraQuinteroNo ratings yet
- S1-PPT - Limite de Una FunciónDocument15 pagesS1-PPT - Limite de Una FunciónRolando0% (1)
- Copia de Lab 4 F - 1 Equilibrio de Fuerzas - Grupo 05Document7 pagesCopia de Lab 4 F - 1 Equilibrio de Fuerzas - Grupo 05AMELY JOELY RAMIREZ TELLONo ratings yet
- Ensayos en Sistemas de AlbañileriaDocument25 pagesEnsayos en Sistemas de AlbañileriaJose Daniel Galindo ObandoNo ratings yet
- Densidad y Peso Molecular Del AireDocument14 pagesDensidad y Peso Molecular Del AireChristopher David Alarcón AliagaNo ratings yet
- Ensayo. La Ing CivilDocument1 pageEnsayo. La Ing CivilEscribiendoAlaVida100% (1)
- Importancia de La Ingeniería Sísmica en El Diseño de EdificacionesDocument6 pagesImportancia de La Ingeniería Sísmica en El Diseño de EdificacionesAlexanderNo ratings yet
- JavierDocument5 pagesJavierStaelVillafaneRAmos50% (2)
- Mecanica de FluidosDocument4 pagesMecanica de FluidosyuriNo ratings yet
- Poster Resistencia MaterialesDocument1 pagePoster Resistencia Materialessaraxis isabel maestre zuñigaNo ratings yet
- INFORME DE LA PRACTICA EXPERIMENTAL Nro.4Document15 pagesINFORME DE LA PRACTICA EXPERIMENTAL Nro.4Teodocio VegaNo ratings yet
- Práctica de BioestadisticaDocument2 pagesPráctica de BioestadisticaKevin Rivera Barrueta100% (1)
- Fisica AnalisisU2Document11 pagesFisica AnalisisU2elizaNo ratings yet
- TEMA I Enlace QuimicoDocument12 pagesTEMA I Enlace QuimicoEmely YoveraNo ratings yet
- Taller Métodos Numéricos PDFDocument2 pagesTaller Métodos Numéricos PDFDavid LucasNo ratings yet
- Examen U2-A2Document3 pagesExamen U2-A2Jean Piere Garcia FloresNo ratings yet
- Taller2 UPTCDocument3 pagesTaller2 UPTCCamilo Alv CepedaNo ratings yet
- FISICA II Segundo Trabajo LaboratorioDocument23 pagesFISICA II Segundo Trabajo LaboratorioCLINTON AYALA HUAMANNo ratings yet
- Trabajo de Qo-7Document20 pagesTrabajo de Qo-7JuanMC100% (1)
- Introducción A La Química Aplicada A La Ingeniería Civil y Sistema Internacional de Unidades (WORD)Document14 pagesIntroducción A La Química Aplicada A La Ingeniería Civil y Sistema Internacional de Unidades (WORD)aleven quispeNo ratings yet
- Electrostatica 2 PreinformeDocument8 pagesElectrostatica 2 PreinformeANGYE15No ratings yet
- Experimento N°4 Efecto Doppler (Virtual)Document3 pagesExperimento N°4 Efecto Doppler (Virtual)ivelliseNo ratings yet
- Examen Parcial-Introduccion A La ComputacionDocument2 pagesExamen Parcial-Introduccion A La ComputacionronaldpjNo ratings yet
- Proceso de Gram Schmidt Clase Del 24 de OctubreDocument4 pagesProceso de Gram Schmidt Clase Del 24 de Octubrecarlos HernandezNo ratings yet
- Introducción A La PsicologíaDocument1 pageIntroducción A La PsicologíaAna Delia Bernardino CruzNo ratings yet
- Monografia de Etica y SociedadDocument21 pagesMonografia de Etica y SociedadJimmythoChahuaPomayayNo ratings yet
- EDO AplicacionesDocument8 pagesEDO AplicacionesJorge Arias AcevedoNo ratings yet
- Matrices Semejantes y Diagonalizacion PDFDocument22 pagesMatrices Semejantes y Diagonalizacion PDFjunior huincho macoteNo ratings yet
- Practica 3 Quimica IIDocument3 pagesPractica 3 Quimica IILFNo ratings yet
- MocoaDocument35 pagesMocoaJuan CuasqueNo ratings yet
- La Importancia de La Química en La Ingeniería CivilDocument3 pagesLa Importancia de La Química en La Ingeniería CivilDEIVI RAMIREZNo ratings yet
- Módulos 1Document4 pagesMódulos 1fvd71No ratings yet
- Evaluacion EstequiometríaDocument3 pagesEvaluacion EstequiometríaMaria Ines Astudillo ParraNo ratings yet
- Ejercicios, FricciónDocument2 pagesEjercicios, FricciónElizabethDelgadoNazarioNo ratings yet
- Informe Acidos OrganicosDocument10 pagesInforme Acidos OrganicosCAMILLA YAMILETH NIMA ENCALADANo ratings yet
- Trabajo Grupal - Libro Zamora PDFDocument59 pagesTrabajo Grupal - Libro Zamora PDFCristhian BustamanteNo ratings yet
- Manual de Quimica General Final Julio 2010 (2)Document148 pagesManual de Quimica General Final Julio 2010 (2)Daniela CasanovaNo ratings yet
- Manual de Quimica General Final Julio 2010Document153 pagesManual de Quimica General Final Julio 2010alejandraamartinezqNo ratings yet
- Manual de Electronica - Upao 2022Document90 pagesManual de Electronica - Upao 2022Jose Antonio Gonzales GuzmanNo ratings yet
- Manual de Prácticas de Laboratorio - Química General: SEMESTRE 2019-20Document66 pagesManual de Prácticas de Laboratorio - Química General: SEMESTRE 2019-20HansNo ratings yet
- Dicroismo Circular s2018Document8 pagesDicroismo Circular s2018Ariel Pinto MarchantNo ratings yet
- BombasDocument16 pagesBombasD IsaacNo ratings yet
- Practica 4 Efecto FotoelectricoDocument5 pagesPractica 4 Efecto FotoelectricoCesar CastillogonzalezNo ratings yet
- Práctica Claisen - SchmidtDocument2 pagesPráctica Claisen - SchmidtMayra HerreraNo ratings yet
- Philips Lighting BBS460 W30L120 1xLED24/830 MLO-PC 1xLED24/830Document3 pagesPhilips Lighting BBS460 W30L120 1xLED24/830 MLO-PC 1xLED24/830Alex Sinailin CtNo ratings yet
- Clasificacion Hotelera 2012Document41 pagesClasificacion Hotelera 2012Yesenia Saraí Perez CasanovaNo ratings yet
- Guía para La Prevención de Explosiones de Polvo de Carbón en Minería Subterránea y Limitación de Sus ConsecuenciasDocument139 pagesGuía para La Prevención de Explosiones de Polvo de Carbón en Minería Subterránea y Limitación de Sus ConsecuenciasAnonymous Kvm4KxY4No ratings yet
- INDUCCIONDocument4 pagesINDUCCIONCristian HerreraNo ratings yet
- 30leroy Somer Manual Mant07 - EsDocument24 pages30leroy Somer Manual Mant07 - Esonyx_lucianoNo ratings yet
- Arbol de Causa Efecto y de Medios y Fines - Proyecto de InvestigacionDocument4 pagesArbol de Causa Efecto y de Medios y Fines - Proyecto de InvestigacionRoberth Erasmo Chavez GallegosNo ratings yet
- Instalación de Motores Eléctricos TrifásicosDocument12 pagesInstalación de Motores Eléctricos TrifásicosLeonardo BarabasNo ratings yet
- Manual Pulverizadoras CarretillaDocument24 pagesManual Pulverizadoras CarretillaIsabel Andrea Vidal JimenezNo ratings yet
- Informe de Práctica #2 Sensor de Luz y Oscuridad Con ReleDocument5 pagesInforme de Práctica #2 Sensor de Luz y Oscuridad Con ReleJonathan EspinNo ratings yet
- Memoria de Calculo Contra Incendio BodegaDocument7 pagesMemoria de Calculo Contra Incendio BodegasoremhalNo ratings yet
- Apuntes de Residuos Solidos UrbanosDocument26 pagesApuntes de Residuos Solidos UrbanosElena Collazos GonzálezNo ratings yet
- Flujo InternoDocument28 pagesFlujo InternoalexNo ratings yet
- Método de BakhmeteffDocument21 pagesMétodo de BakhmeteffSantiago Samaniego Eguiguren100% (1)
- Sistemas de Alarmas.Document34 pagesSistemas de Alarmas.Rodrigo Andres Vallejo CastroNo ratings yet
- Ordenanza 044-97 Codigo de Prevencion Proteccion y Lucha Contra El FuegoDocument44 pagesOrdenanza 044-97 Codigo de Prevencion Proteccion y Lucha Contra El FuegohysgroupNo ratings yet
- Plataformas Articuladas Autopropulsadas: Z - 60/37DC & Z - 60/37FEDocument2 pagesPlataformas Articuladas Autopropulsadas: Z - 60/37DC & Z - 60/37FEJose MelgarNo ratings yet
- Bloque 4 DocumentalDocument38 pagesBloque 4 DocumentalDiego Gpe Ac AcNo ratings yet
- Fisica Mecanica ProblemasDocument4 pagesFisica Mecanica ProblemasgabrielNo ratings yet
- G1. Actividad Sobre Fundamentos de Electricidad 1Document7 pagesG1. Actividad Sobre Fundamentos de Electricidad 1Miguel Angel PerezNo ratings yet
- BiogasDocument5 pagesBiogasOscar Céspedes MalcaNo ratings yet