Professional Documents
Culture Documents
Experiencia N°2 - LABO 3 INO
Uploaded by
Alfredo IvanOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Experiencia N°2 - LABO 3 INO
Uploaded by
Alfredo IvanCopyright:
Available Formats
Experiencia N°2:
a) Observaciones experimentales:
Cuando realizamos la experiencia con mis compañeros de grupo de laboratorio, nos
percatamos que al momento de mezclar las 2 soluciones de NaOH y HCl en el
calorímetro preparado respectivamente con algunos de los instrumentos dados, el
color y la consistencia final no variaba a la vista normal, parecía como si fueran las
mismas soluciones.
La temperatura que variaba en cada mezcla sucesivamente era algo mínimo, casi
siempre tendía a 20°C, y la prof. de laboratorio presente nos dio la razón y nos dijo que
sería de 20°C, por lo cual si hubieran porcentajes de error, pues sería lo mínimo.
b) Diagrama de flujo:
(Deja 1 hoja para esto y mañana lo archivamos)
c) Ecuaciones Químicas:
La ecuación química que se usó en la experiencia actual fue:
NaOH(ac) + HCl(ac) -> NaCl(ac) + H2O(l) + calor
d) Cálculos y resultados:
Lo hallaremos por el Método de la Variaciones Continuas (MVC) o método de JOB.
La temperatura final aprox. en la cual ambas soluciones se mezclaban era: 20°C
Mezcla n° NaOH 0.8M HCl 0.2M Temperatura final (°C) Variación de temperatura (°C)
1 5 ml 45 ml 20 0
2 10 ml 40 ml 20.5 0.5
3 21 ml 29 ml 21 1
4 29 ml 21 ml 20.5 0.5
5 33 ml 17 ml 20 0
6 39 ml 11 ml 19.8 0.2
7 41 ml 9 ml 20 0
8 45 ml 5 ml 19.8 0.2
Mezcla n° XNaOH XHCl Reactivo Limitante Reactivo en Exceso
1 0.1 0.9 NaOH HCl
2 0.2 0.8 NaOH HCl
3 0.42 0.58 NaOH HCl
4 0.58 0.42 HCl NaOH
5 0.66 0.34 HCl NaOH
6 0.78 0.22 HCl NaOH
7 0.82 0.18 HCl NaOH
8 0.9 0.1 HCl NaOH
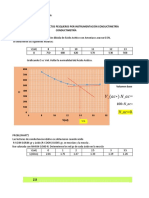
(Deja 1 hoja para archivar la hoja milimetrada con el gráfico y sus ecuaciones y el
punto y mañana lo juntamos)
1.2
0.8
Variación de T
0.6
y = 1.1404x + 0.1294
y = -1.7513x + 1.5309
0.4
0.2
0
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1
-0.2
XA
El punto estequiometrico igualando ambas ecuaciones es XA=0.48 y variación T=0.68
e) Explicación e interpretación de resultados:
Para desarrollar los cálculos teníamos que tener en cuenta que en la ecuación química
la proporción de ambas soluciones estaban de 1 a 1, por lo que hallamos la XA, y por
último las variaciones de temperatura que son pequeñas en la mayoría de casos.
Al tener ambas ecuaciones de las rectas, entonces podremos hallar dicho punto
estequiométrico igualando las 2 ecuaciones.
f) Observaciones finales:
Como vemos, en nuestro gráfico, nos salió una forma de “V” invertida, y por lo general
nos debería salir una “V” invertida, en lo que podemos apreciar que no hubo mucho
error experimental.
g) Comentarios y/o apreciaciones:
Para que nos pueda salir un gráfico bien, en cuanto a la parte experimental,
deberemos tomar en cuenta muchas cosas, ya sea en el tiempo en el cual haremos la
mezcla de ambas soluciones, tener en cuenta también el tiempo en el que estemos
haciendo esperar ambas soluciones antes de hacer dicha mezcla, etc.
h) Conclusiones:
El método que hemos usado, que es el MVC o JOB, nos muestra y ofrece resultados
muy precisos.
You might also like
- Matriz de Evaluación de RiesgosDocument1 pageMatriz de Evaluación de RiesgosAlfredo IvanNo ratings yet
- Curva de TitulacionDocument2 pagesCurva de TitulacionJONATHAN CASTILLEJOS LARANo ratings yet
- Práctica 10 QG2Document5 pagesPráctica 10 QG2Daniel MeloNo ratings yet
- Articulo de Coeficientes de ActividadDocument5 pagesArticulo de Coeficientes de ActividadYuriko BoringNo ratings yet
- Reporte No 1 - Constante Cinética y Orden de Reacción en Un Reactor BatchDocument23 pagesReporte No 1 - Constante Cinética y Orden de Reacción en Un Reactor BatchJimena AlvaradoNo ratings yet
- En BUsca Del KlingsorDocument20 pagesEn BUsca Del KlingsorCesar Augusto Acevedo RamirezNo ratings yet
- Informe Practica 10Document7 pagesInforme Practica 10Roberto SánchezNo ratings yet
- Metodo de Eficiencia de JOBDocument5 pagesMetodo de Eficiencia de JOBJULIANA MARTINEZNo ratings yet
- 2015 CineticaDocument18 pages2015 CineticaAnonymous JUZFQ6GAoNo ratings yet
- Reporte p5 - Lab Qa1 - JCHC - JDRRDocument8 pagesReporte p5 - Lab Qa1 - JCHC - JDRRDaniel RodriguezNo ratings yet
- Practica Nro 5 InstrumentalDocument5 pagesPractica Nro 5 InstrumentalAlvaro CalderonNo ratings yet
- Cinetica QuimicaDocument18 pagesCinetica QuimicajuanNo ratings yet
- Ingeniería Quimica: Química AnalíticaDocument12 pagesIngeniería Quimica: Química Analíticaangel gabrielNo ratings yet
- Examfinqmc1206 22021 OficialDocument7 pagesExamfinqmc1206 22021 OficialDANNER ARANIBARNo ratings yet
- Copia de Calculos Del Laboratorio de Quimica 2Document9 pagesCopia de Calculos Del Laboratorio de Quimica 2Rox ClienteNo ratings yet
- Cinética de La Saponificación Del Acetato de Etilo en Medio BásicoDocument4 pagesCinética de La Saponificación Del Acetato de Etilo en Medio BásicoDaniel Marcelo VelasquezNo ratings yet
- Informe de Determinacion de La Constante de AcidezDocument8 pagesInforme de Determinacion de La Constante de AcidezNadia AuzsaNo ratings yet
- Practica10 Lab31Document8 pagesPractica10 Lab31Dany BuendiaNo ratings yet
- Remedial QuimicaDocument11 pagesRemedial QuimicaYimi Salcedo AvilaNo ratings yet
- Informe de Laboratorio - P6. Método de JobDocument9 pagesInforme de Laboratorio - P6. Método de JobLuisa FernandaNo ratings yet
- Potenciometría-Y-Titulación-Ácido Practica 2Document5 pagesPotenciometría-Y-Titulación-Ácido Practica 2carlosNo ratings yet
- Diagrame Los Resultados de Las Ganancias y Pérdidas de Peso Usando La Ecuación de Vant HoffDocument3 pagesDiagrame Los Resultados de Las Ganancias y Pérdidas de Peso Usando La Ecuación de Vant HoffSaraMartinesNo ratings yet
- Lab - QG II Repor Práctica 3Document4 pagesLab - QG II Repor Práctica 3Ezequiel MedinaNo ratings yet
- R - Curvas de TitulaciónDocument5 pagesR - Curvas de TitulaciónDaniel Santana ReynaNo ratings yet
- Tablas P4 BQDocument1 pageTablas P4 BQFernanda CabreraNo ratings yet
- Práctica 12. Coeficiente de Difusión Efectivo en Un GelDocument10 pagesPráctica 12. Coeficiente de Difusión Efectivo en Un GelItzel Daniela Solis TinocoNo ratings yet
- Calcule La Concentración Del Persulfato de PotasioDocument2 pagesCalcule La Concentración Del Persulfato de PotasioubaldoNo ratings yet
- Problema 1Document11 pagesProblema 1Jonathan Vargas100% (1)
- Práctica 3. Eq. Ác-Base PDFDocument13 pagesPráctica 3. Eq. Ác-Base PDFJennifer GuadarramaNo ratings yet
- Práctica II Equilibrio HeterogeneoDocument10 pagesPráctica II Equilibrio HeterogeneoMarcela MoralesNo ratings yet
- Informe Valoracion Potenciometrica Acido-BaseDocument16 pagesInforme Valoracion Potenciometrica Acido-BasePaola Valverde100% (1)
- Informe Práctica 8Document11 pagesInforme Práctica 8VALENTINA LOPEZ LOPEZNo ratings yet
- Rerporte Practica1q4Document15 pagesRerporte Practica1q4Daniel Josue Hernandez SalazarNo ratings yet
- Acido Base IiDocument13 pagesAcido Base IiZamira RiveraNo ratings yet
- Práctica 8. Informe.Document4 pagesPráctica 8. Informe.Janet QuirozNo ratings yet
- Informe Método de JobDocument4 pagesInforme Método de JobYojan HenaoNo ratings yet
- Cálculos de ConductividadDocument4 pagesCálculos de ConductividadRONDAN LOPEZ ELIAN PIERONo ratings yet
- Refraccion - MeyDocument8 pagesRefraccion - MeyJose murciaNo ratings yet
- Guia Problemas Qac 2018Document24 pagesGuia Problemas Qac 2018Teresa MuchaNo ratings yet
- Informe Experimento #13 Equilibrio de Tres ComponentesDocument6 pagesInforme Experimento #13 Equilibrio de Tres ComponentesferiteNo ratings yet
- Parcial #1.Document7 pagesParcial #1.Deivis GutierrezNo ratings yet
- CALORDocument15 pagesCALORMariela CoyoNo ratings yet
- Practica 8 BrisaDocument10 pagesPractica 8 BrisaBRISA ESTEFANIA HERNANDEZ CARRILLONo ratings yet
- Cuantitativa 5Document11 pagesCuantitativa 5Jean Pierre Cirilo SosaNo ratings yet
- Informe 7 - AnaliticaDocument18 pagesInforme 7 - AnaliticaTeffy LokitaNo ratings yet
- Practica #08 Acidos y Bases en VolumetriaDocument4 pagesPractica #08 Acidos y Bases en VolumetriamiguelringoNo ratings yet
- Trabajo Final de Cáculo IIDocument22 pagesTrabajo Final de Cáculo IILuis CoaquiraNo ratings yet
- Reporte No 2 - Constante Cinética y Orden de Reacción en Un Reactor Batch A Distinta TemperaturaDocument23 pagesReporte No 2 - Constante Cinética y Orden de Reacción en Un Reactor Batch A Distinta TemperaturaJimena AlvaradoNo ratings yet
- Diagrama de FaseDocument9 pagesDiagrama de FaseJaider DeulufeutNo ratings yet
- Resultados - Pract4 - 1Document7 pagesResultados - Pract4 - 1Chris QCNo ratings yet
- Reporte 8 Coeficiente de Distribucion FiDocument5 pagesReporte 8 Coeficiente de Distribucion FiJhonny MaraviNo ratings yet
- Preg 4 AnalDocument3 pagesPreg 4 AnalJULIUS JELIUSNo ratings yet
- PRACTICA 3 FenomrnosDocument14 pagesPRACTICA 3 FenomrnosZuñiga Vazquez LeonardoNo ratings yet
- Inf. Nro 2-2019 - Res-Cues.Document9 pagesInf. Nro 2-2019 - Res-Cues.Aylin JudithNo ratings yet
- R. 6 GiiDocument6 pagesR. 6 GiiGab OCNo ratings yet
- Práctica N 6Document3 pagesPráctica N 6Ja VikiõNo ratings yet
- Practica Volumen Molar ParcialDocument6 pagesPractica Volumen Molar Parcialdiego fernandezNo ratings yet
- Informe 5Document12 pagesInforme 5Brandon RodriguezNo ratings yet
- Anlisis Intrumental Tare 11 ConducDocument14 pagesAnlisis Intrumental Tare 11 ConducAndrea del AguilaNo ratings yet
- L4 Mezcla Acetona - Cloroformo Con Tablas y GraficasDocument10 pagesL4 Mezcla Acetona - Cloroformo Con Tablas y GraficasMinerva AguilarNo ratings yet
- Reactor Químico. Gonzalez Garcia Diana ItzelDocument7 pagesReactor Químico. Gonzalez Garcia Diana ItzelHorus CastilloNo ratings yet
- Informe Lab #1 Agitación - Grupo FDocument43 pagesInforme Lab #1 Agitación - Grupo FAlfredo IvanNo ratings yet
- Tarea Problema Agitacion B EDocument2 pagesTarea Problema Agitacion B EAlfredo IvanNo ratings yet
- Taller Práctico 2 PS PI555A Grupo XXDocument1 pageTaller Práctico 2 PS PI555A Grupo XXAlfredo IvanNo ratings yet
- SocratesDocument4 pagesSocratesAlfredo IvanNo ratings yet
- Estoicismo Listo Pa EntregarDocument21 pagesEstoicismo Listo Pa EntregarAlfredo IvanNo ratings yet
- Sem 7 - Creacion y Aniquilacion de ParesDocument11 pagesSem 7 - Creacion y Aniquilacion de ParesAlfredo IvanNo ratings yet
- 1.2 Características de Los Cables EléctricosDocument3 pages1.2 Características de Los Cables EléctricosEd ColinsNo ratings yet
- 3ER AÑO-fisico QuimicaDocument36 pages3ER AÑO-fisico QuimicaNoeliaSanzNo ratings yet
- Informe Fisica MCUDocument3 pagesInforme Fisica MCUDavid CarabaliNo ratings yet
- Unidad 3 CalculoDocument8 pagesUnidad 3 CalculoJuan TorresNo ratings yet
- 5 Ley de OhmDocument5 pages5 Ley de OhmPaula Yurany Romero RojasNo ratings yet
- Emisiones AcusticasDocument3 pagesEmisiones AcusticasJaasiel MartinNo ratings yet
- Propiedades de La Materia y Su ClasificacionDocument4 pagesPropiedades de La Materia y Su ClasificacionPeter CacheNo ratings yet
- Tesla Fisica PDFDocument30 pagesTesla Fisica PDFJuan GonzalesNo ratings yet
- 2019 1 Ah b09 2 06 03 Emf137 Mecanica de FluidosDocument5 pages2019 1 Ah b09 2 06 03 Emf137 Mecanica de FluidosJhonn Salas LirioNo ratings yet
- Ejemplo 9.10docxDocument10 pagesEjemplo 9.10docxManuel CFNo ratings yet
- Unidad 1 Conceptos Básicos Con Excel y MATLABDocument29 pagesUnidad 1 Conceptos Básicos Con Excel y MATLABJavier ArmentaNo ratings yet
- Procesos TermodinamicosDocument13 pagesProcesos TermodinamicosJoan Montenegro FernándezNo ratings yet
- Guías Electricidad-MagnetismoDocument11 pagesGuías Electricidad-MagnetismoDoloresNo ratings yet
- Diseño de Secador de Tambor Rotatorio Con Recirculación en MathcadDocument5 pagesDiseño de Secador de Tambor Rotatorio Con Recirculación en MathcadMirko Párraga IrustaNo ratings yet
- Post1 Termo2Document9 pagesPost1 Termo2Valeria AlpucheNo ratings yet
- Ejerciciosos ElectriDocument8 pagesEjerciciosos ElectriJuan David OsorioNo ratings yet
- C. Naturales - Fisica I - 11-16-CDocument2 pagesC. Naturales - Fisica I - 11-16-CalbaNo ratings yet
- Práctica RADIACTIVIDADDocument2 pagesPráctica RADIACTIVIDADAlex RodriguezNo ratings yet
- Subestaciones, Ing. Luis TapiaDocument141 pagesSubestaciones, Ing. Luis TapiaWilliamFernando100% (3)
- Fisica II 3er ParcialDocument51 pagesFisica II 3er ParcialJuan GarciaNo ratings yet
- Ampere y Faraday y GeneradoresDocument6 pagesAmpere y Faraday y GeneradoresJose CastañedaNo ratings yet
- DGDC - Fisilab - Bobina de TeslaDocument9 pagesDGDC - Fisilab - Bobina de TeslaFrancisCo MarcanoNo ratings yet
- Informe de Laboratorio Fisica 2Document5 pagesInforme de Laboratorio Fisica 2Kevin Andrés NincoNo ratings yet
- 1.-Enganchar - Física ContemporaneaDocument4 pages1.-Enganchar - Física ContemporaneaAlejandra AlvarezNo ratings yet
- Preinforme Punto de Burbuja 1Document7 pagesPreinforme Punto de Burbuja 1Magaly PinzónNo ratings yet
- Teoria de Suma y Resta de VectoresDocument11 pagesTeoria de Suma y Resta de VectoresMariela Morato0% (1)
- Estabilidad y Determinacion PDFDocument16 pagesEstabilidad y Determinacion PDFbrayan aguilar miguelNo ratings yet
- 11 Fuerzas y Aceleraciones CRDocument10 pages11 Fuerzas y Aceleraciones CRCarlos QuispeNo ratings yet
- Hibridación Del Carbono SP, SP2, SP3Document5 pagesHibridación Del Carbono SP, SP2, SP3Blanca Bohorquez100% (1)