Professional Documents
Culture Documents
Uniones Quimicas, Resumen
Uploaded by
Alexis LartirigoyenOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Uniones Quimicas, Resumen
Uploaded by
Alexis LartirigoyenCopyright:
Available Formats
Sobre la base de su configuración electrónica, los elementos químicos se pueden clasificar en
cuatro grupos:
a) Gases nobles: presentan su órbita electrónica externa completa con ocho electrones, con
excepción del He, que tiene dos electrones. En ellos, la estructura electrónica externa es s2 p6,
salvo en el He, que es s2 por tener un solo nivel de energía. Ocupan el grupo 18 de la Tabla
Periódica.
b) Elementos representativos: son aquellos que tienen su órbita externa incompleta. El
electrón diferencial se encuentra en los subniveles s o p. Comprende a los elementos que
ocupan los grupos 1, 2, 13, 14, 15, 16 y 17 de la Tabla Periódica.
c) Elementos de transición: se caracterizan por presentar sus dos últimas órbitas incompletas.
El electrón diferencial se ubica en los subniveles d. Esto significa que el electrón que se agrega
lo hace en su anteúltima órbita. Corresponden a esta clase los elementos de los grupos 3, 4, 5,
6, 7, 8, 9, 10, 11 y 12 de la Tabla Periódica.
d) Elementos de transición interna: son los que presentan sus tres últimas órbitas
incompletas. El electrón diferencial se halla en el subnivel f, es decir, que se incorpora a la
antepenúltima órbita. Constituyen las denominadas tierras raras (lantánidos y actínidos)
ubicadas generalmente al pie de la Tabla
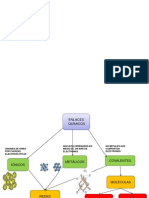
Uniones químicas.
Unión iónica: ocurre entre átomos cuya diferencia de electronegatividad es elevada (mayor a
2), habiendo una trasferencia completa de electrones formándose cationes o aniones.
Sus enlaces son muy fuertes
Sólidos a temperatura ambiente y poseen una estructura cristalina o transparente
Altos punto de fusión y ebullición
Son enlaces resultantes de la interacción entre los metales de los grupos I y II y los no
metales de los grupos VI y VII.
Unión covalente: En este tipo de unión los no metales se unen con los no metales. Se da entre
los átomos con poca o nula diferencia de electronegatividad y a diferencia de las uniones
iónicas no se forman iones. En esta unión los electrones se comparten, de manera que no
ceden ni captan.
Presentan bajos puntos de fusión y ebullición
Son insolubles en solventes polares como el agua y el alcohol
No forman iones
Covalente simple: unión en la que el electrón es aportado por ambos átomos
Covalente dativa: unión en la que el electrón solo es aportado por uno de los átomos
Las uniones metálicas: Los metales reciben o ganan electrones para alcanzar la estabilidad.
Estas partículas negativas se encuentran en constante movimiento, razón por la cual la
mayoría de los metales, en estado sólido a temperatura ambiente, son buenos conductores de
la electricidad. Los dos iones se mantienen fuertemente unidos.
You might also like
- Ft. Acido Extra Fuerte - KazDocument3 pagesFt. Acido Extra Fuerte - KazCristhiam Montalvan Coronel100% (2)
- Cuadro Comparativo de Propiedades de Los Enlaces QuimicosDocument2 pagesCuadro Comparativo de Propiedades de Los Enlaces QuimicosCeledonio Hernandez Sanchez79% (77)
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaFrom EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaRating: 5 out of 5 stars5/5 (1)
- Enlaces QuimicosDocument7 pagesEnlaces QuimicosArnol RodriguezNo ratings yet
- Enlaces QuimicosDocument17 pagesEnlaces Quimicosluisal88No ratings yet
- Guia de Enlaces Quimicos 9Document6 pagesGuia de Enlaces Quimicos 9rubielacardenas60% (5)
- Enlaces QuímicosDocument17 pagesEnlaces Químicosdabe-quimico100% (1)
- Tabla Periodica y EnlacesDocument8 pagesTabla Periodica y EnlacesLaura Cecilia Hernandez DelgadoNo ratings yet
- Concepto de Enlace QuímicoDocument4 pagesConcepto de Enlace QuímicoCarlos Emilio Castillo GuzmanNo ratings yet
- Química 4º 1er TrimDocument9 pagesQuímica 4º 1er TrimvivianaborgetoNo ratings yet
- Enlaces Químicos TeoriaDocument4 pagesEnlaces Químicos TeoriaFabNo ratings yet
- Enlaces QuimicosDocument5 pagesEnlaces QuimicosOscar Hernandez SalinasNo ratings yet
- Enlaces QuímicosDocument15 pagesEnlaces QuímicosAsc phoimpNo ratings yet
- DipolarDocument11 pagesDipolarLaura PaolaNo ratings yet
- Enlace QuímicosDocument4 pagesEnlace QuímicosYabil LopezNo ratings yet
- Enlaces Atómicos: Química Tercero 2020Document24 pagesEnlaces Atómicos: Química Tercero 2020logokillaNo ratings yet
- Enlace QuimicoDocument22 pagesEnlace QuimicoDina luzNo ratings yet
- Hibrid TomDocument77 pagesHibrid TomAlessandra RamosNo ratings yet
- Los Enlaces QuímicosDocument15 pagesLos Enlaces QuímicosLizbeth Moreno MantillaNo ratings yet
- Guia de Ejercicios LewisDocument8 pagesGuia de Ejercicios LewisValeria ApablazaNo ratings yet
- 03 - Enlace QuímicoDocument29 pages03 - Enlace QuímicoardansvalenNo ratings yet
- Que Es Un Enlace SencilloDocument16 pagesQue Es Un Enlace SencilloAnonymous RhRhpeiIR0% (4)
- Apuntes y Problemas Tema 2. Sistema PeriódicoDocument9 pagesApuntes y Problemas Tema 2. Sistema PeriódicoMarcos Guerra HernándezNo ratings yet
- Documento Sin TítuloDocument2 pagesDocumento Sin TítuloKenzo López KobayashiNo ratings yet
- Plan de Química 2º Curso-Ciencias Básicas - Plan ComúnDocument8 pagesPlan de Química 2º Curso-Ciencias Básicas - Plan Comúnsofiadelvalle709No ratings yet
- Enlaces QuimicosDocument10 pagesEnlaces QuimicosJoaquin MartinNo ratings yet
- Actividades de Cuadernillo Química IDocument4 pagesActividades de Cuadernillo Química IGabriela RuizNo ratings yet
- H-18. Ubicacion Periodica de Acuerdo Al Electron Dif.Document3 pagesH-18. Ubicacion Periodica de Acuerdo Al Electron Dif.ALANNo ratings yet
- Propiedades Físicas de Compuestos Iónicos y CovalentesDocument8 pagesPropiedades Físicas de Compuestos Iónicos y Covalentesfabis50% (2)
- Trabajo de Quimica.Document5 pagesTrabajo de Quimica.Anthony LomasNo ratings yet
- Tema 2: Elementos y Compuestos: I. Los Elementos: La Tabla PeriodicaDocument6 pagesTema 2: Elementos y Compuestos: I. Los Elementos: La Tabla PeriodicaJavier Ruiz PerezNo ratings yet
- Biología UNLAM Módulo 3.1Document10 pagesBiología UNLAM Módulo 3.1Rebeca LeónNo ratings yet
- Enlaces QuimicosDocument133 pagesEnlaces QuimicosLauraGarellaNo ratings yet
- 3c Uniones Quimicas IEMDocument54 pages3c Uniones Quimicas IEMmartinutniemNo ratings yet
- El Enlace Químico: ObjetivosDocument12 pagesEl Enlace Químico: ObjetivosMiranda MorenoNo ratings yet
- Parte 13 TEORÍA DE LEWISDocument46 pagesParte 13 TEORÍA DE LEWISErik Ariel LauraNo ratings yet
- Cuestionario 1 CementoDocument3 pagesCuestionario 1 CementoMaria Cristina CuracachiNo ratings yet
- LMyT EvA 3Document9 pagesLMyT EvA 3gera zuñigaNo ratings yet
- Resumen Quimica Primer BloqueDocument21 pagesResumen Quimica Primer BloqueFrancescaNo ratings yet
- Tom y Tev Complemento de LewisDocument217 pagesTom y Tev Complemento de LewisAde RendónNo ratings yet
- Clasificacion de Los Enlaces QuimicosDocument11 pagesClasificacion de Los Enlaces Quimicosblue studioNo ratings yet
- Enlace QuímicoDocument34 pagesEnlace QuímicoMaría José OyolaNo ratings yet
- Clase 4.1 QuimicaDocument10 pagesClase 4.1 QuimicaEugenioNo ratings yet
- Enlaces IntramolecularesDocument2 pagesEnlaces IntramolecularesMartNo ratings yet
- Trabajo de Enlace QuimicoDocument10 pagesTrabajo de Enlace QuimicoFausto Champi ChecyaNo ratings yet
- Configuración Electrónica y Enlaces QuímicosDocument4 pagesConfiguración Electrónica y Enlaces QuímicosSandra MartinezNo ratings yet
- El Enlace QuímicoDocument11 pagesEl Enlace QuímicoThiffany Sherlyn OrtizNo ratings yet
- Apuntes Ud2 Configuración Electrónica y Enlace QuímicoDocument9 pagesApuntes Ud2 Configuración Electrónica y Enlace Químicoexplorers2No ratings yet
- Enlace QuimicoDocument14 pagesEnlace Quimicojhordan bravoNo ratings yet
- Tema 3 Enlace Químico, Quimica General UDO PDFDocument15 pagesTema 3 Enlace Químico, Quimica General UDO PDFArioc ParicaNo ratings yet
- Enlaces Iónico o ElectrovalenteDocument2 pagesEnlaces Iónico o ElectrovalenteHugo Saritama ChérrezNo ratings yet
- Apuntes FyQ 3 Eso Tema 3Document5 pagesApuntes FyQ 3 Eso Tema 3AL3J4NDR0No ratings yet
- Apunte Anlace QuimicoDocument2 pagesApunte Anlace QuimicoSantiago PeñalozaNo ratings yet
- Unidad IIIDocument8 pagesUnidad IIIRonanNo ratings yet
- Enlaces QuímicosDocument26 pagesEnlaces Químicoserick tixiNo ratings yet
- Unidad 1.1 Naturaleza de Los MaterialesDocument12 pagesUnidad 1.1 Naturaleza de Los MaterialesAlvaro Vera0% (1)
- Moléculas y Formulas QuímicasDocument20 pagesMoléculas y Formulas QuímicasDanielaNo ratings yet
- Enlace QuímicoDocument10 pagesEnlace Químicoangel inocencio perezNo ratings yet
- Enlace QuimicoDocument35 pagesEnlace QuimicodavidalvarezbenavideNo ratings yet
- 3529-QT-01 Enlaces Atómicos 7%Document24 pages3529-QT-01 Enlaces Atómicos 7%RodrigoNo ratings yet
- Comunicación Conjunta 8-21 - Utilización de Listados 2021Document2 pagesComunicación Conjunta 8-21 - Utilización de Listados 2021FM Reflejos Sierra de la VentanaNo ratings yet
- DID Salinas Fernandez Unidad 2Document18 pagesDID Salinas Fernandez Unidad 2mgb9815No ratings yet
- Prestaciones Basicas UniversalesDocument2 pagesPrestaciones Basicas UniversalesFrancisco Iurcovich100% (3)
- Entrega de Proyectos y ProgramasDocument1 pageEntrega de Proyectos y ProgramasAlexis LartirigoyenNo ratings yet
- Planilla Informe Trayectorias Turno Tarde-V.2Document1 pagePlanilla Informe Trayectorias Turno Tarde-V.2Alexis LartirigoyenNo ratings yet
- ProspDocument1 pageProspAlexis LartirigoyenNo ratings yet
- Curso de EcuacionesDocument1 pageCurso de EcuacionesAlexis LartirigoyenNo ratings yet
- 1 Hidrostática 13 Pag PDFDocument13 pages1 Hidrostática 13 Pag PDFcarajomierda123No ratings yet
- AUTO PID PLUS Manual-Del-Producto-18Document2 pagesAUTO PID PLUS Manual-Del-Producto-18gumlupestiNo ratings yet
- Informe de YodoDocument13 pagesInforme de YodoDANTE ROBERTO FAILOC ALBANNo ratings yet
- Instalacion de Puestas A Tierra Temporal 4 PDF FreeDocument4 pagesInstalacion de Puestas A Tierra Temporal 4 PDF FreeJohn David Buitron ZevallosNo ratings yet
- Palabras SociolingüísticaDocument5 pagesPalabras SociolingüísticaVanessa Zuleta QuinteroNo ratings yet
- 23 Gatillos Mentales PDFDocument42 pages23 Gatillos Mentales PDFFreddy SolanoNo ratings yet
- El ExistencialismoDocument2 pagesEl ExistencialismoRebeca GarciaNo ratings yet
- GLUCOSADocument2 pagesGLUCOSAJherson ZumaetaNo ratings yet
- Intro EdpDocument310 pagesIntro EdpRoberto Davis100% (1)
- Poster Energias Renovables y No Renovables Ver 3Document14 pagesPoster Energias Renovables y No Renovables Ver 3SALVADOR TORO CONTRERASNo ratings yet
- Taller2-Identif RealesDocument4 pagesTaller2-Identif RealesGean Carlos ValenciaNo ratings yet
- Química - CristaleriaDocument16 pagesQuímica - CristaleriaGuille Rmo57% (7)
- 01 - EETT - Obras Provisionales y Preliminares - Rev 0Document18 pages01 - EETT - Obras Provisionales y Preliminares - Rev 0Çs LeonelNo ratings yet
- PDF Resumen de La Resistencia de Ernesto Sabato Por Capitulo - CompressDocument8 pagesPDF Resumen de La Resistencia de Ernesto Sabato Por Capitulo - CompressMiguel AngelNo ratings yet
- Ficha 2 - 1ero - Exp 6Document3 pagesFicha 2 - 1ero - Exp 6Rene QuispeNo ratings yet
- George H. Mead - WKDocument3 pagesGeorge H. Mead - WKce4ci4visualesNo ratings yet
- Priorizacion Educacion Fisica 2022Document44 pagesPriorizacion Educacion Fisica 2022Juan HectorNo ratings yet
- Guia 7 Tercer GradoDocument4 pagesGuia 7 Tercer GradoPOTOLOXNo ratings yet
- REGULACIÓN DE LA PRESIÓN ARTERIAL EN MAMÍFEROS (Perro)Document7 pagesREGULACIÓN DE LA PRESIÓN ARTERIAL EN MAMÍFEROS (Perro)Luz Janet Terrones RamírezNo ratings yet
- Guía de Física (Calor y Temperatura)Document8 pagesGuía de Física (Calor y Temperatura)Roger Enrique Pinzon GarciaNo ratings yet
- Geopolitica Samuel Marquez SectorEDocument33 pagesGeopolitica Samuel Marquez SectorESamuel MarquezNo ratings yet
- BrochadoDocument5 pagesBrochadoMAnuNo ratings yet
- SOLUCIONES Ejercicios MorfologíaDocument13 pagesSOLUCIONES Ejercicios Morfologíamarudomenech100% (1)
- Modelos y PredicciónDocument9 pagesModelos y PredicciónCarlos MartinezNo ratings yet
- AGUDASDocument3 pagesAGUDASsonyNo ratings yet
- Año de La Promoción de La Industria Responsable y Del Compromiso ClimáticoDocument12 pagesAño de La Promoción de La Industria Responsable y Del Compromiso ClimáticoAnonymous mxvASTPNo ratings yet
- Solicitud de Acciones de Edificacion FRENTE Y REVERSO 02-2016Document2 pagesSolicitud de Acciones de Edificacion FRENTE Y REVERSO 02-2016Jose Garcia100% (1)
- Resum Vestuarios SolarDocument7 pagesResum Vestuarios SolarG. MNo ratings yet
- INFORME DE CARACTERIZACION SAN ALEJANDRO Al 10-1-11 PDFDocument32 pagesINFORME DE CARACTERIZACION SAN ALEJANDRO Al 10-1-11 PDFAnthony Alfredo Diaz CardenasNo ratings yet