Professional Documents
Culture Documents
Soluções e propriedades coligativas
Uploaded by
Heloisa FonsecaOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Soluções e propriedades coligativas
Uploaded by
Heloisa FonsecaCopyright:
Available Formats
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof.
Raphael Cruz 6a Lista de Exerccios
SOLUES E PROPRIEDADES COLIGATIVAS
Lista Resolvida e Comentada
Exerccio 1. Em solues binrias, sabendo-se a expresso da grandeza parcial molar de um dos componentes, a do outro pode ser determinada resolvendo-se a equao de Gibbs-Duhem. Tratando-se do potencial qumico, a equao de Gibbs-Duhem a seguinte: d2 = -(n1/n2)d1 = -(x1/x2)d1. o Da expresso do potencial qumico do componente 1, 1 = 1 + RTlnx1 - Bx22, obtm-se: d1 = RTdx1/x1 - 2Bx2dx2, a T e p constantes, o pois 1 sendo o potencial qumico do lquido 1 puro (x1 = 1 e x2 = 0), no depende nem de x1 nem de x2 . Substituindo a expresso de d1 na equao de Gibbs-Duhem, d2 = -(x1/x2)(RTdx1/x1 - 2Bx2dx2), obtm-se: d2 = 2Bx1dx1 - RTdx1/x2. Da relao entre x1 e x2, x1 = 1 - x2, conclui-se: dx1 = -dx2, e a expresso anterior modifica-se, d2 = -2Bx1dx1 + RTdx2/x2, cuja integrao, desde o componente 2 puro (x2 = 1 e x1 = 0) at o componente 2 na soluo, resultar na expresso do potencial qumico do lquido 2: 2 = o + RTlnx2 - Bx12. 2 A partir das expresses dos potenciais qumicos dos lquidos 1 e 2 em soluo, o 1 = 1 + RTlnx1 - Bx22 e 2 = o + RTlnx2 - Bx12, 2 determinam-se as expresses dos correspondentes coeficientes de atividade 1 e 2, pelas relaes: 1 - 1,ideal = RTln1 e 2 - 2,ideal = RTln2, onde 1,ideal e 2,ideal so os potenciais qumicos de 1 e 2 na respectiva e hipottica soluo ideal, expressos por: o 1,ideal = 1 + RTlnx1 e 2 = o + RTlnx2, 2
o em que 1 e o tm o mesmo significado que se extrai das expresses vigentes: so os potenciais 2 qumicos de 1 e 2 puros. Vem, ento: 1 - 1,ideal = -Bx22 e 2 - 2,ideal = -Bx12. Da, RTln1 = -Bx22 e RTln2 = -Bx12, ou 1 = exp(-Bx22/RT) e 2 = exp(-Bx12/RT). As variaes de V, S, G e H referem-se ao processo, isobrico e isotrmico, de obteno de soluo a partir dos componentes 1 e 2 puros. A seguir determinam-se, um por um, V, S e G. H ser obtido ao final pela relao: H = G + TS. A variao de volume entre a soluo e os lquidos puros explicita-se da seguinte maneira: o o V = n1( V 1 - V 1 ) + n2( V 2 - V 2 ),
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
onde n1 e n2 so os nmeros de moles de 1 e 2 com que se preparou a soluo, V 1 e V 2 so seus o o volumes parciais molares e V 1 e V 2 so seus volumes molares quando puros. Os volumes parciais molares relacionam-se com os respectivos potenciais qumicos por: (1/p)T = V 1 e (2/p)T = V 2 . Como, o 1 = 1 + RTlnx1 - Bx22 e 2 = o + RTlnx2 - Bx12, 2 vem: o (1/p)T = ( 1 /p)T e (2/p)T = ( o /p)T, 2
o V 1 = ( 1 /p)T e V 2 = ( o /p)T . 2 o Ora, sendo 1 e o os potenciais qumicos de 1 e 2 puros, conclui-se: 2 o o o ( 1 /p)T = V 1 e ( o /p)T = V 2 , 2 resultando em: o o V 1 = V 1 e V 2 = V 2 e V = 0 A variao de entropia vir da relao: o S = n1( S 1 - S 1 ) + n2( S 2 - S o ), 2 o de que constam as entropias molares dos componentes puros ( S 1 e S o ) e as respectivas entropias 2
parciais molares ( S 1 e S 2 ). Das expresses dos potenciais qumicos de 1 e 2 tambm se obtm: o (1/T)p = ( 1 /T)p + Rlnx1 e (2/T)p = ( o /T)p + Rlnx2. 2 Sabendo que: o o (1/T)p = - S 1 , ( 1 /T)p = - S 1 , (2/T)p = - S 2 e ( o /T)p = - S o , 2 2 chega-se a: o - S 1 = - S 1 + Rlnx1 e - S 2 = - S o + Rlnx1, 2 ou o S 1 - S 1 = -Rlnx1 e S 2 - S o = -Rlnx2, 2 produzindo o seguinte resultado para a variao de entropia: S = -n1Rlnx1 - n2Rlnx2. A variao de G ser a seguinte: o G = n1(1 - 1 ) + n2(2 - o ), 2 com o 1 - 1 = RTlnx1 - Bx22 e 2 - o = RTlnx2 - Bx12, 2 portanto, G = n1(RTlnx1 - Bx22) + n2(RTlnx2 - Bx12). Por ltimo, a variao de entalpia vir da relao H = G - TS, que produz: H = -n1Bx22 - n2Bx12. Observaes: 1) As identidades usadas, o o o o V 1 = (1/p)T =, V 1 = ( 1 /p)T, - S 1 = (1/T)p e - S 1 = ( 1 /T)p, e as equivalentes para o lquido 2, so extenses dos coeficientes: (/p)T = V e (/T)p = - S , que se derivam da relao fundamental d = - S dT + V dp, aplicados aos constituintes de uma soluo.
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
2) A expresso da variao de entropia encontrada, denominada de entropia de mistura, S = n1Rlnx1 - n2Rlnx2., a mesma de uma soluo que fosse ideal, com o potencial qumico de cada lquido dado por: i = o + RTlnxi, embora o sistema analisado neste exerccio no constitua soluo i ideal. Solues no ideais, cuja entropia de mistura seja idntica de uma soluo ideal, so denominadas de solues regulares. Exerccio 2. A cristalizao do benzeno desta soluo iniciar-se- em temperatura menor que a de fuso do benzeno puro (5,5 oC) e que pode ser determinada pela expresso: lnx1 = (Lf/R)(1/T o - 1/Tf), f Com a substituio dos dados, ln0,9 = (9,82x103/8,31)(1/278,5 - 1/Tf), obtm-se: Tf = 271,8 K = -1,2 oC. Portanto, no processo de resfriamento, surgiro os primeiros cristais de benzeno quando a temperatura do sistema alcanar o valor de -1,2 oC. Prosseguindo o resfriamento, mais benzeno cristalizar, alterando a concentrao da soluo residual e diminuindo mais e mais a temperatura do sistema. Interrompendo-se o resfriamento quando a frao molar do benzeno na soluo residual for igual a x1', separando-se esta soluo residual e aquecendo-a a 80,1 oC, sua presso de vapor ser igual a 670 mm Hg. Pela lei de Raoult, a presso p, de vapor da soluo, explicitar-se- por: o p = p 1 x1' (a 80,1 oC) o com p igual a 670 mm Hg e p 1 , a presso de vapor do solvente puro (benzeno puro), igual a 760 mm Hg, pois sua temperatura de ebulio normal tambm igual a 80,1 oC. Logo, o x1' = p/ p 1 = 670/760 = 0,882. A soluo residual ter, portanto, frao molar do tolueno igual a 0,118. Como x1'/x2' = n1'/n2' e n2' = 0,1 mol, vem: n1' = n2'(x1'/x2') = 0,1x0,882/0,118 = 0,747 mol. Agora, de imediato, calcula-se a quantidade cristalizada de benzeno: n1,crist = 0,9 - 0,747 = 0,153 mol. A temperatura que o sistema alcanar, ao cristalizar-se 0,153 mol de benzeno, pode ser determinada aplicando-se a equao: lnx1' = (Lv/R)(1/T o - 1/Tf'), f com os seguintes valores substitudos: ln0,882 = (2350/1,99)(1/278,5 - 1/Tf'), e com o seguinte resultado: Tf' = 270,5 K = -2,5 oC. Em resumo: a cristalizao da soluo iniciar-se- pelo aparecimento de cristais de benzeno a o 1,2 C e prosseguir cristalizando mais e mais benzeno, medida que a temperatura diminui; a -2,5 oC j se obteve 0,153 mol de benzeno slido. A soluo residual, nesta temperatura, conter 0,1 mol de naftaleno e 0,747 mol de benzeno; esta soluo, separada da fase slida, ter, a 80,1 oC, presso de vapor de 670 mm Hg, enquanto a presso de vapor do benzeno puro, na mesma temperatura, ser igual a 760 mm Hg.
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
Exerccio 3. Nesta soluo o nmero de moles de sacarose por 1000 g de gua o seguinte: n2 = m2/M2 = 1,712/343,2 = 0,005 mol. A soluo tem, portanto, concentrao igual a 0,005 molal e, por ser moderadamente diluda, pode ser considerada como soluo ideal, a que se aplicam as seguintes equaes: - aumento da temperatura de ebulio: Teb = Teb - T o = kebm; eb - diminuio da temperatura de fuso: Tf = T o - Tf = kcm; f - presso osmtica: = cRT; onde T o e T o so as temperaturas de ebulio e de fuso do solvente puro (para a gua e sob presso eb f de 1,01 bar, valem 100 oC e 0 oC, respectivamente), Teb e Tf so as temperaturas de ebulio e de fuso da soluo, keb e kc so as constantes ebulioscpica e crioscpica do solvente, expressas por: keb = R(T o )2M1/1000Lv e kc = R(T o )2M1/1000Lf. eb f Os termos que compem os segundos membros destas ltimas equaes ou so constantes ou so propriedades exclusivas do solvente. Para a gua tm-se os seguintes valores: Lv = 2,26x103 J/g ou Lv = 40,7x103 J/mol, Lf = 334 J/g ou Lf = 6,01x103 J/mol, M1 = 18,0 g/mol, T o = 373 K e T o = 273 K, R = 8,31 J/mol.K. eb f Da, resultar: keb = 8,31x3732x18,0/1000x40,7x103 = 0,511 K/mol, kc = 8,31x2732x18,0/1000x6,01x103 = 1,855 K/mol. Ainda sobre os termos que constam das equaes anteriores, tem-se: m a molalidade da soluo (m o nmero de moles do soluto em 1000 g do solvente) e c a molaridade da soluo (c o nmero de moles do soluto por litro da soluo). Para soluo diluda e aquosa pode-se, com boa aproximao, tomar uma unidade de concentrao no lugar da outra. Ento as temperaturas de ebulio e de fuso da soluo referida, sob presso de 1,01 bar, sero as seguintes: Teb = T o + kebm = 100 + 0,513x0,005 = 100,003 oC, eb o Tf = T f - kcm = 0 - 1,854x0,005 = -0,009 oC. A presso osmtica da soluo ter o seguinte valor: = cRT = 0,005x103x8,31x298 = 0,124x105 Pa = 0,124 bar, onde a concentrao c teve que ser usada na unidade de mol/m3. Em mm Hg: = 92,7 mm Hg. Observao: Neste exerccio e em outros foram ou sero aplicadas, a solues ideais, ora as equaes: o V 1 = -RTlnx1 , lnx1 = (Lv/R)(1/Teb - 1/ T o ) e lnx1 = (Lf/R)(1/T o - 1/Tf); eb f ora estas outras: = cRT, Teb = T o + kebm e Tf = T o - km. eb f Afinal de contas, que equaes so vlidas e aplicveis a solues ideais? Responde-se a esta questo de seguinte forma sucinta: as trs ltimas equaes so vlidas exclusivamente para solues ideais diludas, enquanto as trs primeiras so vigorantes para toda e qualquer soluo ideal, diluda ou no. Partindo desta compreenso, pode-se das trs primeiras equa-
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
es, por seqncia de aproximaes e substituies, obter as trs ltimas. Faz-se, portanto e por ltimo, a sugesto de deduzir as equaes finais, a partir das iniciais, adotando-se as seguintes aproximaes: o ln(1 - x2) -x2 -n2/n1 = -m2M2/m1M1 e Vsoluo n1 V 1 , e considerando que: 1) m = m2: m1 = 1000 g e 2) keb = R(T o )2M1/1000Lv e kc = R(T o )2M1/1000Lf. eb f Exerccio 4. A diferena de potencial qumico fornecida pode ser relacionada a termos da expresso do potencial qumico do solvente em soluo. Pois para soluo ideal, como o caso, o 1 - 1 = Rtlnx1, e a partir do valor fornecido, o 1 - 1 = -141 J/mol, determina-se a frao molar do solvente na soluo: lnx1 = -141/RT = -141/8,31x300, x1 = 0,945. Sabendo a concentrao da soluo, obtm-se sua presso de vapor aplicando-se a lei de o o Raoult: p = p 1 x1, onde p 1 , a presso de vapor da gua pura, na temperatura da soluo, tem o valor fornecido de 26,7 mm Hg. Logo, obtm-se o seguinte valor para a presso de vapor da soluo: p = 26,7x0,945 = 22,5 mm Hg. A presso osmtica da soluo determina-se pela equao: o = -(RT/ V 1 )lnx1,
o em que V 1 o volume molar da gua pura (18,1 cm3 /mol = 18,1x10-6 m3). Da, = -(8,31x300/18,1x10-6)ln0,945 = 77,9x105 Pa = 77,9 bar. As temperaturas de ebulio e fuso da soluo viro das expresses: lnx1 = (Lv/R)(1/Teb - 1/T o ) e lnx1 = (Lf/R)(1/T o - 1/Tf), eb f cujos termos tm os seguintes significados e valores: Lv o calor latente de vaporizao da gua (41,2x103 J/mol), Lf o calor latente de fuso da gua (6,02x103 J/mol), T o a temperatura de eb o ebulio normal da gua (373 K), T f a temperatura de fuso da gua sob presso de 1,01 bar (273 K), Teb e Tf so as temperaturas de ebulio e de fuso da soluo, tambm sob presso de 1,01 bar. A substituio dos dados, numa e noutra equao, leva a: ln0,945 = (41,2x103/8,31)(1/Teb - 1/373), onde: Teb = 374,6 K = 101,6 oC; ln0,945 = (6,02/8,31)(1/273 - 1/Tf), e Tf = 267,3 K = -5,7 oC.
Observao: possvel saber se esta soluo de fato uma soluo ideal? Sim, se ficar evidente que ela uma soluo muito diluda. A composio da soluo (pelo menos na hiptese de ser soluo ideal) a seguinte: frao molar da gua: 0,945 e frao molar do soluto: 0,055. Em mil gramas de gua (55,6 moles) haver n2 moles do soluto, dados por:
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
n2 = (x2/x1)n1 = (0,055/0,945)x55,6 = 3,24 moles. V-se, pois, que a soluo 3,24 molal e, portanto, no pode ser considerada diluda o suficiente para que se possa admiti-la como soluo ideal. Dessa forma, os resultados obtidos certamente no so precisos. Exerccio 5. A 110,6 oC a presso de vapor da soluo vale 713 mm Hg e, nesta temperatura, por ser a de ebulio normal do tolueno, a presso de vapor do tolueno puro vale 760 mm Hg. Com estas o informaes e aplicando-se a lei de Raoult, p = p 1 x1, determina-se a frao molar do tolueno na soluo: o x1 = p/p 1 = 713/760 = 0,938. Com o valor de x1, acha-se a frao molar do soluto na soluo, x2 = 1 - x1 = 1 - 0,938 = 0,062. Como x2 = n2/(n1 + n2) = m2/M2(m1/M1 + m2/M2), ou, dividindo o numerador e o denominador do segundo membro por m2 e aps um pequeno algebrismo, obtm-se: M2 = (x1/x2)(m2/m1)M1. Como a razo das massas (m2/m1) a razo das percentagens ponderais (1,5/98,5) e substituindo-se o valor da massa molecular M1 do tolueno (92 g/mol), chega-se ao valor da massa molecular do soluto: M = (0,938/0,062)x(1,5/98,5)x92 = 21,2 g/mol. A temperatura de ebulio normal da soluo pode ser obtida mediante o uso da equao: lnx1 = (Lv/R)(1/Teb - 1/T o ), eb com os seguintes dados e valores: x1 = 0,938, R = 8,31 J/mol.K, T o = 110,6 oC = 383,6 K e Lv = 87,8T o = 87,8x383,6 (J/mol). eb eb Logo, ln0,938 = (87,8x383,6/8,31)(1/Teb - 1/383,6), de que resulta: Teb = 385,9 K = 112,9 oC. Exerccio 6. Em qualquer circunstncia a condio de equilbrio do sistema ser a igualdade entre o potencial qumico do solvente puro e o potencial qumico do solvente na soluo. O potencial qumico do solvente (1) numa soluo ideal expressa-se pela equao: o 1 = 1 + RTlnx1, o em que x1 a frao molar do solvente na soluo e 1 o potencial qumico do solvente puro (x1 = 1). Nota-se, portanto, que o potencial qumico do solvente puro ser sempre maior que o potencial qumico do solvente na soluo, nas mesmas condies de presso e temperatura, pois, na soluo, x1 ser sempre menor que a unidade. Como a membrana de separao entre o solvente puro e a soluo permevel ao solvente e como a lei natural determina ter o menor valor possvel de potencial qumico,
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
o solvente migrar espontaneamente para a soluo, diluindo-a e aumentando seu volume. Esta migrao do solvente o que constitui o efeito osmtico. A diluio, que far o potencial qumico do solvente na soluo cada vez maior, e o eventual aumento da presso sobre a soluo, que tambm far o crescer o potencial do solvente na soluo, pode levar, ao final, 1 tornar-se igual a 1 . Este o caminho natural e espontneo para que o sistema atinja o estado de equilbrio, quando a soluo estar mais diluda e em presso maior que a do solvente puro e ambos na mesma temperatura. Sabendo que o potencial qumico de qualquer sistema aumenta com a presso de acordo com: (/p)T = V , pode-se pensar em evitar o deslocamento do solvente atravs da membrana, aplicandose soluo uma presso adicional, que torne o potencial qumico do solvente na soluo igual ao potencial qumico do solvente puro. Admitindo a soluo como ideal, esta presso adicional que se deve aplicar sobre a soluo (), ser dada por: o = -(RT/ V 1 )lnx1, onde V o volume molar do solvente puro. A substituio dos dados levar ao valor da presso osmtica: = -(8,31x298/18,0x10-6)ln0,995 = 6,90x105 Pa = 6,90 bar. Assim, a aplicao soluo de presso 6,90 bar maior que a presso sobre o solvente puro, garantir o equilbrio entre os dois, atravs da membrana permevel, a 25 oC, e evitar a migrao da gua. Esta presso adicional, necessria ao equilbrio, o que se denomina de presso osmtica. Se se aplicar sobre a soluo presso adicional de valor menor que este, no se poder impedir a migrao do solvente na direo da soluo; se, ao contrrio, aplicar-se soluo presso adicional maior que 6,90 bar, solvente migrar na direo oposta, concentrando a soluo e aumentando a quantidade de solvente puro. Aplicando-se, por exemplo, 10 bar a mais sobre a soluo, quando o equilbrio, atravs da membrana permevel, entre ela e o solvente puro, for atingido, a concentrao da soluo ser: o lnx1' = - V 1 /RT = -10x105x18,0x10-6/8,31x298: x1' = 0,993, e v-se que a frao molar da gua na soluo tornou-se menor, concentrando-a. Observao: A diferena entre o potencial qumico do solvente puro e o do solvente na soluo pode ser determinada pela expresso: o = 1 - = -RTlnx1. Com os valores o resultado o seguinte: = -8,31x298xln0,995 = 12,4 J/mol. A mesma diferena pode ser determinada pelo coeficiente diferencial: (/p)T = V , ou, a T constante, d = V dp, o que a V admitido como constante e igual a V 1 , produz:
o = V 1 , sendo a presso osmtica da soluo. O resultado o seguinte: = 18x10-6x6,90x105 = 12,4 J/mol. Destes resultados pode-se aduzir ilao que talvez contribua para melhor compreender o mecanismo da osmose. Isto , o potencial qumico do solvente na soluo menor 12,4 J/mol que o o 1
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
potencial qumico do solvente puro, estando os dois na mesma temperatura e presso; a aplicao de o presso extra de 6,90 bar sobre a soluo aumentar 1 da mesma quantidade, igualando-o a 1 e tornando possvel o equilbrio entre a soluo e o solvente puro, atravs da membrana permevel. Exerccio 7. Por efeito da osmose a gua migrar para a soluo, diluindo-a e aumentando seu volume e elevando a altura da soluo no tubo em que est contida; fora do tubo admite-se que o volume e a altura do nvel da gua permanecero os mesmos. H, no incio, 20 ml de soluo, com 0,001 mol do soluto por litro, a que corresponde n2 mol do soluto, dado por: n2 = 20x10-3x0,001 = 2x10-5 mol. Sendo o tubo cilndrico, o volume da soluo nele contido se expressa por: Vi = r2L, onde r o raio do tubo e L a extenso do tubo ocupada pela soluo. Tem-se, ento, para L: L = V1/r2 = 20/x12 = 6,37 cm = 6,37x10-2 m. No estado final e de equilbrio entre a gua pura e a soluo, com a soluo, em virtude da osmose, contendo maior quantidade de solvente e, portanto, mais diluda, a nova concentrao da soluo ser dada pela expresso fornecida: c = /RT. Ocorre que tambm se verificar, c = n2/Vf, onde Vf ser o volume alcanado pela soluo aps a osmose e expresso por: Vf = r2(L + h), em que (L + h) a nova altura atingida pela soluo, em virtude da migrao do solvente puro; h, sendo a diferena de nvel entre a soluo e o solvente puro, determina diferena de presso hidrosttica entre a soluo e o solvente. Esta diferena de presso expressa-se por: p = gh, onde , a massa especfica de soluo diluda, praticamente igual do solvente puro (1 g/cm3 = 1000 kg/m3) e g a acelerao da gravidade (9,80 m/s2). Logo, p = 1000x9,80h = 9800h (em Pa). Ora, esta diferena de presso o que se denomina de presso osmtica (a diferena de presso entre a soluo e o solvente puro, necessria ao equilbrio entre os dois, atravs de uma membrana permevel ao solvente). Portanto, = cRT = 9800h, e c = n2/Vf e Vf = r2(L + h), que por substituio, produz: n2/r2(L + h) = 9800h/RT, ou, com os dados conhecidos: 2x10-5/x0,012x(6,37x10-2 + h) = 9800h/8,31x298, que resulta na seguinte equao do segundo grau: 3,96h2 + 0,252h - 0,0637 = 0, cuja raiz vlida a seguinte: h = 9,90x10-2 m = 9,90 cm. Sabendo o desnvel h, entre a soluo e o solvente puro, determina-se:
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
a) o novo volume da soluo: Vf = r2(L + h) = x1x(6,37 + 9,90) = 51,1 cm3; b) a nova concentrao da soluo: c = n/V = 2x10-5/0,0511 = 3,91x10-4 mol/litro = 3,91x10-1 mol/m3, c) a presso osmtica dessa soluo ser: = cRT = 3,91x10-1x8,31x298 = 968 Pa = 7,26 mm Hg. Observao: A presso adicional sobre a soluo, para que fique em equilbrio com o solvente puro, muito pequena - de apenas uns poucos mm Hg, mas o efeito da diluio, que tambm contribui para o atingimento do equilbrio, grande - a concentrao reduz-se a menos da metade, pois a quantidade de gua na soluo mais que dobra. Os dois efeitos - o aumento da presso sobre a soluo e sua diluio - aditiva e conjuntamente, aumentam o valor do potencial qumico do solvente na soluo; quando este potencial qumico igualar-se ao do solvente puro, o equilbrio ser alcanado. Exerccio 8. A temperatura de ebulio de solues ideais relaciona-se com a frao molar do solvente mediante a equao: lnx1 = (Lv/R)(1/Teb - 1/ T o ). eb Tomando-se o valor do calor latente de vaporizao da gua, o da sua temperatura de ebulio normal (100,000 oC = 373,000 K) e o da constante R, tem-se: lnx1 = (40,6x103/8,31)(1/T - 1/373,000), lnx1 = 4885,7/Teb - 13,0931. Aplicando-se nesta expresso os valores da frao molar da gua nas diversas solues, obtmse as respectivas temperaturas de ebulio. Para x1 1igual a 0,999: ln0,999 = 4885,7/Teb - 13,0931, donde: Teb = 373,179 = 100,029 oC. Prosseguindo-se com a soluo seguinte, com x1 igual a 0,998, a equao anterior fornece a seguinte temperatura de ebulio: 373,208 K ou 100,058 oC; quando x2 for igual a 0,997, Teb valer 100,086 oC. Com estes resultados j se pode ver, por comparao com os valores da tabela fornecida, que apenas as duas primeira solues - as mais diludas - so ideais. Para as solues com frao molar do solvente progressivamente menor - as mais concentradas e menos ideais - a equao que relaciona a temperatura de ebulio da soluo com a do solvente puro a seguinte: lna1 = (Lv/R)(1/Teb - 1/ T o ), eb onde a1 a atividade do solvente na soluo. Com os valores de Lv e T o da gua e o de R, a equao anterior fornecer o valor da atividade eb da gua, conhecendo-se a temperatura de ebulio da soluo. A substituio do valores leva a: lna1 = 4885,7/Teb - 13,0931. Para x1 igual ou maior que 0,998 a atividade da gua ser sua prpria frao molar, pois, neste intervalo de concentrao, as solues sero ideais. Para x1 igual a 0,997 e Teb igual a 100,170, ou 373,320 K, obtm-se o seguinte valor para a1: lna1 = 4885,7/373,320 - 13,0931, a1 = 0,994.
UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Fsico-Qumica Fsico-Qumica VII Prof. Raphael Cruz 6a Lista de Exerccios
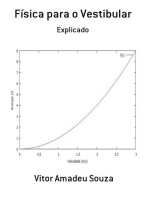
Sabendo que o coeficiente de atividade se define por: 1 = a1/x1, para a soluo considerada, com x1 igual a 0,997, vem: 1 = 0,994/0,997 = 0,997. Operando-se anloga e sucessivamente com as outras solues, determinam-se os valores de a1 e 1 de todas elas, podendo-se organizar a seguinte tabela: x1 T (oC) a1 1
o eb
1,000 100,000 1,000 1,000
0,999 100,029 0,999 1,000
0,998 100,058 0,998 1,000
0,997 100,170 0,994 0,997
0,996 100,285 0,990 0,994
1.20
0,995 100,401 0,986 0,991
0,990 101,196 0,959 0,969
0,980 103,285 0,892 0,910
Com os valores de 1 e x1 traa-se a curva que d a dependncia do coeficiente de atividade da gua com a concentrao. a que consta do grfico a seguir:
1.10
Exerccio 9.
1.00
Sabendo o valor da presso de vapor da l rea soluo (98,5 mm Hg), a atividade do metanol na o ol u s soluo pode ser determinada pela lei de Raoult 0.90 generalizada: o p = p 1 a1, 0.80 donde: 0.97 0.98 0.99 1.00 o a1 = p/p 1 = 98,5/100 = 0,985. x1 O coeficiente de atividade do metanol vir de: 1 = a1/x1 = 0,985/0,953 = 1,034. O coeficiente osmtico de Bjerrum definido por: g = /ideal, onde a real e efetiva presso osmtica da soluo, expressa por: = -(RT/ V 1)lna1, sendo V 1 o volume parcial molar do metanol na soluo (41,25 cm3 /mol), e ideal a presso osmtica da hipottica soluo ideal, dada por: o ideal = -(RT/ V 1 )lnx1,
o sendo V 1 o volume molar do metanol puro (40,49 cm3 /mol). Da, vir: o g = /ideal = ( V 1 lna1)/( V 1lnx1 ). Com os valores, g = (40,49xln0,985)/(41,25ln0,953) = 0,3082.
soluo ideal
Exerccio 10. Esta questo ser comentada em sala!
You might also like
- Reações multicomponentes e multifásicasDocument37 pagesReações multicomponentes e multifásicasCarlosNo ratings yet
- Equação de Nernst 2014Document9 pagesEquação de Nernst 2014Evilasio CostaNo ratings yet
- Aula - 13 Evaporadores Exemplo 2 (EPE Alto) Multiplo EfeitoDocument22 pagesAula - 13 Evaporadores Exemplo 2 (EPE Alto) Multiplo EfeitoJULIA BORGES CAMARGOSNo ratings yet
- 1 Propriedade Parcial e Mistura Gases IdeaisDocument59 pages1 Propriedade Parcial e Mistura Gases IdeaisMiria ReisNo ratings yet
- Flash lista exercícios ELVDocument3 pagesFlash lista exercícios ELVGuilherme FernandoNo ratings yet
- UNIVERSIDADE FEDERAL FLUMINENSE Departamento de Físico-Química Físico-Química VII – Prof. Raphael Cruz 4a Lista de ExercíciosDocument22 pagesUNIVERSIDADE FEDERAL FLUMINENSE Departamento de Físico-Química Físico-Química VII – Prof. Raphael Cruz 4a Lista de ExercíciosClaudio VictorNo ratings yet
- Exercicios Propostos Sala de Aula Resolucao FRSensatoDocument6 pagesExercicios Propostos Sala de Aula Resolucao FRSensatomalikvieNo ratings yet
- QuimicaII FRSensato Noturno P2 1osem 2008 ResolucaoDocument2 pagesQuimicaII FRSensato Noturno P2 1osem 2008 ResolucaoevertonsktNo ratings yet
- Entropia PDFDocument19 pagesEntropia PDFBira VieiraNo ratings yet
- Relatório de Termodinâmica e SolubolubilidadeDocument8 pagesRelatório de Termodinâmica e Solubolubilidadeadriano souzaNo ratings yet
- Perito Criminal Federal - CESPE - 1997 - Área 6 (Química Apenas) - Resolução ComentadaDocument35 pagesPerito Criminal Federal - CESPE - 1997 - Área 6 (Química Apenas) - Resolução ComentadaRobson Timoteo Damasceno0% (1)
- Experimento 1-Solubilidade e TermodinâmicaDocument6 pagesExperimento 1-Solubilidade e TermodinâmicaJosé GuilhermeNo ratings yet
- Lista 8 - ResolvidaDocument13 pagesLista 8 - Resolvidarobertamarla0% (1)
- Rumo ao ITA - 1a Lei da TermodinâmicaDocument5 pagesRumo ao ITA - 1a Lei da TermodinâmicaviniiboyNo ratings yet
- Resumo Sobre Propriedade Dos Gases - IIIDocument4 pagesResumo Sobre Propriedade Dos Gases - IIIRobson Timoteo DamascenoNo ratings yet
- Energia cinética e velocidade de moléculas em gás idealDocument2 pagesEnergia cinética e velocidade de moléculas em gás idealLucasNo ratings yet
- 2019 2f ResolucaoDocument6 pages2019 2f ResolucaosofiaarosoNo ratings yet
- 11394418082016termodinamica Quimica Aula 9Document10 pages11394418082016termodinamica Quimica Aula 9Nelson Miguel VézuaNo ratings yet
- Simulado Sobre Transformações Químicas e Energia Concurso Professor de Química 1Document5 pagesSimulado Sobre Transformações Químicas e Energia Concurso Professor de Química 1Anonymous aPzoIa4No ratings yet
- Relatório 1, Calorimetria UC Físico-Química Versão FinalDocument7 pagesRelatório 1, Calorimetria UC Físico-Química Versão FinalAna Paula SousaNo ratings yet
- ENTROPIA DE MISTURAS E SISTEMAS MULTICOMPONENTESDocument28 pagesENTROPIA DE MISTURAS E SISTEMAS MULTICOMPONENTESDavid Santos de França33% (3)
- Basica Equilibrio TeoriaDocument26 pagesBasica Equilibrio TeoriaErica ItoNo ratings yet
- Química discursiva sobre moléculas polares e apolaresDocument7 pagesQuímica discursiva sobre moléculas polares e apolaresWylson AlmeidaNo ratings yet
- Volume Molar ParcialDocument4 pagesVolume Molar ParcialcujeraNo ratings yet
- Solução ideal e propriedades coligativasDocument15 pagesSolução ideal e propriedades coligativasLucas LiraNo ratings yet
- Determinação da entalpia de neutralizaçãoDocument13 pagesDeterminação da entalpia de neutralizaçãoHélio BellagambaNo ratings yet
- Multicomponent, homogeneous nonreacting systems: solutionsDocument44 pagesMulticomponent, homogeneous nonreacting systems: solutionsThays AlvesNo ratings yet
- Cap 11 Moyses FisicaDocument8 pagesCap 11 Moyses FisicaLeonardo Batista RibeiroNo ratings yet
- Lista 4Document4 pagesLista 4Cíntia SalibNo ratings yet
- Cálculo da entropia em processos termodinâmicosDocument7 pagesCálculo da entropia em processos termodinâmicosThiago MenzonattoNo ratings yet
- Aula 2 Difusão em Estado Não EstacionárioDocument45 pagesAula 2 Difusão em Estado Não EstacionárioRamon da Silva GonçalvesNo ratings yet
- Temodinamica Aula 9 - Tabelas TermoDocument47 pagesTemodinamica Aula 9 - Tabelas TermoSidsambangaNo ratings yet
- PME3238 RL ConveccaoDocument6 pagesPME3238 RL ConveccaoPrince of persia 3No ratings yet
- Resolucao Quimica FisicaDocument10 pagesResolucao Quimica FisicaSamuel JosexNo ratings yet
- Termodinâmica Aula 2 - Equações e Experimento de Joule-ThomsonDocument46 pagesTermodinâmica Aula 2 - Equações e Experimento de Joule-ThomsonANDRE LUIZ RAMOS LINONo ratings yet
- Gas Real - Alunos 2020.1Document21 pagesGas Real - Alunos 2020.1José Gabriel De Almeida VieiraNo ratings yet
- Perigos do gás sulfídricoDocument5 pagesPerigos do gás sulfídricoldx1982No ratings yet
- Reações Irreverssíveia A Vol VarDocument6 pagesReações Irreverssíveia A Vol VarMarcos SilvaNo ratings yet
- Lista 3Document3 pagesLista 3Marcello SeveroNo ratings yet
- Lista 1Document3 pagesLista 1flaviagoncalvesNo ratings yet
- Termodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem - 2005 Resolução Comentada Prof. Fabrício R. SensatoDocument6 pagesTermodinâmica Química Prova P1, Eng. Materiais, Noturno, 2º Sem - 2005 Resolução Comentada Prof. Fabrício R. SensatoUelder Jeferson SantosNo ratings yet
- Termodinâmica química - expansão de CO2Document6 pagesTermodinâmica química - expansão de CO2Claudenor Piedade100% (1)
- Operações unitárias de evaporação e separação de componentes em misturasDocument16 pagesOperações unitárias de evaporação e separação de componentes em misturasAndressa BritoNo ratings yet
- RELATÓRIO 2-G3-TermodinâmicaDocument18 pagesRELATÓRIO 2-G3-TermodinâmicaJúlia Hartmann MozeticNo ratings yet
- Potência compressor gás ideal, virial, PRDocument23 pagesPotência compressor gás ideal, virial, PRCarlos AdrianoNo ratings yet
- Quimica - Misturas SimplesDocument35 pagesQuimica - Misturas SimplesMarcio100% (1)
- Equilíbrio Químico: Estudo das Reações ReversíveisDocument10 pagesEquilíbrio Químico: Estudo das Reações ReversíveisJonacir NovaesNo ratings yet
- 2 - Termodinâmica Dassoluções Não-Eletrolíticas - Soluções IdeaisDocument3 pages2 - Termodinâmica Dassoluções Não-Eletrolíticas - Soluções IdeaisJuliane Froncheti de MouraNo ratings yet
- BET Adsorção IsotermaDocument10 pagesBET Adsorção IsotermaJunin Oliveira100% (2)
- Determinação da energia de dissolução de cloretos de metais alcalinosDocument13 pagesDeterminação da energia de dissolução de cloretos de metais alcalinosFRANCISCO C.N. SANTOS100% (1)
- Prova 2017.1Document2 pagesProva 2017.1ISRAEL DA LUZ RODRIGUESNo ratings yet
- Lista de Exercícios - Termodinâmica Dos Materiais - Comentários - FDocument9 pagesLista de Exercícios - Termodinâmica Dos Materiais - Comentários - FLeandro FortunatoNo ratings yet
- Microbiologia ScientificDocument10 pagesMicrobiologia ScientificHeloisa FonsecaNo ratings yet
- Fabricação de polpa e néctar de frutas: processos e operaçõesDocument7 pagesFabricação de polpa e néctar de frutas: processos e operaçõesInácio SantosNo ratings yet
- WEB - Cartilha Eficiência Energética - 15x21cm4Document28 pagesWEB - Cartilha Eficiência Energética - 15x21cm4Heloisa FonsecaNo ratings yet
- Apostila Boas Praticas Modulo 1Document28 pagesApostila Boas Praticas Modulo 1Thiago LucasNo ratings yet
- Curso de Gestão de Pessoas PDF - 01Document76 pagesCurso de Gestão de Pessoas PDF - 01welderlemes3090No ratings yet
- CTB - ResumoDocument34 pagesCTB - ResumoHeloisa FonsecaNo ratings yet
- 1522090484EBOOK 2 Guia Pratico Boas Praticas FabricacaoDocument13 pages1522090484EBOOK 2 Guia Pratico Boas Praticas FabricacaoHeloisa FonsecaNo ratings yet
- 1522090484EBOOK 2 Guia Pratico Boas Praticas FabricacaoDocument13 pages1522090484EBOOK 2 Guia Pratico Boas Praticas FabricacaoHeloisa FonsecaNo ratings yet
- Administração de Recursos Humanos: Equilíbrio Organizacional e Funções do RHDocument1,120 pagesAdministração de Recursos Humanos: Equilíbrio Organizacional e Funções do RHBrunaNo ratings yet
- ADM DE MATERIAIS - Livro Castanhal PDFDocument106 pagesADM DE MATERIAIS - Livro Castanhal PDFAnonymous fn9QPGNo ratings yet
- Lei 6583 - 1978 Cria CFN-CRNDocument4 pagesLei 6583 - 1978 Cria CFN-CRNglaucialimaNo ratings yet
- RESOLUÇÃO CFN 304/2003 CRITÉRIOS DIETÉTICADocument3 pagesRESOLUÇÃO CFN 304/2003 CRITÉRIOS DIETÉTICACristianeNo ratings yet
- Plano de negócios da Padaria AlternativaDocument71 pagesPlano de negócios da Padaria AlternativaHeloisa FonsecaNo ratings yet
- 295 PN Paes Da ColoniaDocument10 pages295 PN Paes Da ColoniaSecondhand PortugalNo ratings yet
- RESOLUÇÃO CFN 304/2003 CRITÉRIOS DIETÉTICADocument3 pagesRESOLUÇÃO CFN 304/2003 CRITÉRIOS DIETÉTICACristianeNo ratings yet
- Determinacao Dos Constituintes Principais e de MicronutrientesDocument41 pagesDeterminacao Dos Constituintes Principais e de MicronutrientesHeloisa FonsecaNo ratings yet
- Daikin RelatorioDocument13 pagesDaikin RelatorioAlex SilvaNo ratings yet
- Manual de Synop emDocument42 pagesManual de Synop emIzinha99100% (1)
- Calorímetro determina calor específicoDocument10 pagesCalorímetro determina calor específicoBrenda MeloNo ratings yet
- Dilatação Térmica e Calorimetria - Questões e ProblemasDocument4 pagesDilatação Térmica e Calorimetria - Questões e ProblemasThyale MeloNo ratings yet
- Calor: transferência e conversão de unidadesDocument25 pagesCalor: transferência e conversão de unidadesEdnaldo SilvaNo ratings yet
- NBR 6467 - 1987 - Agregado - Determinação Do Inchamento de Agregado MiúdoDocument5 pagesNBR 6467 - 1987 - Agregado - Determinação Do Inchamento de Agregado MiúdoHélio JúlioNo ratings yet
- Exercicio Aula Remota 37 e 38Document3 pagesExercicio Aula Remota 37 e 38Tauã PaternostroNo ratings yet
- UFF - Físico-Química I - Lista de ExercíciosDocument3 pagesUFF - Físico-Química I - Lista de ExercíciosBruno PaivaNo ratings yet
- 2º ANO Revisão para A AV2Document15 pages2º ANO Revisão para A AV2Erman NaumNo ratings yet
- Noções Básicas de Transferência de CalorDocument12 pagesNoções Básicas de Transferência de CalorRodrigues MillsNo ratings yet
- Química Analítica F - Notas de aula sobre equilíbrios e titulaçõesDocument118 pagesQuímica Analítica F - Notas de aula sobre equilíbrios e titulaçõesVitor Jurciukonis CelescuekciNo ratings yet
- Determinação Da Eficiência Energética de Um Sistema Bomba de CalorDocument16 pagesDeterminação Da Eficiência Energética de Um Sistema Bomba de Calorgino_silva_1No ratings yet
- Secagem de sólido com ar de secagemDocument51 pagesSecagem de sólido com ar de secagemNazareno Braga100% (1)
- Propagação de CalorDocument2 pagesPropagação de CalorMarisa Cezar PereiraNo ratings yet
- Relatório de Físico-Química Experimental 1-2Document15 pagesRelatório de Físico-Química Experimental 1-2jpaullogamaNo ratings yet
- Aula 6 - Temperaturas Extremas - CalorDocument4 pagesAula 6 - Temperaturas Extremas - CalorPedro Cordeiro NevesNo ratings yet
- FT Aquatherm 220621 15Document9 pagesFT Aquatherm 220621 15Heliton FerezinNo ratings yet
- Química Analítica QuantitativaDocument122 pagesQuímica Analítica QuantitativaMax SouzaNo ratings yet
- Química Analítica UFRGSDocument152 pagesQuímica Analítica UFRGSrubensjunior1652No ratings yet
- Relatório - Equação Termométrica - Laboratório VirtualDocument7 pagesRelatório - Equação Termométrica - Laboratório VirtualJosé Rosa de Souza Farias100% (2)
- Atividade 1 TermodinâmicaDocument6 pagesAtividade 1 TermodinâmicaJoão VictorNo ratings yet
- Calores Latentes de Substâncias PurasDocument10 pagesCalores Latentes de Substâncias PurasVictor FelipeNo ratings yet
- Piloto privado meteorologia testeDocument8 pagesPiloto privado meteorologia testeWillian NascimentoNo ratings yet
- Avaliação de CalorDocument4 pagesAvaliação de CalorDenilson SantosNo ratings yet
- Exercícios ELVDocument1 pageExercícios ELVCarolBorgesNo ratings yet
- Destilação Flash: Separação Rápida por Vaporização ParcialDocument16 pagesDestilação Flash: Separação Rápida por Vaporização ParcialRinaldo MendesNo ratings yet
- 345129-Exercicios NTU 20junho2016 24nov2016COMPLETO (Cortes)Document6 pages345129-Exercicios NTU 20junho2016 24nov2016COMPLETO (Cortes)Guilherme RighetoNo ratings yet
- Taxa de transferência de calor entre cilindros concêntricos preenchidos com ar ou águaDocument11 pagesTaxa de transferência de calor entre cilindros concêntricos preenchidos com ar ou águaLaboratório Siap ParacatuNo ratings yet
- Máquinas Térmicas - Exercícios de MEC011Document2 pagesMáquinas Térmicas - Exercícios de MEC011ElenKarolinaNo ratings yet
- ATIVIDADE Semana 5Document3 pagesATIVIDADE Semana 5gregoey gomesNo ratings yet